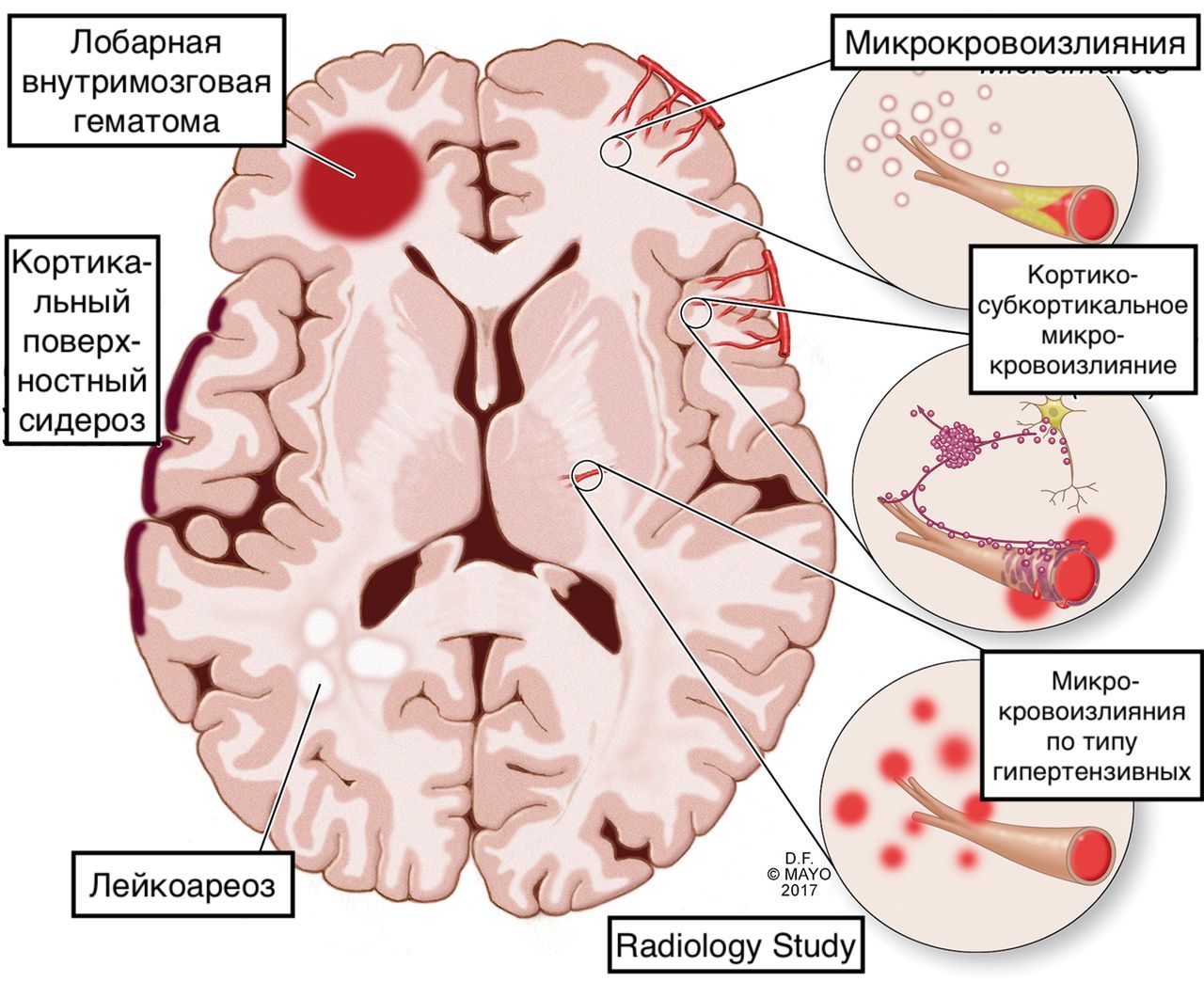
амилоидоз головного мозга мрт
Амилоидоз головного мозга мрт
а) Терминология:
1. Сокращения:
• Церебральная амилоидная ангиопатия (ЦАА)
2. Синонимы:
• «Конгофильная ангиопатия», церебральный амилоидоз
3. Определение:
• ЦАА является частой причиной «спонтанных» долевых кровоизлияний у пожилых
• Наблюдается три морфологических варианта отложения амилоида в головном мозге:
о ЦАА (часто)
о Амилоидома (нечасто)
о Воспалительная ЦАА: ангиит, обусловленный отложением β-а-милоида (БАА) с диффузными воспалительными изменениями белого вещества (редко)
1. Общие характеристики амилоидоза головного мозга:
• Лучший диагностический критерий:
о Пациенты, страдающие деменцией и имеющие нормальное артериальное давление:
— Лобарное кровоизлияние(я) различной давности
— Мультифокальные кортикальные/субкортикальные микрокровоизлияния в виде «черных точек» при МРТ на Т2* или SWI
• Локализация:
о Кора/субкортикальное БВ (переход между серым и белым веществом)
о При аутопсии наиболее часто выявляется поражение теменных + затылочных долей; по данным диагностической визуализации-лобные + височные
о Менее частая локализация патологических изменений-ствол головного мозга, глубокие ядра, мозжечок, гиппокамп
• Размеры:
о Для острого долевого кровоизлияния более характерны крупные размеры
о Гипоинтенсивные очаги на Т2*/последовательностях, взвешенных по восприимчивости (участки «выцветания» изображения) характеризуют хронические микрокровоизлияния (не специфичные для ЦАА):
— Микрокро- и макрокровоизлияния могут представлять собой отличительные признаки ЦАА САА
• Морфология:
о Острые гематомы имеют крупные размеры, часто неправильную форму в зависимости от скорости оседания эритроцитов
2. КТ при амилоидозе головного мозга:
• Бесконтрастная КТ:
о Разрозненные или сливные очаги кровоизлияния кортикальной/субкортикальной локализации с неровными границами, окруженные перифокальным отеком
о Кровоизлияние может прорываться в субарахноидальное пространство или в полость желудочков
о Пациенты могут поступать в лечебное учреждение с конвекситальными субарахноидальными кровоизлияниями
о Редко: гиральная кальцификация
о Часто встречается генерализованная атрофия мозговой ткани
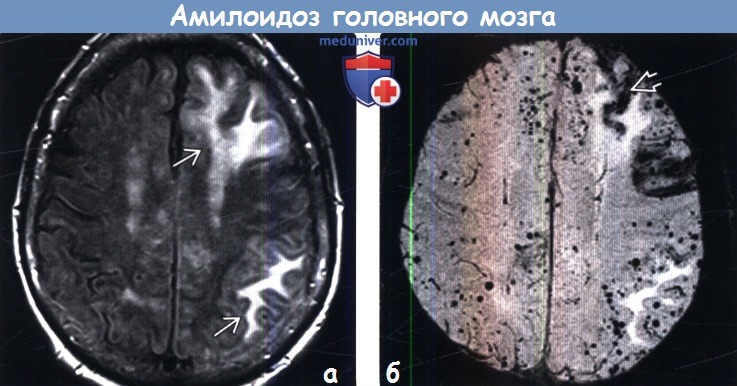
(б) MPT, SWI, аксиальный срез: у этой же пациентки определяются многочисленные очаги артефакта восприимчивости по типу «выцветания» изображения, представляющие собой типичные при ЦАА микрокровоизлияния в паренхиму мозга. Линейный гипоинтенсивный участок представляет собой зону поверхностного сидероза.
При биопсии была диагностирована воспалительная форма амилоидоза. Ответ на стероидную терапию был удовлетворительным.
3. МРТ при амилоидозе головного мозга:
• Т1-ВИ:
о Лобарная гематома (характеристики сигнала варьируют в зависимости от ее давности)
• Т2-ВИ:
о Острая гематома, изо-/гипоинтенсивный сигнал:
— У 1 /3 пациентов имеются признаки старых кровоизлияний (долевых, петехиальных), визуализируемых, как мультифокальные «черные точки»
о Сочетается с разрозненными/сливными очагами поражения БВ почти в 70% случаев
о Редкие формы: не геморрагическое диффузное воспаление со сливными гиперинтенсивными очагами в структуре БВ:
— Острый вазогенный отек белого вещества может визуализироваться при острых воспалительных формах:
Визуализационная картина может имитировать синдром задней обратимой энцефалопатии (СЗОЭ)
— Асимметричный характер повреждения и наличие множественных микрокровоизлияний позволяют выдвинуть предположение о наличии ЦАА
— Отсутствие типичных для СЗОЭ предрасполагающих факторов (например, гипертонический криз, иммунодепрессорная терапия)
— Острая воспалительная ЦАА = ответ на стероидную терапию
• Т2* GRE:
о Мультифокальные «черные точки»
• Постконтрастные Т1-ВИ:
о ЦАА, долевые кровоизлияния обычно не контрастируются
о Амилоидома (фокальное объемное образование[я] без геморрагического компонента):
— Масс-эффект обычно минимальный/умеренный
— Возможно умеренно интенсивное/выраженное контрастирование, что может имитировать новообразование
— Часто распространяются от медиальной к латеральной желудочковой стенке с тонкими радиальными накапливающими контраст краями
— Редко: инфильтрация
о Воспалительная форма (БАА):
— Возможно контрастное усиление борозд, цистерн
• Изображение, взвешенное по магнитной восприимчивости (SWI):
о Мультифокальные гипоинтенсивные очаги (микрокровоизлияния) сходные с таковыми на Т2* GRE, но данный метод более чувствителен в их выявлении
4. Радионуклидная диагностика:
• 99m Tc-ECD ОФЭКТ: снижение церебральной перфузии
• Агенты для ПЭТ визуализации амилоидоза (меченный углерод-11 питтсбургского состава В [11С PiB])
о Демонстрация накопления β-амилоида
5. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о Бесконтрастная КТ = лучший скрининговый метод (для визуализации острых кровоизлияние)
о МРТ с Т2* или SWI для оценки неострой патологии (деменция)
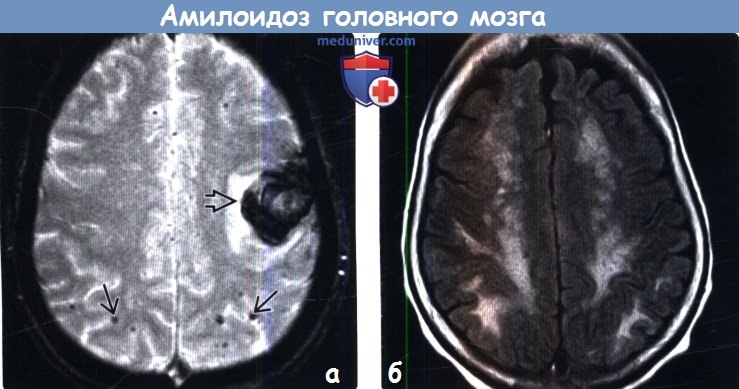
(б) МРТ, FLAIR, аксиальный срез: у пациента 73 лет с WFF определяются типичные сливные очаги в структуре белого вещества, которые могут визуализироваться при церебральной амилоидной ангиопатии и атеросклерозе (хроническая микроваскулярная ишемия). По данным SWI изображений (не представлены) были подтверждены множественные микрокровоизлияния, типичные для ЦАА, 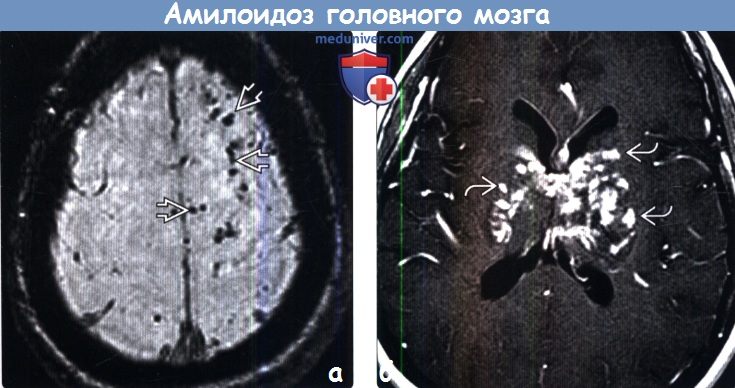
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: билатерально в структуре базальных ганглиев, а также перивентрикулярного белого вещества периваскулярно по ходу сосудистых структур определяются множественные мелкие очаги контрастного усиления с умеренным масс-эффектом. Такие признаки («амилоидомы», имитирующие неопластический процесс или возможную атипичную инфекционную/воспалительную этиологию) наблюдаются в меньшинстве случаев амилоидоза.
в) Дифференциальная диагностика:
3. Течение и прогноз:
• Неоднократные рецидивирующие кровоизлияния
• Прогрессивное ухудшение когнитивных функций
4. Лечение:
• Эвакуация фокальной гематомы при возрасте пациента
Видео этиология, патогенез амилоидоза
Редактор: Искандер Милевски. Дата публикации: 18.3.2019
Амилоидоз головного мозга
Амилоидоз головного мозга или церебральная амилоидная ангиопатия (ЦАА) является частой причиной «спонтанных» долевых кровоизлияний у пожилых. Синонимы:
Наблюдается три морфологических варианта отложения амилоида в головном мозге:
Эпидемиология
20-40%-у пожилых пациентов без клинических проявлений (выявляемые при аутопсии) и у 90%-пациентов с болезнью Альцгеймера. Часто встречается при синдроме Дауна.
Демография
Классификация амилоидоза по ВОЗ:
Патология
ЦАА обусловлена накоплением агрегированного р-амилоида в сосудах мелкого калибра
Амилоидоз = редкое системное заболевание, вызванное внеклеточным отложением р-амилоида
В 10-20% наблюдается локализованная форма с поражением структур ЦНС
Может иметь первичный/идиопатический генез
Может иметь вторичный генез (при диализе, медуллярном раке щитовидной железы, сахарном диабете 2 типа)
Макроскопические особенности:
Микроскопические особенности:
Генетика
Спорадический характер (амилоид типа р)
— Аллель АРОЕ*Е4 связана с развитием ЦСА-ассоциированных кровоизлиянии
— Пациенты пожилого возраста, ± болезнь Альцгеймера.
Наследственные внутримозговые кровоизлияния с амилоидозом.
— Аутосомно-доминантный тип наследования
— Белок-предшественник амилоида кодируется геном АРР, локализующимся в 21 хромосоме
— Выделяют голландский, британский, фламандский, итальянскии и другие типы
— Более тяжелое и более раннее начало, чем при спорадической форме
Клинические проявления
Острые: инсультоподобные клинические проявления при спонтанном долевом внутричерепном кровоизлиянии.
Хронические: деменция (ЦДЛ)
Бостонские критерии для постановки ЦАА:
Радиологические находки:
Пациенты, страдающие деменцией и имеющие нормальное артериальное давление
— Лобарное кровоизлияние различной давности
— Мультифокальные кортикальные/субкортикальный микрокровоизлияния в виде «черных точек» при МРТ на Т2* или SWI.
Локализация
Кора/субкортикальное белое вещество (переход между серым и белым веществом).
При аутопсии наиболее часто выявляется поражение теменных + затылочных долей, по данным диагностической визуализации-лобные + височные
Размеры
Для острого долевого кровоизлияния более характерны крупные размеры
Гипоинтенсивные очаги на Т2* характеризуют хронические микрокровоизлияния (не специфичные для ЦАА)
Морфология:
Острые гематомы имеют крупные размеры, часто неправильную форму в зависимости от скорости оседания эритроцитов
Компьютерная томография (КТ)
Магнитно-резонасная томография (MPT).
Радионуклидная диагностика
Дифференциальный диагноз:
Гипертензивные микрокровоизлияния
Множественные кавернозные мальформации
Ишемический инсульт с микрокровоизлиянием
Другие причины появления мультифокальных «черных точек»:
Травматическое диффузное аксональное повреждение
Метастатические поражения с геморрагическим компонентом.
Микроэмболы из искуственных клапанов сердца.
Острая гиперэнтензивная энцефалопатия
CADASIL
Церебральная амилоидная ангиопатия
Церебральная амилоидная ангиопатия (ЦАА) – цереброваскулярное заболевание, причиной которого является накопление церебрального амилоида-бета (Ав) в средней оболочке и адвентиции лептоменингиальных и кортикальных сосудов головного мозга. Нарушение прочности сосудистой стенки у пожилых нормотензивных пациентов может приводить к лобарным интрацеребральным кровоизлияниям. Данное заболевание, наряду с болезнью Альцгеймера, принадлежит группе нозологий, характеризующихся отложением амилоида в головном мозге.
Эпидемиология
Церебральная амилоидная ангиопатия подразделяется на спорадические и семейные формы.
Спорадическая ЦАА
Спорадическая ЦАА – частая (16%) случайная находка у пожилых пациентов при проведении МРТ с последовательностью градиентного эха. При аутопсических исследованиях ЦАА выявляется у 5-9% среди пациентов в возрасте 60-69 лет, и у 43-58% среди пациентов старше 90 лет.
При аутопсии пациентов со всеми признаками болезни Альцгеймера ЦАА подтверждалась в 90% случаев.
Важно, что данная форма обычна не ассоциирована с системным амилоидозом.
Семейная ЦАА
Под семейной ЦАА описывается группа очень редких заболеваний, которые преимущественно являются аутосомно-доминантными состояниями. Большая их часть встречается внутри определенных семей, и главное их отличие от спорадической формы – начало в более раннем возрасте, обычно в среднем или позднем среднем. Более того, данный вид ЦАА может быть также частью мультисистемных (или с преимущественным поражением ЦНС) генетических заболеваний.
Примеры семейной формы ЦАА:
Клиническое представление
Вовлечение кортикальных сосудов приводит к интрацеребральным кровоизлияниям (чаще к лобарным, нежели мозжечковым), что может проявляться как инсульт или небольшие лобарные микрокровоизлияния, которые часто можно выявить радиологически. Повреждение сосудов в кортико-субкортикальных областях может стать причиной ишемической лейкоэнцефалопатии. Считается, что лобарные церебральные микрокровоизлияния и ишемическая лейкоэнцефалопатия играют роль в развитии когнитивных нарушений, которые не зависят от болезни Альцгеймера, хотя повторяющиеся лобарные кровоизлияния также могут приводить к постепенному снижению когнитивных функций.
Возможно наличие необычной воспалительной реакции, проявляющаяся в подостром состоянии с когнитивными нарушениями, судорогами, головной болью инсульто-подобными эпизодами (без кровоизлияния). Данный симптомокомплекс получил название ЦАА-опосредованное воспаление и обсуждается отдельно.
Также имеются сообщения о массоподобном поражении, получившим название церебральная амилоидома. Не следует путать с церебральным амилоидозом, являющимся проявлением системного амилоидоза.
Патология
ЦАА характеризуется отложением амилоида в средней оболочке и адвентиции лептоменингиальных и кортикальных артерий головного мозга малого и среднего калибра. На фоне фибриноидной дегенерации происходит отделение интимы от средней оболочки и образование микроаневризм.
Существует большое количество различных белков, участвующие в процессе интраваскулярного отложения амилоида, однако, наиболее распространенным (особенно в случае спорадических форм ЦАА) является Ав, короткий пептид из 42 аминокислот, отщепляющийся от белка-предшественника амилоида (APP), ген которого расположен в 21 хромосоме.
Связь с другими заболеваниями
Радиографические признаки
Радиографические признаки отражают различные проявления ЦАА:
Диагностические критерии
Бостонские критерии и их модификаци включают сочетание клинических, радиологических и патологоанатомических критериев, которые используются для оценки вероятности наличия церебральной амилоидной ангиопатии. Эти критерии требуют наличия биопсии и данных МР исследования. Кроме этого могут использоваться Эдинбургские критерии для внутримозговых кровоизлияний, особенно у пациентов не прошедших МР исследование.
β-амилоид: невидимый враг или тайный защитник? Запутанная тропка болезни Альцгеймера
Авторы
Редакторы
Болезнь Альцгемера — нейродегенеративное заболевание с крайне удручающими симптомами: пациенты становятся беспомощными, утрачивают связь с реальностью и даже теряют способность говорить. В 2016 году научным коллективам удалось немного продвинуться как в понимании молекулярных основ этой патологии, так и в разработке способов борьбы с ней. В частности, были проведены клинические испытания сразу двух препаратов, направленных на уничтожение β-амилоидных частиц — структур, связанных с развитием болезни Альцгеймера. В то же время эксперименты на живых организмах подтвердили предположение о том, что β-амилоид обладает полезными для нашего организма свойствами — он является важным элементом врожденного иммунитета.
12 биологических новостей в картинках
Вообще, мы серьезные люди. Гранит науки хрустит на наших зубах. Мы освещаем такие суровые, такие сложные закоулки биологического знания, до которых не дотянулись фонари других научно-популярных сайтов. Но иногда нам так хочется подурачиться. И рассказать о науке веселым языком, показать ее под другим углом. Нарисовать забавных картинок, написать легкий и смешной текст. Поэтому мы и открыли новую рубрику — «12 биологических новостей в картинках».
Интеллектуальный партнер этих иллюстрированных рассказов — АО РВК.
Болезнь Альцгеймера, как правило, развивается у людей старше 65 лет. Внешне она проявляется триадой «афазия-апраксия-агнозия»: человек утрачивает способность совершать элементарные действия, распознавать предметы и лица людей, нарушается его речевая активность. При этом отклонениям в поведении пациентов предшествуют физиологические изменения в их организме. За 10–15 лет до первых проявлений заболевания в мозге начинают откладываться так называемые β-амилоидные бляшки. Эти характерные скопления сформированы преимущественно β-амилоидом — пептидом, образующимся особым ферментативным расщеплением белка — предшественника β-амилоида. Многие исследователи считают, что эти образования способствуют прогрессирующей дегенерации клеток мозга, в связи с чем разрабатывают лекарства, направленные на уничтожение или уменьшение числа β-амилоидных скоплений. В 2016 году сразу два таких противоамилоидных препарата проходили клинические испытания.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Одно из этих лекарств разработали в Швейцарии. Вначале ученые отбирали образцы крови у пожилых людей, которые не демонстрировали никаких когнитивных нарушений. Затем из отобранной крови они выделяли B-лимфоциты. При этом важно было выделить такие клетки, антитела которых распознавали бы «токсичные» β-амилоидные бляшки, но не белок-предшественник. Дело в том, что предшественник β-амилоида присутствует во всем организме и играет важную роль в росте нервных клеток, поэтому затрагивать его крайне нежелательно — можно навредить здоровью. В результате было получено моноклональное антитело адуканумаб (aducanumab) [1]. Оно избирательно реагирует с вредным β-амилоидом, но не атакует полезный белок-предшественник. Предположительно, это антитело может помочь пациентам на ранней стадии болезни Альцгеймера.
К настоящему моменту уже завершена первая фаза клинических испытаний адуканумаба [2], [3]. Лечению этим антителом подвергались 165 пациентов на ранней стадии болезни Альцгеймера: часть из них получала адуканумаб, а часть (контрольная группа) — плацебо. Сравнивая между собой такие группы, можно судить об эффективности лекарства. Оказалось, что у пациентов из группы плацебо значительно снижались когнитивные способности, тогда как у пациентов, получающих антитело, они стабилизировались. Проверяли это при помощи стандартных вопросников для оценки познавательных способностей. Также методом позитронно-эмиссионной томографии (ПЭТ) ученые выяснили, что адуканумаб способствует уменьшению β-амилоидных отложений в мозге. В настоящее время проводятся новые клинические исследования для дальнейшей оценки безопасности и эффективности адуканумаба.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Второй препарат получили исследователи из США и Канады [4]. Называется он верубецестат (verubecestat), и его функция заключается в ингибировании фермента бета-секретазы (BACE1). Этот фермент — один из главных «производителей» β-амилоида в мозге. Исследования, которые проводились на грызунах и приматах, показали, что у животных, принимавших верубецестат на протяжении 6–9 месяцев, содержание β-амилоида в центральной нервной системе заметно снижалось. К сожалению, результаты оказались не столь вдохновляющими, когда очередь дошла до лечения людей. В феврале 2017 года было решено прекратить клинические испытания верубецестата, поскольку препарат не проявлял эффективности в борьбе с уже развившейся болезнью Альцгеймера — по крайней мере, в случае ранней или умеренной деменции. Независимые эксперты сошлись во мнении, что в данном случае шансов получить положительный клинический эффект практически нет. Однако исследователи не теряют надежды: есть вероятность, что верубецестат подойдет для лечения пациентов с первыми проявлениями болезни Альцгеймера. Результаты этих клинических испытаний будут известны в феврале 2019 года.
В последнее время амилоидная гипотеза развития болезни Альцгеймера постепенно теряет свои позиции. Один из главных фактов, опровергающих устойчивое мнение о вредоносности β-амилоида, обнаружили исследователи из Массачусетской клинической больницы [5], [6]. Оказалось, что β-амилоид представляет собой нормальный компонент врожденного иммунитета. Ранее ученые подтвердили это предположение в экспериментах in vitro, то есть продемонстрировали соответствующие эффекты в модельных системах вне живого организма [7]. Сейчас же они получили аналогичные результаты в опытах in vivo, то есть на живых организмах. Новые исследования на мышах и круглых червях, как и эксперименты с культивируемыми клетками человеческого мозга, показали, что β-амилоид способен защищать организм от потенциально летальных инфекций. Ученые сравнивали синтетические формы β-амилоида с кателицидином — антимикробным пептидом, который помогает справляться с инвазивными бактериальными инфекциями. Оказалось, что β-амилоид ингибирует рост нескольких опасных патогенов так же, а иногда даже и лучше, чем кателицидин.
β-Амилоид, выделенный из мозга пациентов с болезнью Альцгеймера, подавлял рост культивируемых дрожжей Candida, а его синтетический аналог оказался эффективен против вирусов гриппа и герпеса. Также ученые выяснили, что трансгенные мыши, у которых экспрессировался ген человеческого β-амилоида, жили после заражения сальмонеллой значительно дольше их обычных сородичей. А быстрее всех погибали мыши, лишенные какого бы то ни было амилоидного предшественника. Трансгенная экспрессия β-амилоида защищала круглых червей и культуры нейронов от заражения микроорганизмами Candida и Salmonella. И, как вишенка на торте, последний факт: человеческий β-амилоид, синтезируемый живыми клетками, оказался в 1000 раз эффективнее в борьбе с инфекциями по сравнению с его синтетическими аналогами.
Почему так происходит? Вероятно, антимикробный эффект β-амилоида объясняется как раз его способностью образовывать агрегаты: его молекулы связываются с поверхностью микробов, а затем объединяются в плотные структуры, что предотвращает прикрепление патогенных микроорганизмов к клеткам макроорганизма. Тогда почему же амилоидные бляшки накапливаются именно в мозге? Ученые не исключают следующий вариант: возможно, мозг по каким-то причинам начинает воспринимать себя «атакованным» вторгающимися патогенами (и, возможно, в действительности так оно и есть), в результате чего запускается усиленная выработка амилоида. Но для подтверждения этой гипотезы требуются дальнейшие исследования.
Так каков же итог? Как лечить болезнь Альцгеймера? Пока очевидного ответа на этот вопрос, увы, нет. Однако, учитывая новые данные, следует понимать: тотальное уничтожение β-амилоида может быть чревато негативными последствиями для здоровья. Амилоидная гипотеза выглядит уже не так многообещающе, и ученым предстоит искать новые мишени для лечения этого тяжелого недуга. Хочется верить, что эра новых лекарств против болезни Альцгеймера уже не за горами.
Клинические рекомендации по диагностике и лечению системного амилоидоза
В клинических рекомендациях, подготовленных специалистами различного профиля, рассматриваются методы диагностики и лечениясистемного амилоидоза, в том числе АА (вто-ричный амилоидоз при хронических воспалительных заболеваниях, включая ревматоидныйартрит, анкилозирующий спондилит, аутовоспалительные заболевания, хроническиенагноения, злокачественные опухоли и др.), AL (амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема) иATTR (транстиретиновый; семейные формыполиневропатического, кардиопатического идругого амилоидоза, системный старческийамилоидоз). Диагноз амилоидоза, которыйможно заподозрить на основании клиническихданных, необходимо подтвердить при гистологическом исследовании (окрашивание препаратов ткани конго-красным с последующей микроскопией в поляризованном свете). Чтобы замедлить или приостановить прогрессирование амилоидоза любого типа, необходимо добиться уменьшения количества (или, если возможно, удаления) белков-предшественников путем лечения хронического воспаленияпри АА-амилоидозе или подавления пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуно-глобулинов при AL-амилоидозе. Для замедления прогресирования ATTR-амилоидоза упациентов с полиневропатией применяют тафамидис, который ингибирует диссоциацию мутантного транстиретина и снижает его амилоидогенность.
Определение, классификация, группы риска и принципы диагностики
Амилоидоз – группа заболеваний, отличительным признаком которых является отложение в тканях и органах фибриллярного гликопротеида амилоида. Специфическое свойство амилоида, отличающее его от других фибриллярных белков стромы, – способность к двойному лучепреломлению, что проявляется свечением в поляризованном свете предварительно окрашенных конгокрасным препаратов амилоида с изменением красного цвета конгофильных амилоидных отложений на яблочно-зеленый (дихроизм).
В основе амилоидогенеза лежит синтез большого количества нестабильных белковпредшественников, которые агрегируются с образованием амилоидной фибриллы. Клю чевое значение имеет амилоидогенность основного белка-предшественника амилоида, специфичного для каждой формы амилоидоза (в настоящее время известно более 30 таких белков), обозначение которого положено в основу современной классификации заболевания (ВОЗ, 2016 г.). Названия типов амилоида включают в себя букву А, означающую “амилоид», и обозначение конкретного фибриллярного белка амилоида – А (амилоидный А-протеин), L (легкие цепи иммуноглобулинов), TTR (транстиретин), β2М (β2-микроглобулин), В (В-протеин), IAPP (островковый амилоидный полипептид). Используют также производные наименования – иммуноглобулиновый амилоидоз (AL), транстиретиновый (ATTR) и др. (табл. 1) 1. Следует отметить, что Международная классификация болезней (МКБ) 10-го пересмотра базируется на клиническом принципе, не учитывает особенности патогенеза различных форм амилоидоза и не позволяет обосновать адекватное лечение.
| Белок амилоида | Белок-Белок-предшественник | Клиническая форма амилоидоза |
|---|---|---|
| АА | SSA-белок | Вторичный амилоидоз при хронических воспалительных заболеваниях, в том числе периодической болезни и синдроме Макла-Уэллса |
| AL | λ, κ-легкие цепи иммуноглобулинов | Амилоидоз при плазмоклеточных дискразиях – идиопатический, при миеломной болезни и макроглобулинемии Вальденстрема |
| ATTR | Транстиретин | Семейные формы полиневропатического, кардиопатического и др. амилоидоза, системный старческий амилоидоз |
| Аβ2М | β2-микроглобулин | Диализный амилоидоз |
| AGel | Гелсолин | Финская семейная амилоидная полиневропатия |
| AApoAI | Аполипопротеин А-I | Амилоидная полиневропатия (III тип по van Allen, 1956 г.) |
| AFib | Фибриноген | Амилоидная нефропатия |
| Aβ2 | β-белок | Болезнь Альцгеймера, синдром Дауна, наследственные кровоизлияния в мозг с амилоидозом |
| APrPScr | Прионовый белок | Болезнь Крейтцфельда-Якоба, болезнь Герстманна-Штраусслера-Шейнкера |
| AANF | Предсердный натрийуретический фактор | Изолированный амилоидоз предсердий |
| AIAPP | Амилин | Изолированный амилоидоз в островках Лангерганса при сахарном диабете 2 типа, инсулиноме |
| ACal | Прокальцитонин | При медуллярном раке щитовидной железы |
| ACys | Цистатин С | Наследственные кровоизлияния в мозг с амилоидозом (Исландия) |
АА-амилоидоз чаще всего развивается при ревматоидном артрите, серонегативных спондилоартропатиях, аутовоспалительных наследственных периодических лихорадках, в том числе периодической болезни (семейной средиземноморской лихорадке), а также при хронических нагноениях, туберкулезе. АА-амилоид образуется из сывороточного предшественника SAA (serum amyloid A) – острофазового белка, продуцируемого в значительных количествах в ответ на воспаление. По этой причине АА-амилоидоз называют также реактивным или вторичным.
Клинические формы AL-амилоидоза обусловлены единым этиологическим фактором – В-лимфоцитарной дискразией, характеризующейся формированием аномального клона плазматических или В-клеток в костном мозге, которые продуцируют аномальные иммуноглобулины, обладающие амилоидогенностью (легкие цепи моноклонального иммуноглобулина, чаще λ, реже κ-типа). При первичном AL-амилоидозе плазмоклеточная дискразия относительно более доброкачественная, в то время как при В-гемобластозах (множественной миеломе, болезни Вальденстрема и др.) она обладает признаками злокачественной опухоли. Аномальный амилоидогенный клон плазматических клеток может формироваться также из плазмоцитов, локализующихся вне костного мозга, что может привести к развитию локального амилоидоза. Наиболее распространенные локальные формы AL-амилоидоза – амилоидоз трахеи, бронхов и гортани, мочевого пузыря. Выявление плазмоклеточной дискразии необходимо для диагностики AL-амилоидоза, а также для оценки его риска и дифференциального диагноза.
ATTR-амилоидоз является необратимо прогрессирующим заболеванием с высокой степенью инвалидизации вследствие тяжелого поражения сердца, периферической и/или автономной полиневропатии. Пациенты обычно умирают в течение 10-12 лет от первых проявлений. Развитие ATTR-амилоидоза обусловлено мутациями в молекуле транстиретина или возрастным нарушением секреции тетрамеров транстиретина печенью. В обоих случаях происходит распад тетрамеров транстиретина до мономеров, обладающих выраженной конформационной нестабильностью.
Рекомендации:
Клинические проявления
Для вторичного АА-амилоидоза характерно более раннее начало, чем для AL-амилоидоза (средний возраст больных составляет около 40 и 65 лет, соответственно). ATTR-амилоидоз, несмотря на наследственную природу, характеризуется низкой пенетрантностью и также проявляется обычно после 35 лет.
Поражение почек – ведущий клинический признак АА- и AL-амилоидоза, наблюдающийся практически у всех больных. Поражение почек встречается и у больных с многими формами семейного амилоидоза (AFib, ALys, AGel и др.). При ATTR-амилоидозе нефропатия отмечается лишь у 20-23% больных. Клинически амилоидная нефропатия характеризуется неуклонно прогрессирующим течением с последовательной сменой стадий: протеинурия, нефротический синдром, хроническая почечная недостаточность (ХПН). Иногда возможно развитие ХПН без предшествующего нефротического синдрома.
Поражение сердца развивается у подавляющего большинства больных AL-амилоидозом и у 50-60% пациентов с АTTR-амилоидозом, но не характерно для АА-амилоидоза (рис. 1). При эхокардиографии у больных амилоидозом сердца наблюдается утолщение межжелудочковой перегородки и стенки левого желудочка (чаще симметричное), которое не сопровождается электрокардиографическими признаками гипертрофии миокарда. У части больных отмечается снижение вольтажа зубцов на ЭКГ, хотя отсутствие этого признака не исключает диагноз амилоидоза сердца. Нарушение диастолической функции левого желудочка (рестриктивный тип) приводит к развитию сердечной недостаточности, которая быстро прогрессирует, плохо поддается лечению и почти у 50% пациентов оказывается причиной смерти. Кроме того, у больных амилоидозом сердца часто наблюдаются различные аритмии и нарушения проводимости.
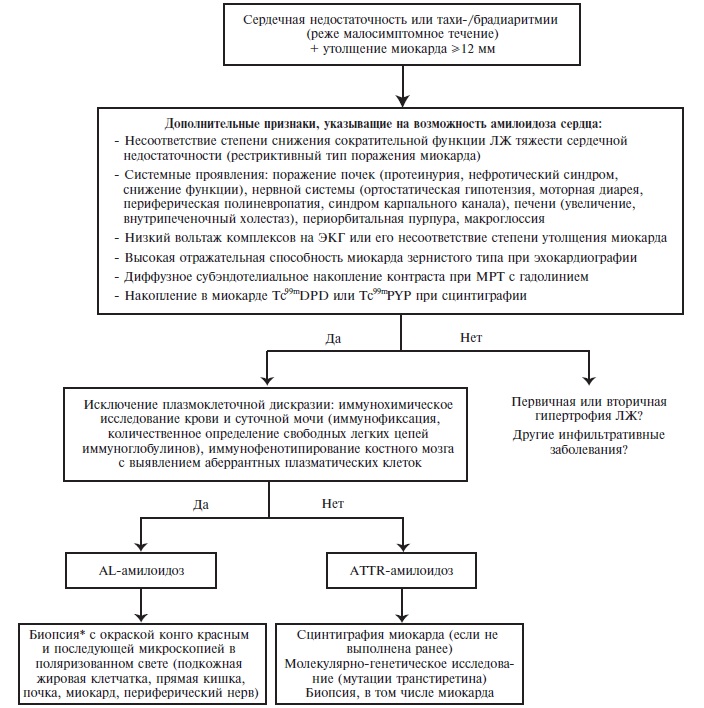
При AL-амилоидозе и особенно ATTR-амилоидозе часто встречается ортостатическая артериальная гипотензия – вариант сосудистой недостаточности, при которой сосуды теряют способность поддерживать нормальное артериальное давление в условиях ортостатических нагрузок. Она проявляется ощущением дурноты и потемнением в глазах в ортостазе в сочетании с резким снижением АД. Обычно этот симптом связан с дисфункцией автономной нервной системы (амилоидоз нервных сплетений сосудов). Тяжелая ортостатическая гипотензия сопровождается обмороками, а иногда приводит к развитию острого нарушения мозгового кровообращения.
Поражение желудочно-кишечного тракта может проявляться, особенно при AL-амилоидозе, тяжелой диареей или динамической непроходимостью, которые чаще связаны с нарушениями моторики кишечника вследствие дисфункции автономных нервных сплетений. Иногда выявляют изъязвления или перфорацию стенок с возможным кровотечением. При поражении пищевода возможна дисфагия.
Поражение печени при АА- и AL-типах амилоидоза наблюдают практически в 100% случаев. Функция печени чаще остается сохранной, редким признаком амилоидоза печени является внутрипеченочная портальная гипертензия. При некоторых вариантах семейного ALys-амилоидоза описаны тяжелые спонтанные внутрипеченочные кровотечения.
Увеличение селезенки, обусловленное амилоидным поражением, отмечается у большинства больных и обычно сопутствует увеличению печени.
Поражение нервной системы, представленное симптомами периферической соматической и автономной невропатии, отмечают у 17-35% больных AL-амилоидозом и практически у всех пациентов с наследственной амилоидной полиневропатией разных типов (ATTR, AApoA1 и др.). В большинстве случаев развивается дистальная симметричная полиневропатия с неуклонно прогрессирующим течением, различные дисфункции автономной нервной системы. Реже выявляют двусторонний синдром запястного канала, обусловленный сдавлением срединного нерва депозитами амилоида.
Поражение кожи наблюдают почти у 40% больных AL-амилоидозом. Помимо параорбитальных геморрагий описаны также папулы, бляшки, узелки, пузырьковые высыпания, склеродермоподобная индурация кожи.
Амилоидные отложения в мышцах чаще встречаются при AL-амилоидозе. Макроглоссия – патогномоничный симптом AL-амилоидоза, развивающийся примерно у 20% пациентов.
Редким проявлением амилоидоза, описанным при AL- и, в особенности, АTTR-типах, бывает поражение глаз (сухой кератоконъюнктивит, вторичная глаукома, помутнение стекловидного тела, дисфункции зрачка).
Клиническая картина других типов амилоидоза варьируется в зависимости от основной локализации и распространенности амилоидных депозитов, которые иногда могут быть значительными и напоминать проявления AL-амилоидоза.
Рекомендации:
Лечение системного амилоидоза
Целью терапии любого типа амилоидоза служит уменьшение количества (или, если возможно, удаление) белков-предшественников для того, чтобы замедлить или приостановить прогрессирование болезни. Неблаго приятный прогноз при естественном течении амилоидоза оправдывает применение агрессивных методов лечения. Клиническое улучшение, достигаемое с помощью лечения, включает стабилизацию или восстановление функции жизненно важных органов, а также предотвращение функциональных нарушений с увеличением продолжительности жизни больных. Лечение амилоидоза должно включать симптоматические методы, направленные на уменьшение выраженности сердечной недостаточности, аритмии, отечного синдрома, коррекцию артериальной гипотензии и др.
Лечение АА-амилоидоза
Цель терапии АА-амилоидоза – подавление продукции белка-предшественника SAA (вплоть до устойчивой нормализации), что достигается активным лечением хронического воспаления (в том числе субклинического). Это позволяет уменьшить клинические проявления и предотвратить прогрессирование амилоидной нефропатии и существенно улучшить прогноз.
Рекомендации:
Лечение АL-амилоидоза
При AL-амилоидозе, как и при множественной миеломе, целью лечения служит подавление пролиферации клона плазматических клеток для уменьшения продукции легких цепей иммуноглобулинов. В отличие от множественной миеломы, принципиальной задачей лечения AL-амилоидоза является по возможности полная элиминация патологического клона. В связи с быстрым прогрессированием заболевания важное значение имеет применение быстродействующих схем лечения на основе бортезомиба. По мере достижения ремиссии у некоторых больных применяют высокодозную химиотерапию с поддержкой аутологичными стволовыми клетками. При строгом подборе больных с исключением противопоказаний к этой терапии эффект достигают у 60% больных. У больных с клиническими симптомами амилоидоза сердца, ортостатической гипотензией, диареей, желудочно-кишечными кровотечениями в анамнезе, а также у лиц старше 70 лет с амилоидным поражением двух и более систем организма проведение высокодозной химиотерапии не рекомендуется. Тяжелый агранулоцитоз и другие осложнения существенно ограничивают ее применение. Проводят также лечение талидомидом или леналидомидом. Колхицин при AL-амилоидозе не эффективен.
Рекомендации:
Лечение ATTR-амилоидоза
До недавнего времени единственным методом лечения ATTR-амилоидоза была трансплантация печени, секретирующей нормальный транстиретин. Поскольку 98% всего сывороточного транстиретина синтезируется печенью, это позволяло прервать продукцию мутантного транстиретина. Трансплантация печени существенно замедляет прогрессирование ATTR-амилоидоза, а 20летняя выживаемость больных после трансплантации составляла 55,3% [36]. Однако уже имеющиеся массы амилоида способны выступать в роли ядра нуклеации для новых депозитов амилоида на основе нормального транстиретина (амилоидускоряющая субстанция). В настоящее время у больных с ранними стадиями ATTRамилоидной полиневропатии апробированы консервативные методы стабилизации тетрамерной структуры мутантного транстиретина и, следовательно, подавления его амилоидогенности. Один из таких препаратов – тафамидис замедлял на 52% (р=0,027) прогрессиро вание неврологических нарушений у больных ATTRамилоидозом, сохраняя функцию периферических соматических и автономных нервных волокон [12]. В клиническом исследовании III фазы лечение тафамидисом по сравнению с плацебо у больных с ATTR-амилоидозом сердца вызывало снижение общей смертности и частоты госпитализаций по сердечно-сосудистым причинам и задерживало ухудшение функциональной активности [81]. В Российской Федерации применение тафамидиса зарегистрировано только для лечения ATTR-амилоидоза с периферической полиневропатией.
В качестве стабилизатора транстиретина изучается также дифлюнизал из группы нестероидных противовоспалительных препаратов, однако его эффективность показана только в экспериментальных условиях.