Авто на проточных аккумуляторах
Автомобили на «жидком» электричестве
Пролог
Эх, нам электричество сделать все сумеет,
Нам электричество мрак и тьму развеет,
Нам электричество все сделает дела:
Нажал на кнопку – чик-чирик, поехала, пошла.
В 2015 году компания nanoFlowcell AG представила два необычных концептуальных электрокара — спорт-седан Quant F и небольшой хэтчбек Quantino. Главной особенностью тех автомобилей стала система жидких проточных батарей, электроэнергия в которых вырабатывается за счет прохождения двух отдельно запасаемых жидких составов через специальную ячейку. Прошёл год, и на Женевском автосалоне 2016 мы вновь видим Quant F и Quantino, в серийном варианте.
Quant F — спорткар, Quantino — городской хэтчбек. Quant F оснащается силовой установкой мощностью 1090 л.с., крутящий момент 2900 Н•м, способен разогнаться с места до «сотни» за 2,8 секунды и развить 380 км/ч максимальной скорости. И главное: пробег Quant e на одной зарядке (или заправке!) достигает 600 км.
Quantino естественно скромнее и обладает мощностью в 109 л.с., разгоняется до 100 км/ч менее чем за 5 секунд и развивает 200 км/ч «максималки». Но, что более интересно, имеет запас хода в 1000+км.
Компания производитель уже получила официальный допуск на дороги общего пользования в Европе. Производитель провёл испытания хэтчбека на выносливость, в рамках которых главный технолог nanoFlowcell Нунцио ла Веккиа управлял Quantino в течение 14 часов без остановки. В конце тестов в электролитных баках этого малыша оставалось 78% «топлива», что означает, что заявленный запас хода в 1000 км более чем реален.
Автомобиль на дорогах Цюриха:
Технический аспект
Технология потоковых батарей уходит корнями в космическую отрасль: впервые подобный источник энергии был запатентован NASA в 1976 году и предназначался для обеспечения энергией космических аппаратов. Он сочетает в себе конструктивные принципы и преимущества традиционных аккумуляторов, топливных ячеек и даже двигателей внутреннего сгорания.
Потоковые батареи можно как перезаряжать, так и мгновенно заправлять новым электролитом, словно бензином. Они не имеют эффекта памяти и не уменьшают емкости с годами. В теории у них нет технологического предела по емкости (зависит от объема «топливных» баков) и мощности (зависит от размеров реактора). Проблема лишь в том, что до недавнего времени они были крайне неэффективны с точки зрения сочетания всех этих параметров, то есть давали небольшое напряжение и мощность при слишком больших размерах. Специалисты nanoFlowcell утверждают, что им удалось упаковать в литр электроактивной жидкости небывалое количество энергии с помощью нанотехнологий. Состав «топлива», технология его производства и конструкция энергетической ячейки, разумеется, держатся в строжайшем секрете.
Чтобы разобраться, как работают современные потоковые батареи, стоит освежить в памяти принцип действия более простых источников энергии. Напомним, что в самом простом гальваническом элементе, например пальчиковой батарейке, анод (отрицательный электрод) и катод (положительный электрод) разделены электролитом — раствором, проводящим электрический ток за счет подвижности содержащихся в нем ионов. На поверхности анода протекает реакция окисления, в ходе которой высвобождаются положительные ионы и свободные электроны. На поверхности катода идет реакция восстановления, протекающая с поглощением свободных электронов и положительных ионов. При этом положительные ионы движутся от анода к катоду через электролит, а отрицательные — через нагрузку: электромотор, лампу или иную электрическую схему.
В самых простых угольных батарейках цинковый стакан, который служит анодом, постепенно растворяется, отдавая ионы и электроны. В перезаряжаемых аккумуляторах процессы окисления и восстановления обратимы. К примеру, в литий-ионных элементах положительно заряженные ионы лития переходят от катода к аноду при зарядке и от анода к катоду при разрядке. Независимо от характеристик, большинство привычных нам батареек и аккумуляторов роднит замкнутая конструкция. В их закрытом корпусе содержатся и электроды, и электролит, и запас электроактивных элементов (поставщиков расходных материалов для реакций), в роли которых, как правило, выступают сами электроды. Это значит, что и мощность, и емкость батареи ограничены размерами ее корпуса.
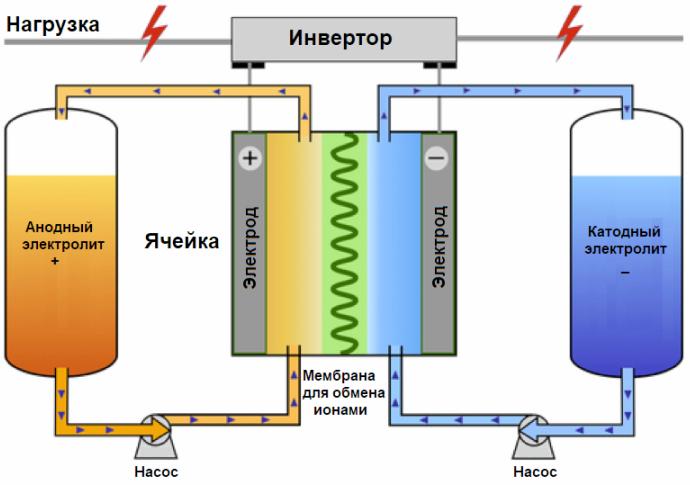
Этого недостатка лишены потоковые батареи, в которых электролит содержит растворенные электроактивные вещества, хранится в отдельных баках и прокачивается насосами через топливную ячейку. В классической потоковой батарее redox (сокращение от reduction-oxidation, восстановление-окисление) имеется два бака: в одном хранится жидкость для окислительной реакции, в другом — для восстановительной.
Топливная ячейка состоит из двух электродов, разделенных мембраной. Мембрана препятствует смешиванию жидкостей между собой, но не препятствует ионному обмену между электродами. Продукты окислительно-восстановительных реакций удаляются из ячейки вместе с протекающей жидкостью, которая по замкнутому контуру возвращается обратно в бак.
Зарядка и разрядка в потоковой батарее происходят так же, как и в любой другой: во время работы концентрация электроактивных веществ в баках падает, а во время зарядки — растет. Емкость потокового аккумулятора зависит от размеров топливных баков, поэтому потенциал данной конструкции трудно переоценить. Мало того, при необходимости быстро пополнить заряд жидкость можно просто заменить. Это так же просто и удобно, как заправить бензиновый автомобиль.
Однако мощность потоковой батареи по-прежнему определяется размерами электродов в топливной ячейке и интенсивностью происходящих на ней реакций. Именно поэтому до недавнего времени перспективы таких источников питания в промышленности, особенно в автомобильной, были не радужными.
Нанореволюция
Что стоит за витиеватыми высказываниями Нунцио ла Веккии о нанотехнологиях и квантовой химии?
(Нунцио ла Веккия, технический директор лихтенштейнской компании nanoFlowcell, — мастер делать столь громкие заявления: «Наша методика целенаправленных исследований позволила нам прорваться сквозь барьеры, установленные квантовой химией». Или чуть точнее: «Физические и химические границы, установленные уравнением Нернста (лауреат Нобелевской премии по химии, связавший термодинамику с электрохимией), были отодвинуты нами настолько далеко, что мы не могли поверить глазам»).
Очевидный путь к повышению мощности топливной ячейки — увеличение площади поверхности электрода: ведь именно на ней протекает химическая реакция и вырабатываются заветные электроны. Самый простой путь — экспериментировать с геометрической формой электродов: сворачивать их в спираль, гофрировать, придавать им самые причудливые формы, чтобы увеличить площадь поверхности, не выходя за приемлемые габариты ячейки. И конечно же, любой производитель батарей уже выжал весь потенциал геометрии досуха.
В своей цюрихской лаборатории специалисты nanoFlowcell экспериментировали не с конструкцией ячейки и не с химическим составом электродов. Объектом их изысканий была так называемая жидкость. Помимо электроактивных веществ она содержит кристаллические наночастицы, способные формировать в непосредственной близости от электродов пространственные структуры. В результате заряд формируется не только на поверхности электродов, но и в пространстве вокруг них, в самой жидкости. Пространство, в котором происходит реакция, оказывается многократно больше обычного.
При сопоставимой массе аккумуляторная установка nanoFlowcell имеет емкость в пять раз больше, чем емкость литий-ионных батарей. Один литр «ионной жидкости» вмещает в 400 раз больше энергии, чем обычный свинцовый автомобильный аккумулятор. Приятные бонусы — практически полное отсутствие склонности к саморазряду и гарантированный ресурс в 10000 зарядных циклов.
Однако в обычную машину такую батарею не поставишь. Автомобили Quant E, Quant F и Quantino пришлось проектировать буквально вокруг аккумуляторной установки. Судите сами: объем топливных баков Quant E — 200 л каждый. 400 л ионной жидкости нужно разместить без ущерба для комфорта и управляемости.
Потоковая батарея неустанно вырабатывает электроэнергию, которая запасается в емких суперконденсаторах. Эти устройства способны отдавать энергию очень быстро большими порциями, именно они обеспечивают столь внушительную пиковую мощность и динамические характеристики автомобиля. В них же запасается энергия торможения машины.
Когда заряд батареи подходит к концу, владелец авто направляется вовсе не к ближайшей розетке, а на заправку. Компания разработала специальный заправочный терминал высокого давления с двойными шлангами и пистолетами, который позволяет быстро заполнить баки новым комплектом ионных жидкостей.
Эпилог
Информации о ценах и сроках поставки машин потребителям пока не нашел, однако, думаю, nanoFlowcell AG выведет на рынок электрокар, который действительно может произвести революцию в автомобильном мире. Причем произойти это может совсем скоро.
Как Вы думаете, какова будет цена готовой серийной машины?
Авто на проточных аккумуляторах
Запас хода и время на зарядку являются двумя базовыми аргументами противников электромобилей, не понимающих их принципиального отличия от тостера. Споры между поклонниками водородных баков и адептами розетки сводятся к тому, что первые готовы продолжить движение через несколько минут зарядки, и они смеются над теми, кому надо ждать несколько часов для пополнения батареи, а то, что большинство электромобилей полностью заряжаются за то время, пока их владельцы спят, в расчет не берется.
Исследователи из Университета Пердью (США) готовы положить конец этому спору, предлагая владельцам электромобилей «возвратную технологию» зарядки, которая немного похожа на проточный (редокс) аккумулятор, но имеет принципиальное отличие. Вместо двух жидких электролитов с положительным и отрицательным зарядом в системе вместе с одним жидким электролитом используется один протекторный анод, подлежащий замене через каждые 4800 километров пробега.
Разработчики утверждают, что с такой системой заряд батареи осуществляется всего за 5 минут, а на замену анода потребуется не больше 15 минут. Дополнительное преимущество состоит в том, что при массовом внедрении технология не потребует принципиальной перестройки топливной инфраструктуры – базами для закачки электролита и замены протекторного катода могут стать обычные бензозаправки.
В новой системе водород производится по мере необходимости и хранить его можно при давлении в 500 раз ниже, чем в водородном баке, говорят ученые. До сих пор проточные батареи не были конкурентным энергоносителем на рынке из-за низкой удельной энергоемкости, а именно 20 ватт/кг против 130-140 ватт/кг в литий-ионных батареях. Однако батареи нового типа потенциально в 5-10 раз более энергоемкие.
Отработанные аккумуляторные жидкости могут собираться и восстанавливаться за счет энергии солнечных, ветровых или гидроэлектростанций. Их компоненты вполне безопасны для хранения в жилом доме, достаточно стабильны, чтобы соответствовать основным требованиям производства и дистрибуции, и являются экономически эффективными.
Для коммерческой реализации технологии разработчиками уже создана компания IFBattery и ведутся испытания на транспортных средствах, работающих в реальных условиях. Предполагается, что замена анода будет стоить около 65 долларов. Предприятия по хранению и перекачке нефтепродуктов могут легко перепрофилироваться на работу с электролитом и установку свежих анодов. Обычные заправки также легко могут перейти на новую технологию, поскольку у них уже есть 100-летний опыт работы с резервуарами и насосами.
Проточные аккумуляторы — аккумуляторы нового типа, представляющие собой накопители электрической энергии, отличающиеся по конструкции от традиционных аккумуляторов. В проточном аккумуляторе жидкий электролит прокачивается через ядро при помощи насосов.
Принципиально электролит такой батареи представляет собой раствор металлических солей, способный переносить положительный и отрицательный заряды. В процессе прокачки электролита через разделенный мембраной резервуар, положительный и отрицательный электрод обеспечивают ионный обмен с электролитом и генерацию электричества в ходе окислительно-восстановительных реакций.
В качестве электролита для проточных аккумуляторов хорошо подходит раствор серной кислоты и ванадиевой соли, тогда как электроды изготавливаются из графита (ванадиевый проточный аккумулятор).
Суть в том, что ванадий, 23-й элемент периодической таблицы Менделеева, относится к тем немногим активным веществам, с которыми эрозию можно держать под контролем. Сегодня исследователи ищут менее дорогостоящие вещества, которые позволили бы сделать технологию проточных аккумуляторов широко доступной и недорогой.
Одна ячейка способна производить разность потенциалов от 1,15 до 1,55 вольт. Как и в любой другой системе батарей, для получения нужного уровня напряжения на клеммах, достаточно соединить несколько таких ячеек последовательно.
Удельная энергоемкость проточного аккумулятора на основе соли ванадия составляет около 40 Вт · ч/кг, то есть аккумулятор на 20 кВт · ч будет весить полтонны, приблизительно как свинцово-кислотный аккумулятор аналогичной емкости. Но жить проточный аккумулятор будет дольше, что делает его пригодным для хранения электрической энергии в больших количествах. Однако скорость потребления энергии должна оставаться умеренной.
Электролит проточного аккумулятора физически распределен оп двум резервуарам (анодный и катодный резервуары — для анодной и катодной частей электролита), размер которых для аккумуляторов разной емкости может варьироваться. При необходимости замены ячеек на новые, допускается повторное использование электролита, что приводит к существенной экономии материалов.
Самая же уязвимая часть проточного аккумулятора — мембрана в центре ячейки, отделяющая друг от друга соответствующие полуячейки. Проблема в том, что мембрана со временем корродирует (испытывает разрушительную коррозию), поэтому к электролиту добавляют специальные примеси, замедляющие коррозию мембраны.
Тем не менее тенденция к использованию ванадия в чистой энергетике уже намечается, ведь это позволит создавать аккумуляторы большой емкости, по характеристикам превосходящие литиевые, при том вдвое более дешевые. Стандартизированные проточные аккумуляторы на мощность 250 кВт могут собираться в батареи необходимой емкости вплоть до огромных.
Россия пока лишь отрабатывает технологию проточных аккумуляторов в условиях лаборатории — исследует режимы и характеристики, изучает реальный потенциал системы.
Конечно, концепция остается стандартной: окислительно-восстановительная батарея с парой емкостей для жидкого электролита, который пропускается одновременно через положительную и отрицательную полуячейки, разделенные мембраной. При движении в одну сторону, электролит заряжается, а при движении в противоположную сторону — отдает накопленную энергию.
Объемы резервуаров варьируют, изменяя таким образом емкость аккумулятора, а для повышения токовых характеристик — увеличивают площадь мембраны между полуячейками, что позволяет повысить предельно допустимую скорость передачи энергии через батарею.
Хотя тема проточных аккумуляторов давно набирает популярность в мире, в России ей пока не очень активно занимаются, лаборатория Сколтеха, на начало 2020 года, была единственной.
Справедливости ради отметим, что еще в 1996 году японцы уже использовали у себя в стране подобные проточные аккумуляторы общей мощностью более 100 кВт. Сегодня уже можно говорить о достижимых мощностях в десятки мегаватт.
По сей день такие системы применяются в Японии для стабилизации частоты переменного тока с номинальной мощностью в 60 мегаватт. Таким образом, уже сейчас перспективы проточных аккумуляторов вполне очевидны. Они хорошо подойдут для хранения электрической энергии в больших объемах, остается довести технологию до совершенства.
«Проточная батарея» обеспечит электромобилю запас хода в 5000 км
Американские ученые из Университета Пердью, штат Индиана, совершили огромный скачок в развитии технологии «многоразового использования» новых типов аккумуляторов – электромобиль в состоянии проехать около 3000 миль (4828 км).
Борьба с «главным недостатком» электромобилей
Количество разнообразных электромобилей в мире постоянно растет и уже достигло отметки в 5 млн транспортных средств. Наверное, одним из самых главных недостатков электротранспорта является малый запас хода, который составляет, для большинства моделей, 200-400 км, а затем необходима подзарядка, которая может продолжаться несколько часов.
Американские ученые из Университета Пердью продолжают совершенствовать новую технологию, которая увеличивает запас хода без многочасовой подзарядки до фантастической на сегодняшний день величины – около 5000 км, т.е. более чем в десять раз.
В этой технологии используется безопасная и доступная методика перезарядки автомобильных аккумуляторов – жидкий электролит просто и быстро заменяется в батарее и электромобиль может продолжить движение. А отработанная аккумуляторная жидкость собирается и в дальнейшем отправляется на электростанции для повторной зарядки. Особенно эффективно заряжать электролит от солнечных и ветровых электростанций, которые достаточно часто вырабатывают «излишки» энергии и имеют проблемы с их использованием и хранением.
Как мы видим, новая технология не обеспечивает «чудеса из воздуха» – электромобили могут стать еще «более похожими» на привычные бензиновые модели и регулярно заезжать на заправочные станции для замены электролита. Успешное применение «проточных батарей» на основе этой технологии было продемонстрировано в 2017 году – в тестовых испытаниях принимали участие электрические гольф-кары и промышленные вилочные погрузчики. «Безопасная проточная батарея делает две вещи – она вырабатывает энергию и водород», – утверждают разработчики.
«Это переломный момент для следующего поколения электромобилей, потому что технология не требует очень дорогостоящей перестройки электросети на всей территории США. Вместо этого можно было бы переоборудовать заправочные станции для перекачки свежего электролита и утилизации истощенного электролита, а также установить оборудование для замены анодов. Это проще, безопаснее и более экологично, чем существующая система батарей для электромобилей», – утверждает профессор Джон Кушман.
Конечно, новая технология еще не полностью готова для массового коммерческого использования – впереди многочисленные тестирования на реальных электромобилях. Не полностью изучены вопросы функционирования «проточных батарей» при низких температурах. Но уже достигнут значительный прогресс – «Сейчас мы находимся в точке, где мы можем генерировать много энергии. От такой батареи может получиться больше энергии, чем можно было бы предположить», – подтверждает профессор Джон Кушман.
Проточные батареи — почему за ними будущее
Изобретение проточных батарей — нового уникального источника хранения энергии, стало настоящим прорывом в промышленной отрасли. Почему их называют аккумуляторами будущего, где они применяются и чем лучше других накопителей энергии, мы подробно расскажем в данной статье.
Проточная батарея (аккумулятор) — что это такое и как работает
Проточная батарея (или проточная редокс-батарея) – тип гальванического элемента, в котором химическая энергия обеспечивается за счет двух химических компонентов, растворенных в жидкости, содержащейся в системе и разделенной мембраной.
Ионный обмен, сопровождающийся движением электрического тока, происходит через мембраны, в то время как обе жидкости циркулируют в собственном отдельном пространстве. Напряжение элемента определяется химически через уравнение Нернста и в практических отраслях колеблются от 1 до 2,2 Вт.
Проточная батарея может использоваться как топливный элемент (где извлекается потраченное топливо и добавляется новое), или как перезаряжаемая батарея (где источник электрической энергии запускает регенерацию топлива).
Хотя она обладает такими техническими преимуществами над традиционными перезаряжаемыми батареями, как потенциально отделяемые баки для жидкости и почти безграничный срок службы, на данный момент разработки обладают сравнительно меньшей мощностью и требуют большего количества сложной электроники.
Энергетическая емкость зависит от объема электролита (количества жидкого электролита), а мощность – от площади поверхности электродов.
Принцип построения
Проточная батарея – перезаряжаемая топливная ячейка, где электролит содержит один или больше растворенных электропроводящих элементов, протекающих сквозь гальванический элемент, который напрямую преобразует химическую энергию в электричество (электропроводящие элементы – «элементы в растворе, которые могут участвовать в реакции электрода, или которые могут быть адсорбированы электродом»).
Резервный электролит располагается снаружи, как правило – в емкости, и, как правило, закачивается через элемент (или элементы) реактора, хотя известны и системы подачи самотеком. Проточные батареи могут быстро «перезаряжаться» путем замены жидкого электролита (наподобие заправки топливных баков для двигателей внутреннего сгорания), или синхронного восстановления затраченного материала для повторной подачи питания.
Другими словами, проточная батарея практически похожа на обычный гальванический элемент за исключением того, что ионный раствор (электролит) не сохраняется в элементе вокруг электродов. Чаще всего, ионный раствор хранится вне элемента и может подаваться туда для выработки электричества. Общий объем потенциально произведенной энергии зависит от размера емкостей для хранения.
Работа проточных батарей происходит по принципам, заложенным электрохимической технологией.
Типы батарей
Были разработаны различные типы проточных элементов (батарей), в том числе – редокс-батареи, гибридные и безмембранные. Фундаментальным отличием между стандартными батареями и проточными элементами является то, что энергия хранится не в материале электродов, как в стандартных батареях, а в электролите, как в проточных элементах.
Редокс-батареи
Редокс-элемент (окислительно-восстановительный элемент) – реверсивный элемент, где электрохимические компоненты растворены в электролите. Проточные редокс-батареи являются перезаряжаемыми (аккумуляторами). Так как они работают чаще по принципу переноса разнозаряженных электронов, чем диффузии в твердом теле или внедрения, они, скорее всего, могут называться топливными элементами, а не батареями. В промышленной практике топливные элементы – обычное дело, и, как правило, первичные элементы типа системы H2/O2, не требуются.
Еще одним примером реверсивного топливного элемента является составной регенеративный топливный элемент, используемый на аппарате «Helios Prototype» от НАСА. Европейская патентная организация классифицирует проточные редокс-элементы (H01M8/18C4) как подкласс регенеративных топливных элементов (H01M8/18). Примерами проточных редокс-элементов являются ванадиевая проточная батарея, полисульфидно-бромидная батарея (Regenesys) и урановая проточная батарея. Топливные редокс-элементы менее распространены в коммерческих масштабах, хотя предлагалось большое количество подобных систем.
Был продемонстрирован прототип полийодно-цинковой проточной батареи с плотностью 167 Вт*ч/л. Более старые бромидно-цинковые элементы достигают плотности в 70 Вт*ч/л. Для сравнения, литий-железо-фосфатные батареи накапливают 233 Вт*ч/л энергии.
Из-за роста дендритов цинка галоидно-цинковые батареи не могут работать при высокой плотности электрического тока (свыше 20 мА/см2), что, таким образом, ограничивает емкость энергии. Добавление спирта в электролит йодно-цинковой батареи частично помогает решить проблему.
При полной разрядке батареи обе емкости содержат одинаковый раствор электролита: смесь положительно заряженных ионов цинка (Zn2+) и отрицательно заряженных ионов йода, I-. При заряде одна из емкостей содержит еще один отрицательно заряженный ион йода – полийодид (I3-). Батарея производит энергию, закачивая жидкость из внешних емкостей в сечение канала батареи, где жидкости смешиваются. Внутри канала ионы цинка проходит через селективную мембрану и превращается в металлический цинк в отрицательной клемме сечения канала.
Чтобы увеличить энергетическую емкость йодно-цинковой проточной батареи, ионы бромида (Br-) используются в качестве комплексообразующего агента для стабилизации свободного йода, формируя ионы бромистого йода (I2Br-) для освобождения ионов йода для хранения заряда.
Стандартные химикаты проточной батареи обладают как низкой удельной энергией (которая делает их слишком тяжелыми для полноразмерных электромобилей), так и малой удельной мощностью (которая делает ее слишком дорогой для стационарного накопления энергии). Однако была продемонстрирована высокая мощность (в 1,4 В/см2) для бромо-водородных проточных батарей, а броматно-водородные проточные батареи показали удельную энергию в 530 Вт*ч/кг на уровне емкости.
Одна из систем использует органические полимеры и солевой раствор с целлюлозной мембраной. Прототип был способен выдержать 10 000 циклов зарядки при сохранении значительной доли емкости. Плотность энергии составляла 10 Вт*ч/л. Плотность тока достигала 100 мА/см2.
Гибридные батареи
Гибридная проточная батарея использует один и более электропроводящих компонентов, оседающих как твердый слой. В этом случае гальванический элемент содержит один электрод батареи и один электрод топливного элемента. Этот тип ограничен в производстве энергии из-за площади поверхности электрода. Среди гибридных батарей – цинк-бромные, цинк-цериевые и свинцово-кислые проточные батареи.
Безмембранные батареи
Безмембранные батареи основаны на принципе ламинарного потока, где две жидкости перекачиваются через канал. Они проходят через электрохимические реакции для хранения и высвобождения энергии. Растворы перетекают параллельно и немного смешивается. Поток легко разделяет жидкости, устраняя потребность в мембране.
Мембраны часто – самый дорогостоящий и ненадежный компонент батарей, так как они могут ржаветь при повторном воздействии определенных реагентов. Отсутствие мембран позволяет использовать раствор жидкого брома и водорода. Это сочетание проблематично при использовании мембран, потому что они образуют бромистоводородную кислоту, которая может разрушить мембрану. Оба материала доступно по низкой цене.
Концепт использует маленький канал между двумя электродами. Жидкий бром перетекает через канал над графитовым катодом, а бромистоводородная кислота – под пористым анодом. В то же время газообразный водород протекает через анод. Химическая реакция может быть обращена для перезарядки батареи – новация для безмебранных батарей. Одна из таких безмембранных проточных батарей была продемонстрирована в августе 2013 года. Ее максимальная емкость энергии составляет 7950 Вт/м2 — в три раза больше, чем у других безмембранных систем – а ее размеры — гораздо больше, чем у ионно-литиевых батарей.
Компания «Primus Power» разработала запатентованную технологию для своей цинк-бромной проточной батареи – типа проточной редокс-батареи, для устранения потребности в мембране или сепараторе, что уменьшает цену и количество ошибок. Безмембранная проточная редокс-батарея от этой компании работает в сооружениях США и Азии, а появление изделия второго поколения обещалось на 21 февраля 2017 года.
Органические батареи
По сравнению с традиционными водными неорганическими проточными редокс-батареями, как-то ванадиевые или бромисто-цинковые, которые были разработаны десятки лет назад, органические проточные редокс-батареи появились в 2009 году и подавали большие надежды в плане уменьшения главных недостатков, предотвращающих экономическое и экстенсивное сворачивание разработок традиционных неорганических проточных редокс-батарей. Главной заслугой органических проточных редокс-батарей являются изменяемые окислительно-восстановительные свойства редокс-активных компонентов.
В дальнейшем органические проточные редокс-батареи можно разделить на две категории: Водные Органические Проточные Редокс-Батареи (ВОПРБ) и Неводные Органические Проточные Редокс-Батареи (НВОПРБ).
ВОПРБ используют воду в качестве электролита, а НВОПРБ используют органические растворители для растворения редокс-активных материалов.
В зависимости от использования одного или двух органически редокс-активных материалов в качестве анода и/или катода, ВОПРБ и НВОПРБ можно разделить на исключительно органические системы и гибридные органические системы, использующие неорганические материалы в качестве анода или катода. Экспериментальная версия ВОПРБ произошла раньше, чем НВОПРБ.
В случае накопления энергии в промышленных масштабах, ВОПРБ обладает потенциалом куда большим, чем НВОПРБ, так как первые – дешевле, лучшие эксплуатационные характеристики и производительность, а также – преимущества водных электролитов в области безопасности над неводными.
НВОПРБ могут быть применены в ограниченных специальных отраслях за счет более высокой плотности энергии по сравнению с ВОПРБ, несмотря на большее количество проблем безопасности, стоимость органических растворителей, вызванные радикалами побочные реакции, смешение электролитов и ограниченный срок службы. Данные ниже демонстрируют, в основном, особенности ВОПРБ.
Основой некоторых ВОПРБ являются хиноны. В одном исследовании в качестве катодов использовались 1,2-дигидробензохинон-3,5-дисульфокислота и 1,4- дигидробензохинон-2-дисульфокислота, а анолитом в кислотном ВОПРБ служило соединение Pb/PbSO4.
Первые ВОПРБ были гибридными системами, так как они используют органические редокс-активные материалы только для катода. Хиноны принимают две единицы электрического заряда, в сравнении с одной в традиционном католите, что подразумевает, что такая батарея может хранить в два раза больше энергии при аналогичном объеме.
9,10-антрихинон-2,7-дисульфокислота, как и хинон, также была оценена по достоинству. Это соединение подвергается быстрому обратимому восстановлению двух электронов/двух протонов в электроде из стеклоуглерода, погруженного в серную кислоту.
Водная проточная батарея с недорогими углеродными электродами, сочетающая хиноновую/гидрохиноновую пару с окислительно-восстановительную пару Br2/Br-, вырабатывают пиковую гальваническую удельную мощность свыше 6 000 Вт/м2 при 13 000 А/м2. Циклирование показывает сохранение емкости за цикл на уровне свыше 99 %. Удельная энергия за единицу объема достигала 20 Вт*ч/л. Антрахинон-2-дисульфокислота и антразинон-2,6-дисульфокислота на отрицательном полюсе и 1,2-дигидробензохинон-3,5-дисульфокислота на положительном полюсе предотвращают образование опасного брома.
Несмотря на отсутствие опубликованной официальной информации, заявлялось о том, что батарея после тысячи циклов не показала тенденции к ухудшению свойств. Несмотря на то, что эта целиком органическая система оказалась громоздкой, она обладает небольшим напряжением элемента (около 0,55 В) и малой плотностью энергию (менее 4 Вт*ч/л.).
Бромистоводородная кислота, используемая в качестве электролита, была замещена гораздо менее токсичным щелочным раствором (1 моль/литр гидроксида калия) и ферроцианидом. Более высокий pH дает меньшую коррозию, что позволяет использовать недорогие полимерные емкости. Увеличившееся электрическое сопротивление в мембране компенсируется ростом напряжения.
Напряжение элемента составило 1,2 В. КПД элемента превышает 99 %, в то время как цикличный КПД равен 84 %. Батарея обладает ожидаемым сроком службы, как минимум, в 1 000 циклов. Теоретическая плотность энергии составила 19 Вт*ч/л. Химическая стабильность ферроцианидов в растворе гидроксида калия с высоким pH без формирования гидроксида железа (II) и гидкросида железа (III) должна быть проверена, прежде чем пойти в промышленность.
Другая органическая ВОПРБ показала работу параквата в качестве анолита, а 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксил – в качестве католита, а также – соль и дешевая мембрана обмена анионов для обеспечения заряда и разряда. Эта система класса «MV/TEMPO» обладает наибольшим напряжением элемента (1,25 В) и, возможно, наименьшими капитальными затратами (180 долларов/кВт*ч) для класса ВОПРБ.
Жидкие электролиты на водной основе были разработаны как случайная замена для нынешних систем без замены существующей инфраструктуры. Тестовая 600-мВ батарея была способна работать после 100 циклов с КПД около 100 %, плотность тока достигает 20-100 мА/см2, а оптимальная характеристика оценивается на уровне 40-50 мА, что позволяет сохранить примерно 70 % изначального напряжения батареи.
Важность исследований состоит в том, что нейтральные ВОПРБ будут гораздо безопаснее для окружающей среды, чем кислотные или щелочные аналоги, хотя они показывают электрохимические свойства, сравнимые с коррозийными кислотными или щелочными ПРБ.
ВОПРБ типа «MV/TEMPO» обладают плотностью энергии 8,4 Вт*ч/л с ограничением на полюсе «TEMPO». Следующий шаг – определение высшей емкости католита, подходящей для «MV» (растворимость в воде – примерно 3,5 М/л, 93,8 А*ч/л).
Один из концептов проточной батареи основан на редокс-активных органических полимерах, использующих паракват и TEMPO с диализными мембранами. Полимерная проточная редокс-батарея (ППРБ) использует функционализированные макромолекулы (схожие с органическим стеклом или пенопластом), растворенные в воде, выступающей в качестве активной среды и для анода, и для катода.
Таким образом, металлы и сильно коррозионные электролиты – типа солей ванадия в серной кислоте – уже не используются, и можно использовать простые диализные мембраны. Мембрана, разделяющая катод и анод в проточной ячейке, работает как фильтр и гораздо проще и дешевле в производстве, чем обычные ионоселективные мембраны. Она сохраняет крупные полимерные «спагетти-подобные» молекулы, хоть и позволяет пройти мелким противоионам.
Концепт может решить проблему дороговизны стандартной мембраны на основе полифторэтилена с боковыми сульфогруппами, но разработка и синтез редокс-активных полимеров с высокой растворимостью в воде – нестандартная задача.
Металлогидридные батареи
Протонные проточные батареи (ППБ) включает топливный элемент, состоящий из металлогидридного накопительного электрода в реверсивной мембране протонного обмена. Во время зарядки, ППБ сочетает ионы водорода, произведенные после разложения воды, с электронами и частицами метала в одном электроде топливного элемента. Энергия хранится в форме твердого металлогидрида. Разрядка производит электричество и воду, когда процесс обращается вспять, а протоны сочетаются с кислородом из окружающей среды. Могут применяться металлы, гораздо более дешевые, чем литий, и обеспечивать большую плотность энергии в сравнении с литиевыми элементами.
Батареи с сетью наночастиц
Серно-литиевая система, которая была смонтирована в сеть наночастиц, устраняет потребность в том, чтобы заряд двигался к частицам и от них, которые находятся в прямом производстве с проводящей пластиной. Вместо этого сеть наночастиц позволяет электричеству протекать сквозь жидкость. Это позволяет извлекать больше энергии.
Полутвердые батареи
В полутвердых проточных батареях, аноды и катоды состоят из частиц, подвешенных в жидкости-носителя. Суспензии для положительных и отрицательных полюсов хранятся в отдельных емкостях и перекачиваются по отдельным трубопроводам в ряд смежных реакционных камер, где они разделяются барьером типа тонкой пористой мембраны. Подход сочетает основную структуру проточных батарей на водной основе, использующих электродный материал, подвешенный в жидком электролите, с химией ионно-литиевых батарей с безуглеродными суспензиями и жидкими растворами с проводящей углеродной сетью. Безуглеродной полутвердой проточной редокс-батареей также иногда называется проточная редокс-батарея с твердой суспензией. Растворение материала сильно меняет ее химический процесс. Однако, взвешенные частицы твердого материала сохраняют характеристики твердого тела. В результате появляется вязкая суспензия, текущая как меласса.
Преимущества и недостатки
Проточные редокс-батреи и менее распространенные гибридные проточные батареи обладают преимуществами в плане гибкости компоновки (благодаря разделению активных составляющих), длительности срока службы (так как там не происходит фазовых переходов их твердого состояния в твердое), скорости времени отклика, отсутствия потребности в «уравнивании» заряда (перезарядка батареи для обеспечения равным зарядом всех элементов) и отсутствия вредных выбросов. Некоторые типы также предлагают легкое изменение заряда (через зависимость напряжения от заряда), низкую стоимость обслуживания и допуск перезарядки и переразряду. В сравнении с твердыми перезаряжаемыми батареями типа ионно-литиевых, проточные редокс-батареи, а также – их аналоги на водной основе, в частности, могут работать при больших напряжении и плотности энергии. Эти технические достоинства делают проточные редокс-батареи отличным вариантом для хранения энергии в промышленных масштабах.

Также в сравнении с нереверсивными топливными элементами или электролизерами, использующими простые электролитические соединения, проточные батареи, в основном, обладают несколько меньшим КПД.
Развитие и экономия, идущая от лабораторий к промышленным предприятиям, продолжается и сегодня. Стоимость компонентов – один из важных аспектов этого процесса. В лаборатории было продемонстрировано серно-кислородно-солевое соединение.
Отрасли применения
Проточные батареи в большинстве случаев нужны для относительно крупных (1 кВт*ч – 10 МВт*ч) стационарных сооружений. Здесь присутствуют следующие отрасли: