Что кровоснабжает височная артерия
Что кровоснабжает височная артерия
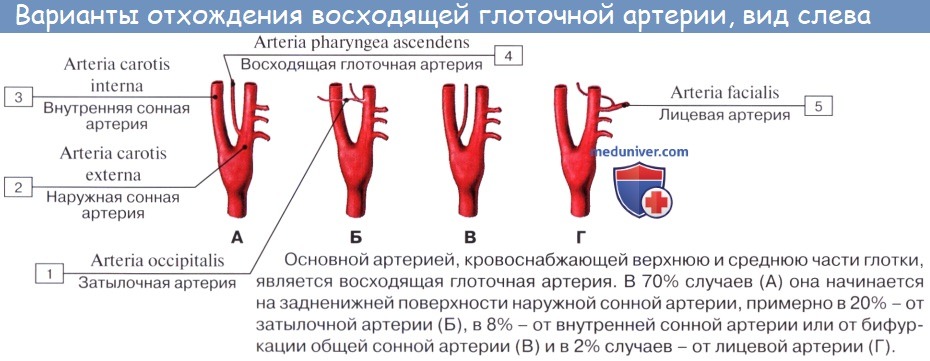
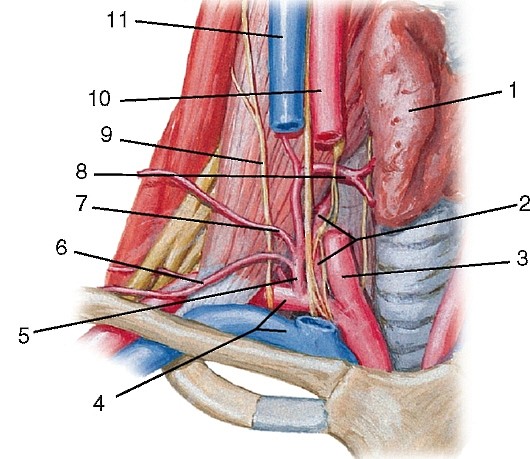
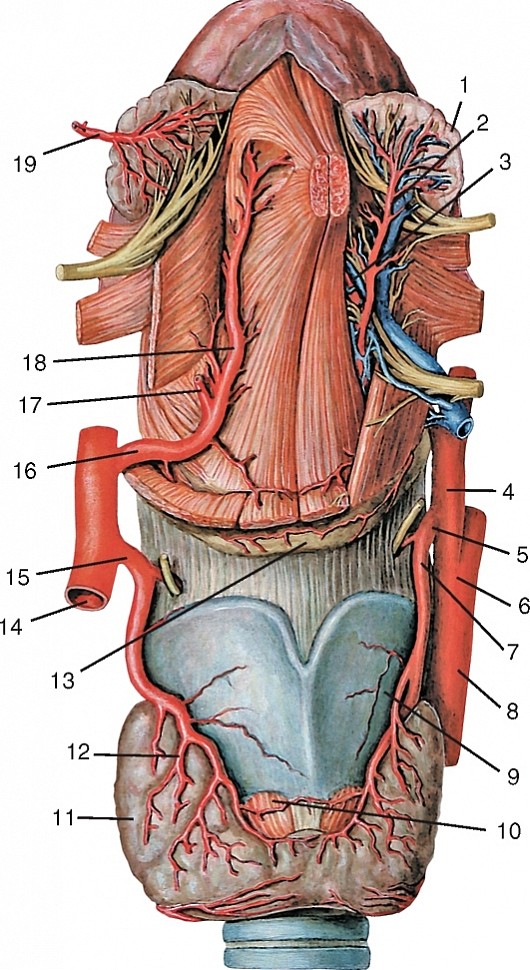
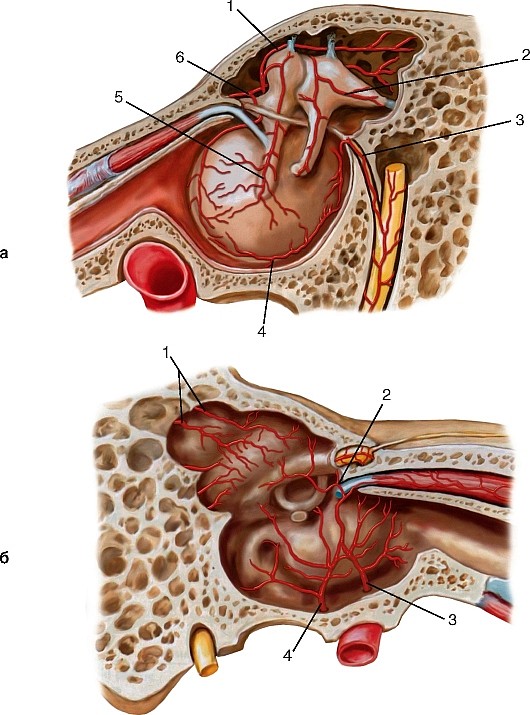
1. A. pharyngea ascendens, восходящая глоточная артерия, направляется кверху по стенке глотки, снабжая ее, мягкое нёбо, нёбную миндалину, слуховую трубу, барабанную полость и твердую оболочку головного мозга.
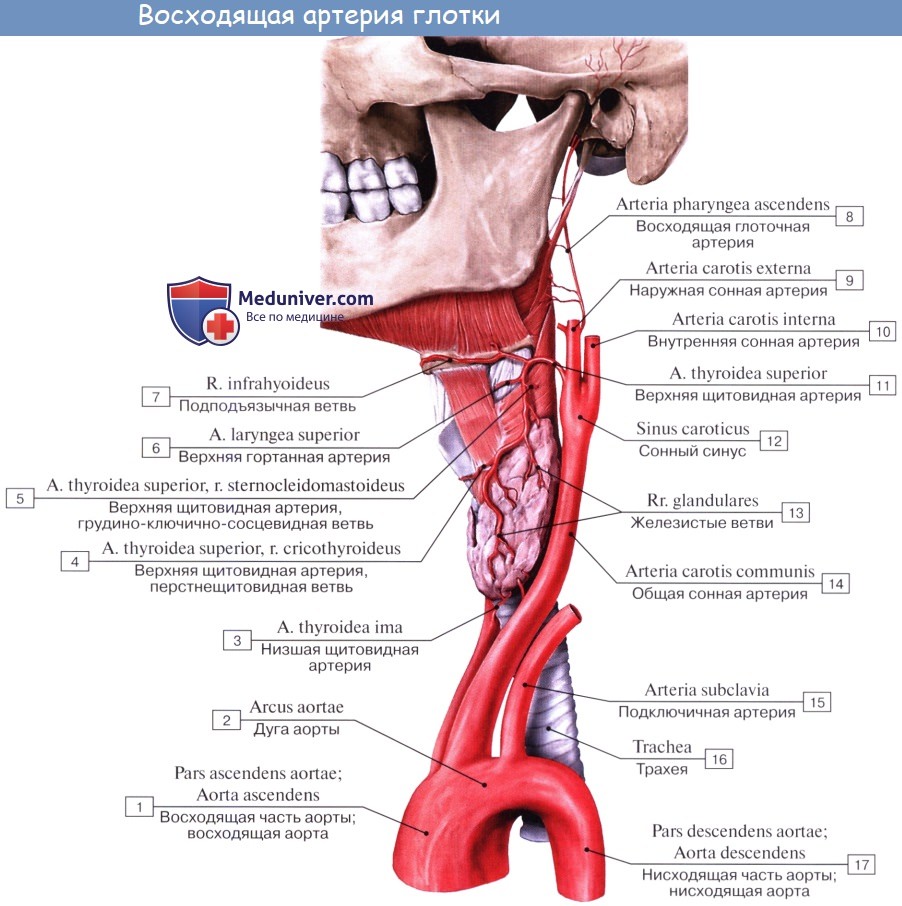
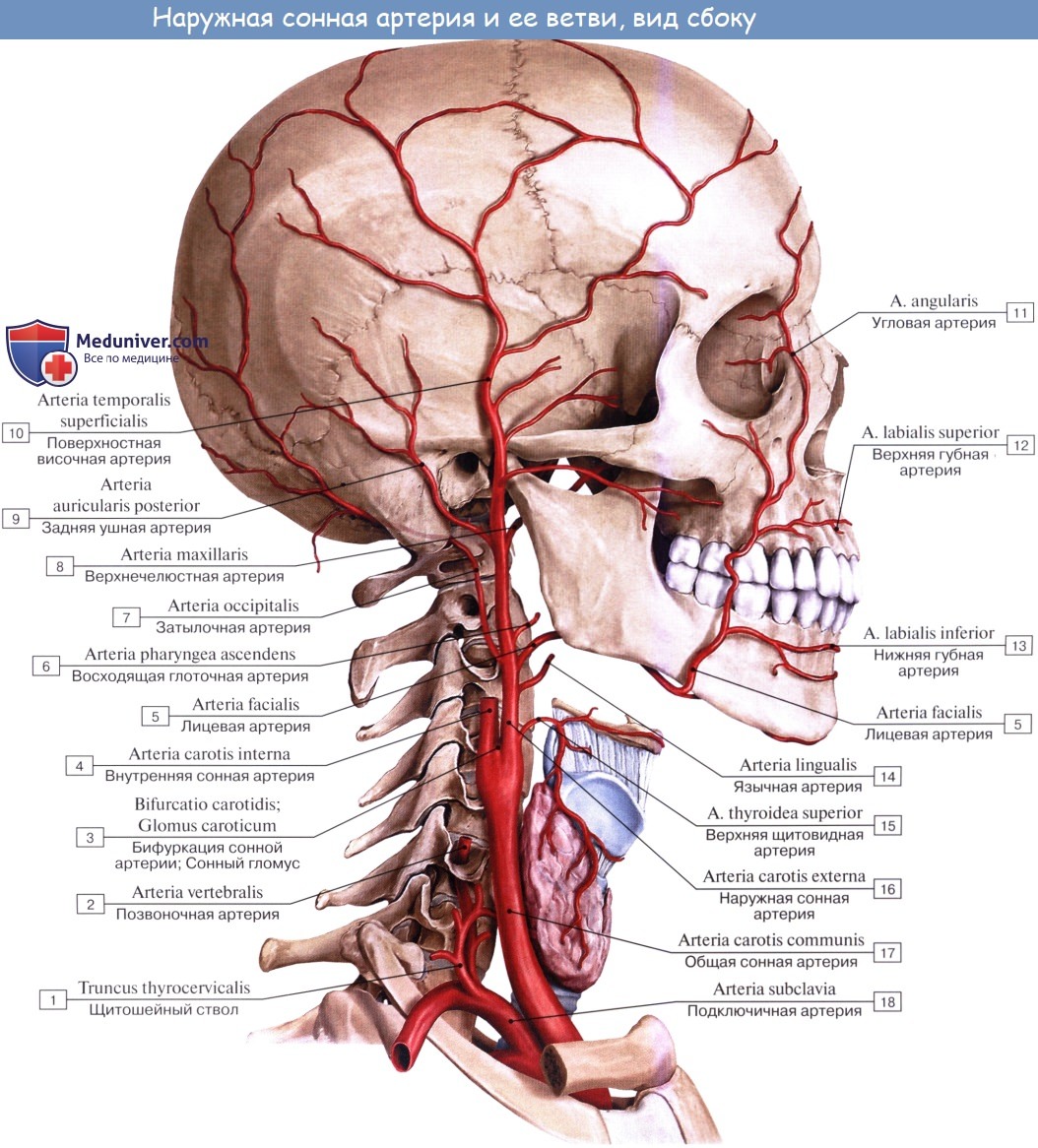
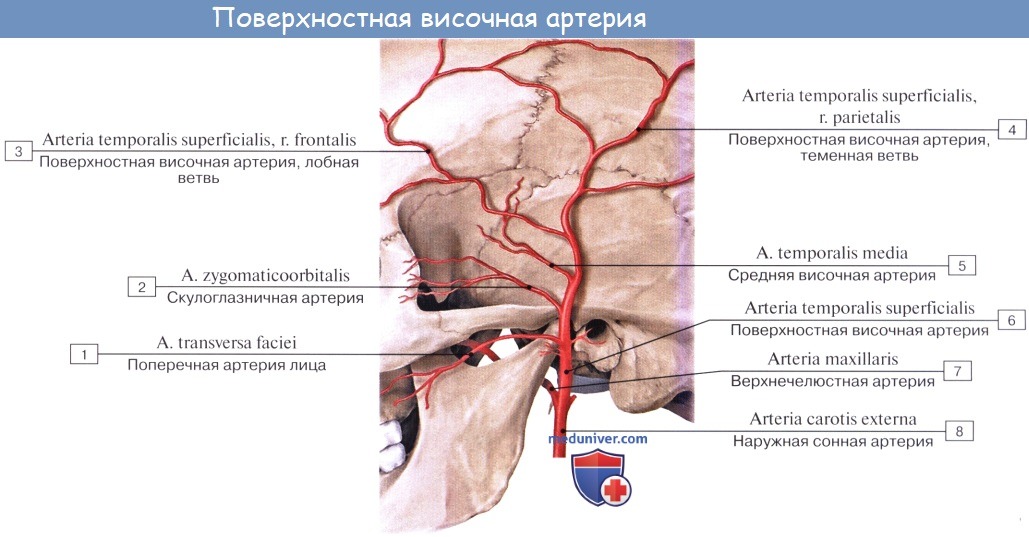
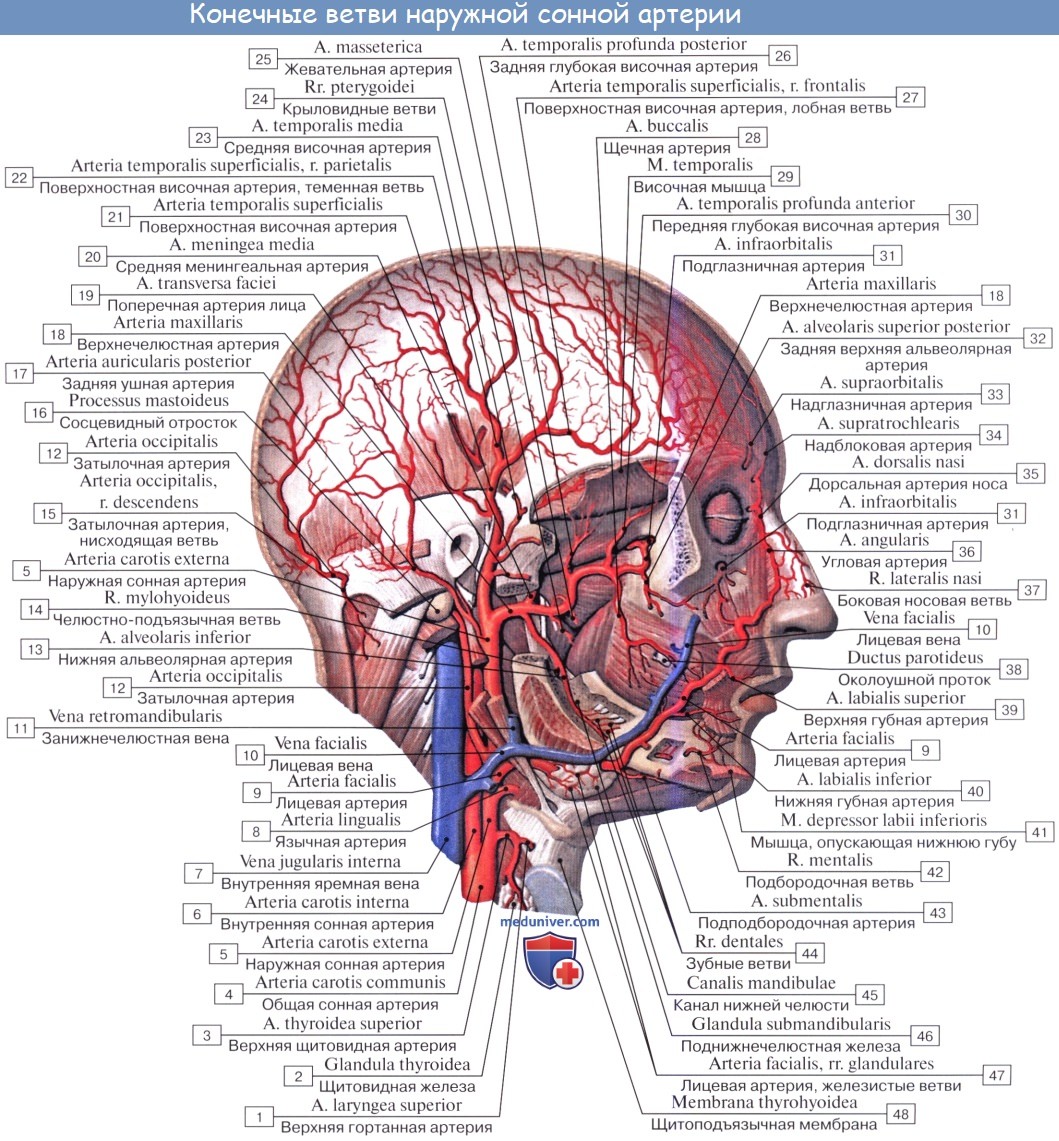
2. A. temporalis superficialis, поверхностная височная артерия, одна из двух конечных ветвей наружной сонной артерии, идет как продолжение ствола a. carotis externa впереди наружного слухового прохода на висок, располагаясь под кожей на фасции височной мышцы. Здесь артерия может быть прижата к височной кости.
Ее конечные ветви, ramus frontalis и ramus parietalis, разветвляются в области темени и виска. По пути она дает ветви к околоушной железе, к латеральной поверхности ушной раковины и к наружному слуховому проходу; часть ветвей идет к задней области лица, к наружному углу глаза, к m. orbicularis oculi и скуловой кости. A. temporalis superficialis снабжает также m. temporalis.
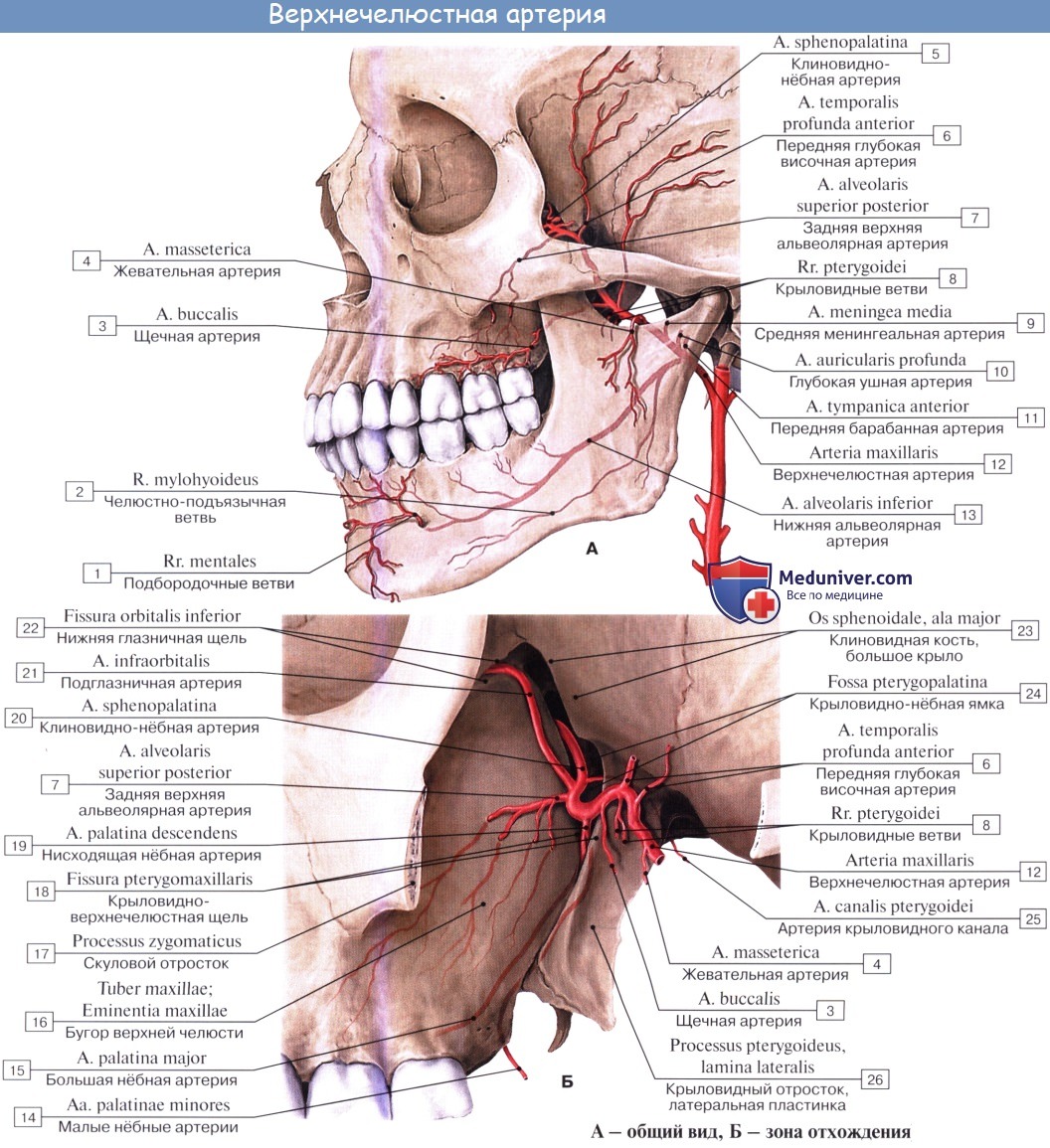
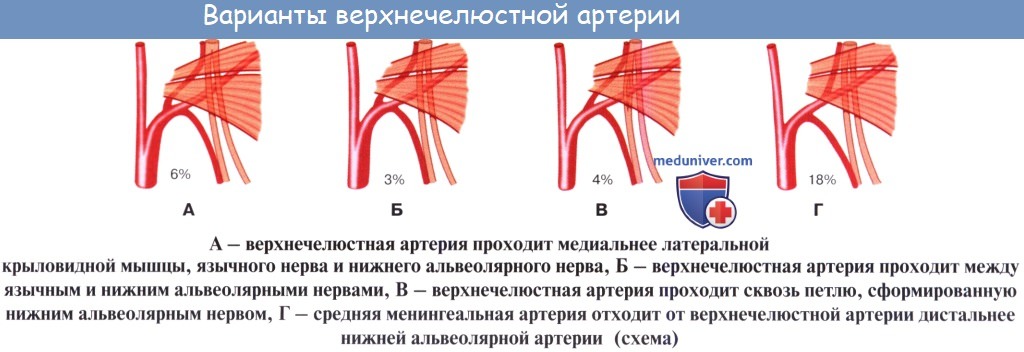
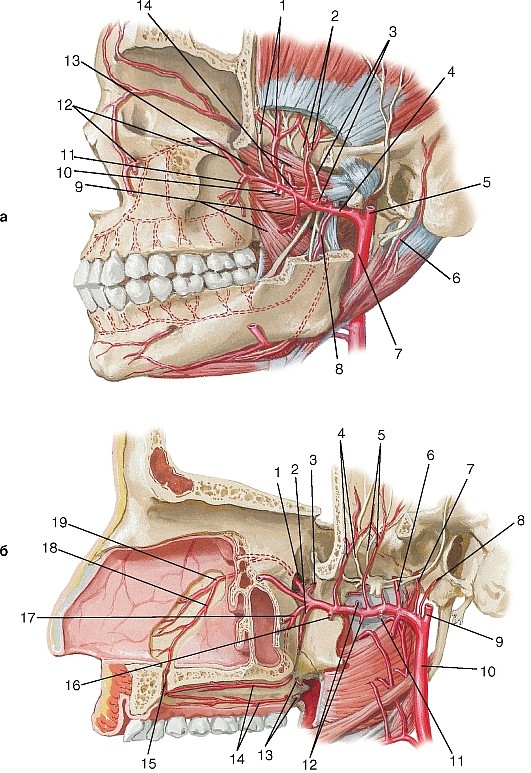
Ветви верхнечелюстной артерии. Отрезки верхнечелюстной артерии (a. maxillaris)
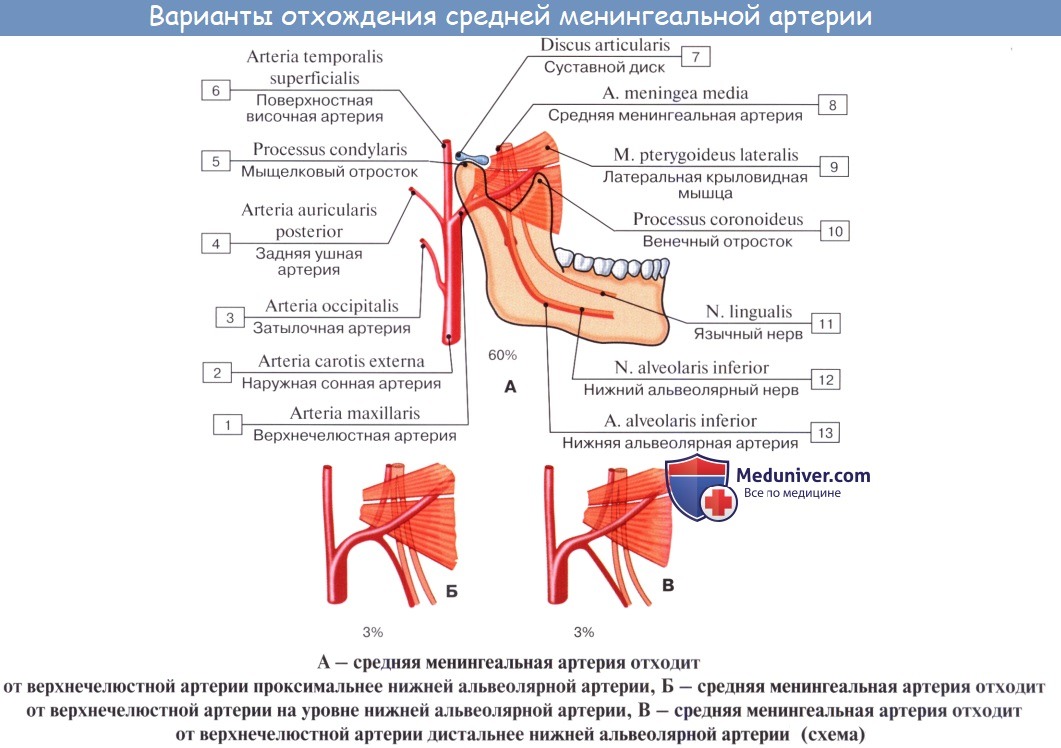
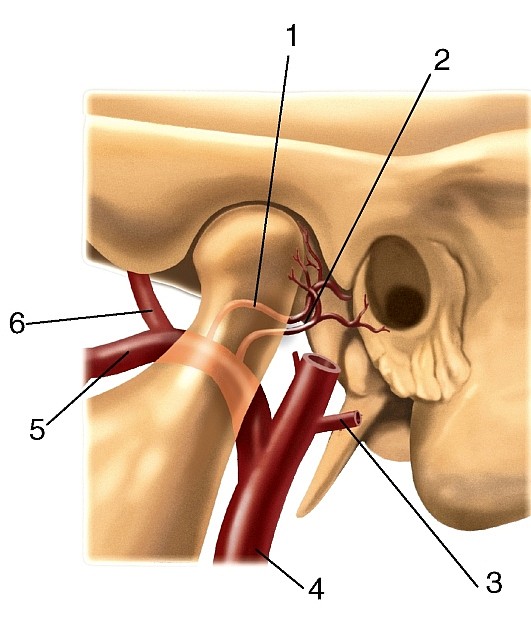
Ветви первого отдела верхнечелюстной артерии идут вверх к наружному слуховому проходу, в барабанную полость, куда они проникают через fissura petrotympanica; к твердой оболочке головного мозга — a. meningea media, средняя менингеальная артерия (самая крупная ветвь), куда она проникает через foramen spinosum, и вниз — к нижним зубам, a. alveolaris inferior, нижняя альвеолярная артерия.
Последняя проходит в нижнюю челюсть через canalis mandibulae. До вступления в канал a. alveolaris inferior отдает r. mylohyoideus к соименной мышце, а в канале снабжает своими ветвями нижние зубы и выходит из него через foramen mentale, получив название a. mentalis (подбородочная артерия), которая разветвляется в коже и мышцах подбородка.
Ветви второго отдела верхнечелюстной артерии идут ко всем жевательным и щечному мускулам, получая соответствующие мышцам названия, а также к слизистой оболочке sinus maxillaris и верхним коренным зубам — аа. alveolares superiores posteriores, задние верхние альвеолярные артерии.
Ветви третьего отдела верхнечелюстной артерии:
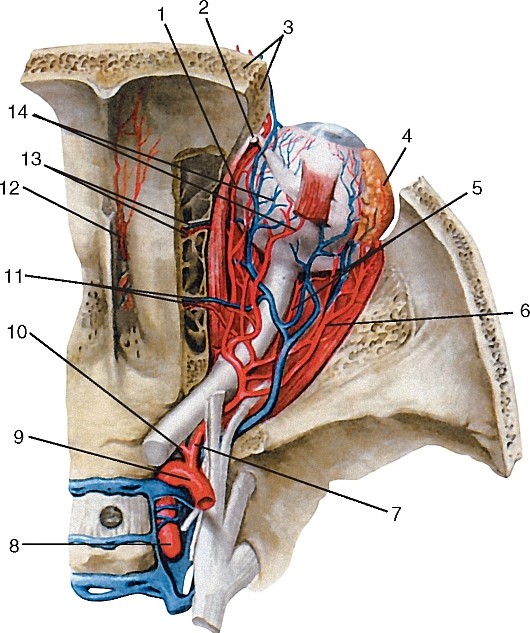
1) a. infraorbital, подглазничная артерия, входит через fissura orbitalis inferior в глазницу, затем через canalis infraorbitalis выходит на переднюю поверхность верхней челюсти и посылает ветви к нижнему веку, к слезному мешку и вниз к верхней губе и к щеке.
Здесь она анастомозирует с ветвями лицевой артерии, так что при затруднении кровотока в стволе a. maxillaris кровь в ее бассейн может поступать через a. facialis.
Еще в глазнице a. infraorbitalis дает ветви к мышцам глазного яблока; проходя в подглазничном канале, снабжает веточками клык и резцы <аа. alveolares superiores anteriores)и слизистую sinus maxillaris;
2) ветви к нёбу, глотке и слуховой трубе, часть из которых спускается вниз в canalis palatinus major, выходит через foramina palatina majus et minores и разветвляется в твердом и мягком нёбе;
3) a. sphenopalatina, клиновидно-нёбная артерия, проникает через одноименное отверстие в носовую полость, давая ветви к латеральной стенке ее и к перегородке; передняя часть полости носа получает кровь через аа. ethmoidales anterior et posterior (от a. ophthalmica).
Особенности кровоснабжения в области лица.
Особенности кровоснабжения в области лица.
Челюстно-лицевая область снабжается кровью ветвями наружной сонной артерии, которые образуют группу передних, средних и задних ветвей.
К передней группе относятся щитовидная, язычная и лицевая артерии.
Среднюю группу составляют восходящая глоточная артерия, поверхностная височная и верхнечелюстная артерии.
Заднюю группу образуют грудино-ключично-сосцевидная ветвь, затылочная артерия и задняя ушная артерия.
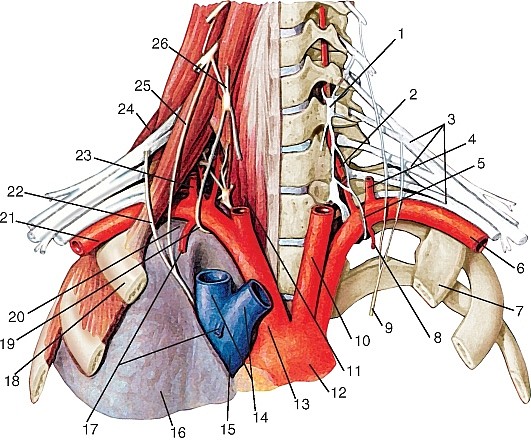
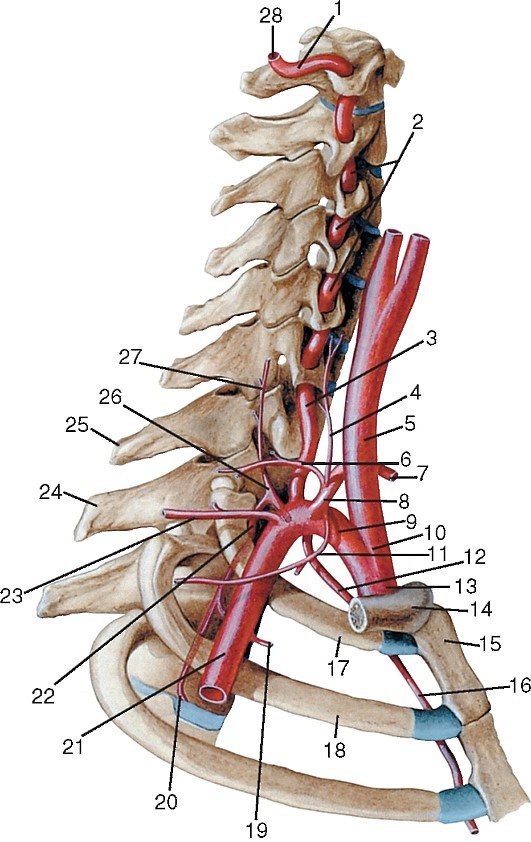
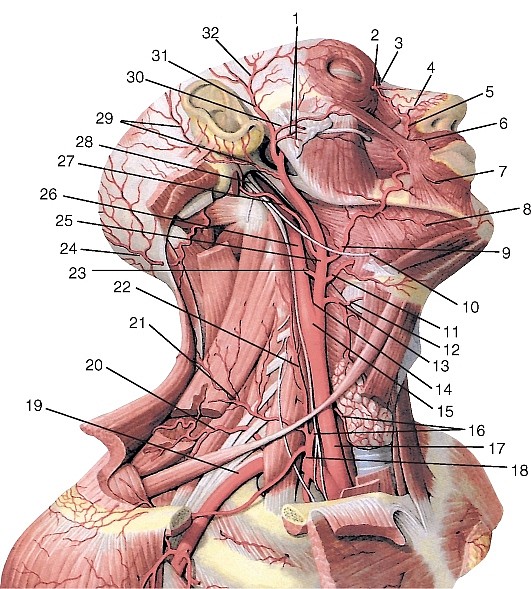
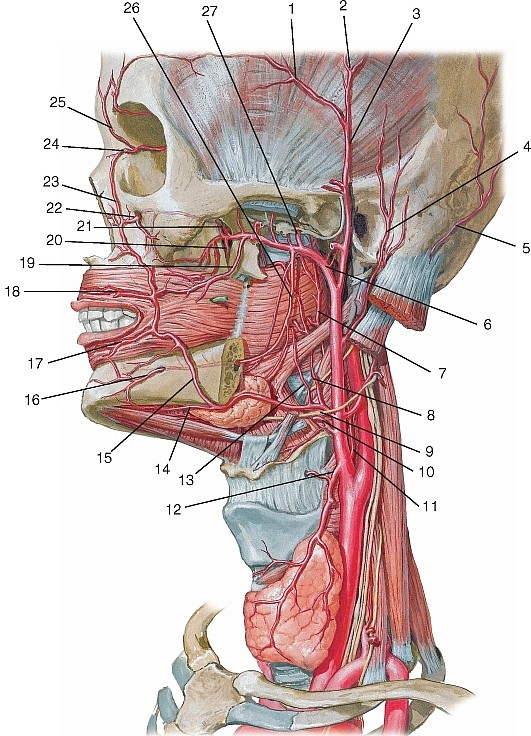
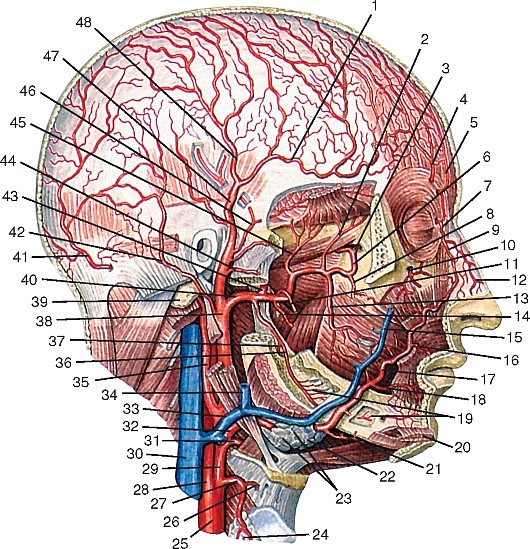
Ветви наружной сонной артерии.
1 – поверхностная височная артерия; 2 – затылочная артерия;
3 – верхнечелюстная артерия; 4 – наружная сонная артерия;
5 – восходящая глоточная артерия; 6 – внутренняя сонная артерия;
7 – мышца, поднимающая лопатку; 8 – трапециевидная мышца;
9 – надлопаточная артерия; 10 – плечевое сплетение;
13 – верхняя щитовидная артерия; 14 – язычная артерия; 15 – лицевая артерия;
16 – переднее брюшко двубрюшной мышцы; 17 – щечная мышца; 18 – средняя менингеальная артерия.
Отток венозной крови от органов и тканей челюстно-лицевой области осуществляется во внутреннюю яремную вену, куда поступает кровь из лицевой вены, крыловидного венозного сплетения, язычной, щитовидной и занижнечелюстной вен.
Лимфа из области головы и шеи собирается в яремные лимфатические стволы, куда поступает также лимфа из сосцевидных, околоушных, поднижнечелюстных, окологлоточных и подбородочных регионарных узлов.
Регуляция кровообращения в сосудистой системе челюстно-лицевой области осуществляется нервным и гуморальным путем. Кроме того, сосуды имеют собственный базальный тонус (миогенный механизмам регуляции).
Сосудодвигательный центр продолговатого мозга по нервным волокнам посылает импульсы через шейные симпатические узлы к сосудам челюстно-лицевой области.
Сосуды лица образуют обильную сеть с хорошо развитыми анастомозами, поэтому раны на лице быстро заживают.
При проведении всех процедур следует быть максимально острожным, чтобы избежать внутриартериального и внутривенного введения препарата.
Безопасно вводить препарат в надкостницу, можно при помощи канюли, которые менее опасны, чем иглы.
ОПАСНЫЕ ЗОНЫ ДЛЯ ВВЕДЕНИЯ ФИЛЛЕРОВ.
Проекция костных отверстий лицевого отдела черепа.
Глубокие инъекции в проекции сосудисто-нервных пучков могут приводить к сдавлению сосудов и нарушению кровоснабжения, могут быть болезненными и вызывать изменение кожной чувствительности.
Область носа содержит много терминальных артерий.
При коррекции данной области важно соблюдать особую осторожность, ведь там проходят терминальные ветви артерий, и инъекционное введение Гиалуроновой кислоты может иметь катастрофические последствия.
Благодаря увеличению научных данных об эмболизации мелких артерий лица после инъекций филлеров, необходимо осуществлять процедуры в области носа только с помощью канюлей.
От глазной артерии Дорсальная носовая артерия Сосуды угла носа Латеральная носовая артерия
От наружной сонной артерии Артерия колумеллы.
Межбровная область.
При инъекциях филлерами в область глабелы, может развится локальный некроз из-за малого количества сосудов в этой зоне.
В зоне отграниченной точками фиксации к кости m. orbicularis oculi с боков, m. сorrugator supercilii сверху и m. procerus снизу распределение филлера затруднено (особенно препаратов высокой вязкости ГК), создается высокое локальное давление препарата на ткани и сосуды.
Височная и периорбитальная области.
Поверхностная височная (сторожевая) вена находится в височной области позади от одноимённой артерии и повторяет её ход. Пересекая височную область на 1—1,5 см выше скуловой дуги, вена в слое подкожной жировой клетчатки направляется к ушной раковине.
У медиального края орбиты, поверхностно расположена угловая вена, она через вены глазницы сообщается с кавернозным синусом твердой мозговой оболочки.
Неосторожное введение филлера в просвет вены или избыточное его количество может привести к тромбозу, гематоме или более поздним осложнениям инфекционного характера.
temporales (височная ветвь) лицевого нерва в височной области залегает под SMAS и направляется к хвосту брови.
Место его поверхностного залегания расположено в проекции треугольника, вершина которого расположена на 2 см. выше конца брови, а основание – по нижнему скуловой дуги.
Околоушная слюнная железа в форме перевернутого треугольника с основанием на скуловой дуге и вершиной в области угла нижней челюсти.
Проток околоушной слюнной железы залегает ниже и параллельно скуловой дуги под слоем SMAS, он горизонтально пересекает m. masseter и, попадая в щечную мышцу, оказывается в преддверии ротовой полости.
Повреждение протока приводит к развитию хронического локального воспаления прилежащих мягких тканей.
transversa facies (поперечная артерия лица) расположена в скуловой области. Параллельно и выше протока околоушной железы. Сосуд снабжает кровью мягкие ткани области, включая кожу и подкожную клетчатку посредством сосудов-перфорантов, постоянный перфорант расположен на середине расстояния между крылом носа и слуховым проходом или 3 см медиальнее и 3,5 ниже края орбиты.
При проведении процедур с канюлей в скуловой области, следует избегать повреждения постоянного перфоранта а. transversa facies.
marginalis mandibulae (краевая ветвь нижней челюсти) лицевого нерва находится под SMAS и опускается вниз сначала позади ветви и угла нижней челюсти и, не доходя до заднего края m. depressor anguli oris, заходит на лицо, располагаясь в этой точке на кости.
Глубокие накостные инъекции в этой зоне следует проводить с осторожностью, т.к. эта ветвь иннервирует мышцы нижней губы и часть подкожной мышцы шеи.
Телефоны Учебного центра «Олта»: 8-812-248-99-34, 8-812-248-99-38, 8-812-243-91-63, 8-929-105-68-44
Сосуды головы и шеи. Анатомия. Видеоатлас доктора Роберта Акланда. Часть 1, 2.
Сосуды головы и шеи. Анатомия. Видеоатлас доктора Роберта Акланда. Часть 1, 2.
Сосуды головы и шеи. Часть 1. Автор лекции профессор В. А. Изранов
Сосуды головы и шеи. Часть 2. Автор лекции профессор В. А. Изранов
АРТЕРИИ ГОЛОВЫ И ШЕИ
Ветви первого отдела (рис. 179):
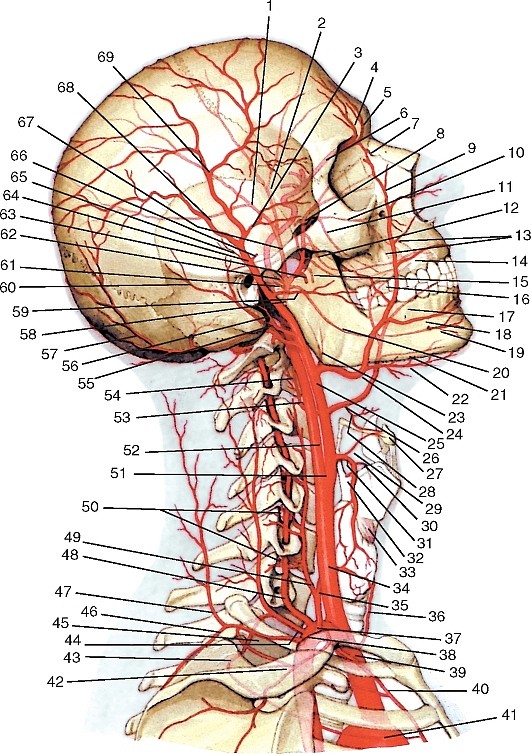
Рис. 177. Общий вид артерий головы и шеи, вид справа (схема):
Ветви базилярной артерии:
3) задняя мозговая артерия (a. cererbriposterior), посылающая артерии затылочной доле конечного мозга.
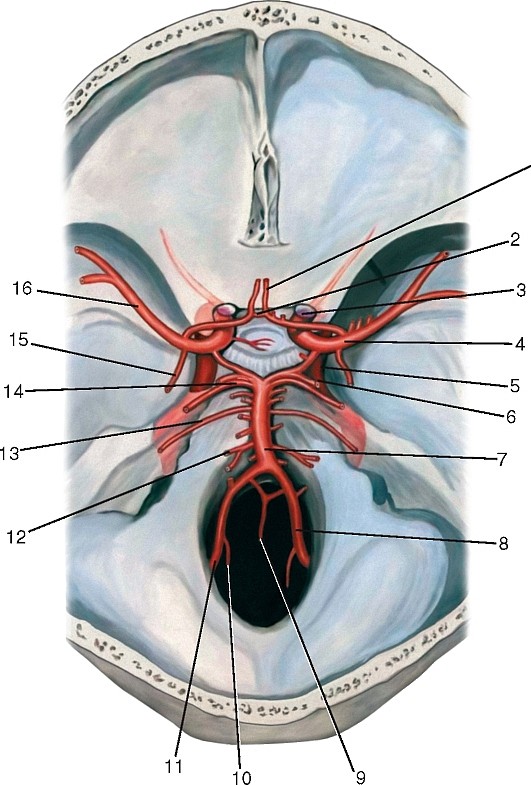
Рис. 180. Ветви базилярной и внутренней сонной артерий в полости черепа, вид со стороны полости черепа:
2) восходящую шейную (a. cervicalis ascendens);
Артерии третьего отдела (см. рис. 179).
Внутренняя сонная артерия (a. carotis interna) парная, отходит от общей сонной артерии на уровне верхнего края щитовидного хряща; в артерии выделяют 4 части: шейную, каменистую, пещеристую и мозговую (рис. 186, 187, см. рис. 177, 180, 181).
На шее внутренняя сонная артерия сначала располагается латеральнее наружной сонной артерии, затем направляется кверху и медиальнее ее, идет между внутренней яремной веной (снаружи) и глот кой (изнутри) и достигает наружной апертуры сонного канала. На шее ветвей не отдает. Каменистая часть (pars pertrosa) расположена в сонном канале пирамиды височной кости и окружена густыми венозным и нервным сплетениями; здесь артерия переходит из вертикального положения в горизонтальное. В пределах канала от нее отходят сонно-барабанные артерии (аа. caroticotimpanicae), проникающие через отверстия в стенке канала в барабанную полость, где они анастомозируют с передней барабанной и шилососцевидной артериями.
Задняя соединительная артерия (a. communicans posterior) соединяет внутреннюю сонную артерию с задней мозговой артерией (см. рис. 180, 181).
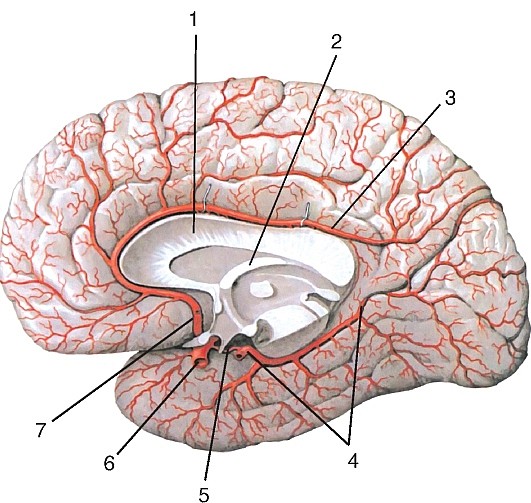
Передняя мозговая артерия (a. cerebri anterior) идет на медиальную поверхность лобной доли мозга, прилегая сначала к обонятельному треугольнику, затем в продольной щели большого мозга переходит на верхнюю поверхность мозолистого тела; кровоснабжает конечный мозг. Недалеко от своего начала правая и левая передние мозговые артерии соединяются посредством передней соединительной артерии (a. communicans anterior) (см. рис. 181, 188).
Рис. 186. Внутренняя сонная артерия, вид справа:
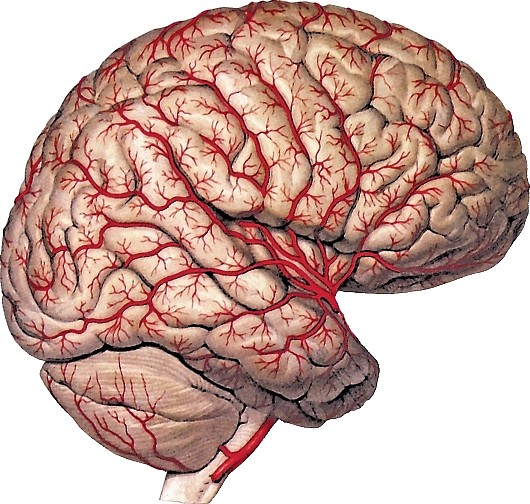
Средняя мозговая артерия (a. cerebri media) более крупная, располагается в латеральной борозде, по которой восходит вверх и латерально; отдает ветви к конечному мозгу (см. рис. 181, 189).
Рис. 188. Артерии на медиальной и нижней поверхностях полушария головного мозга:
Рис. 189. Ветви средней мозговой артерии на дорсолатеральной поверхности полушария головного мозга
Верхняя щитовидная артерия (a. thyroidea superior) отходит вблизи бифуркации общей сонной артерии ниже большого рога подъязычной кости, идет дугообразно вперед и вниз к верхнему полюсу щитовидной железы (рис. 191, см. рис. 177, 184, 186). Анастомозирует с нижней щитовидной артерией и верхней щитовидной артерией противоположной стороны. Отдает подподъязычную ветвь (r. infrahyoideus), грудино-ключично-сосцевидную ветвь (r. sternocleidomastoideus) и верхнюю гортанную артерию (а. laringea superior), сопровождающую верхний гортанный нерв и кровоснабжающую мышцы и слизистую оболочку гортани выше голосовой щели.
Рис 192. Язычная артерия, вид слева:
От лицевой артерии отходят артерии к соседним органам:
1) восходящая нёбная артерия (а. palatina ascendens) идет кверху между шилоглоточной и шилоязычной мышцами, проникает через глоточно-базилярную фасцию и снабжает кровью мышцы глотки, нёбную миндалину, мягкое нёбо;
2) миндаликовая ветвь (r. tonsillaris) прободает верхний констриктор глотки и разветвляется в глоточной миндалине и корне языка (см. рис. 186);
3) железистые ветви (rr. glandulares) идут к поднижнечелюстной слюнной железе;
4) подподбородочная артерия (а. submentalis) отходит от лицевой артерии у места ее перегиба через основание нижней челюсти и идет кпереди под челюстно- подъязычной мышцей, отдавая ветви к ней и к двубрюшной мышце, затем подходит к подбородку, где разделяется на поверхностную ветвь к подбородку и глубокую ветвь, перфорирующую челюстно-подъязычную мышцу и кровоснабжающую дно полости рта и подъязычную слюнную железу;
5) нижняя губная артерия (а. labialis inferior) ответвляется ниже угла рта, извилисто продолжается между слизистой оболочкой нижней губы и круговой мышцей рта, соединяясь с одноименной артерией другой стороны; дает ветви к нижней губе;
6) верхняя губная артерия (а. labialis superior) отходит на уровне угла рта и проходит в подслизистом слое верхней губы; анастомозирует с одноименной артерией противоположной стороны, составляя околоротовой артериальный круг.
Отдает ветви к верхней губе.
На лице наружная сонная артерия располагается в занижнечелюстной ямке, в паренхиме околоушной слюнной железы или глубже нее, кпереди и латеральнее внутренней сонной артерии. На уровне шейки нижней челюсти она разделяется на конечные ветви: верхнечелюстную и поверхностную височную артерии.
1) поперечная артерия лица (a. transversa faciei) ответвляется в толще околоушной слюнной железы ниже наружного слухового прохода, выходит из-под переднего края железы вместе со щечными ветвями лицевого нерва и разветвляется над протоком железы; кровоснабжает железу и мышцы лица. Анастомозирует с лицевой и подглазничной артериями;
2) скулоглазничная артерия (а. zygomaticifacialis) отходит выше наружного слухового прохода, идет вдоль скуловой дуги между пластинками височной фасции к латеральному углу глазной щели; кровоснабжает кожу и подкожные образования в области скуловой кости и глазницы;
3) средняя височная артерия (a. temporalis media) отходит над скуловой дугой, перфорирует височную фасцию; кровоснабжает височную мышцу; анастомозирует с глубокими височными артериями.
Рис. 195. Артерии среднего уха:
Глубокая ушная артерия (a. auricularis profunda) проходит назад и кверху к наружному слуховому проходу, отдаёт ветви к барабанной перепонке.
Передняя барабанная артерия (a. tympanica anterior) проникает по барабанно- чешуйчатой щели в барабанную полость, снабжает кровью её стенки и барабанную перепонку. Нередко отходит общим стволом с глубокой ушной артерией.
Анастомозирует с артерией крыловидного канала, шилососцевидной и задней барабанной артериями.
Средняя менингеальная артерия (a. meningea media) поднимается между крыловидно-нижнечелюстной связкой и головкой нижней челюсти по медиальной поверхности латеральной крыловидной мышцы, между корешками ушно- височного нерва к остистому отверстию и через него входит в твёрдую оболочку головного мозга. Обычно залегает в борозде чешуи височной кости и борозде теменной кости. Разделяется на ветви: теменную (r. parietalis), лобную (r. frontalis) и глазничную (r. orbitalis). Анастомозирует с внутренней сонной артерией через анастомотическую ветвь со слезной артерией (r. anastomoticum cum a. lacrimalis). Отдаёт также каменистую ветвь (r. petrosus) к тройничному узлу, верхнюю барабанную артерию (a. tympanica superior) к барабанной полости.
Глубокие височные артерии, передняя и задняя (aa. temporales profundae anterior et posterior) идут в височную ямку, располагаясь между височной мышцей и костью. Кровоснабжают височную мышцу. Анастомозируют с поверхностной и средней височными и слезной артериями.
Крыловидные ветви (rr. pterygoidei) снабжают кровью крыловидные мышцы.
Щечная артерия (a. buccalis) проходит вместе со щечным нервом вперед между медиальной крыловидной мышцей и ветвью нижней челюсти к щечной мышце, в которой разделяется; анастомозирует с лицевой артерией.
Ветви крыловидно-нёбной части (рис. 198, см. рис. 186):
Задняя верхняя альвеолярная артерия (a. alveolaris superior posterior) отходит в месте перехода верхнечелюстной артерии в крыловидно- нёбную ямку позади бугра верхней челюсти. Через задние верхние альвеолярные отверстия проникает в кость; разделяется на зубные ветви (rr. dentales), проходящие вместе с задними верхними альвеолярными нервами в альвеолярные каналы в заднелатеральной стенке верхней челюсти к корням верхних больших коренных зубов. От зубных ветвей отходят околозубные ветви (rr. peridentales) к тканям, окружающим корни зубов.
Подглазничная артерия (a. infraorbitalis) ответвляется в крыловидно- нёбной ямке, являясь продолжением ствола верхнечелюстной артерии, сопровождает подглазничный нерв. Вместе с подглазничным нервом через нижнюю глазничную щель входит в глазницу, где располагается в одноименной борозде и в канале.
Выходит через подглазничное отверстие в клыковую ямку. Конечные ветви снабжают кровью прилежащие лицевые образования. Анастомозируют с глазной, щечной и лицевой артериями. В глазнице посылает ветви к глазным мышцам, слёзной железе. Через одноименные каналы верхней челюсти отдает передние верхние альвеолярные артерии (aa. alveolares superiors anterior et posterior), от которых к корням зубов и околозубным образованиям (rr. peridentales) направляются зубные ветви (rr. dentales).
Артерия крыловидного канала (a. canalis pterygoidei) нередко отходит от нисходящей нёбной артерии, направляется в одноименном канале вместе с одноименным нервом к верхнему отделу глотки; кровоснабжает слуховую трубу, слизистую оболочку барабанной полости и носовую часть глотки.
Нисходящая нёбная артерия (a. palatine descendens) проходит в большом небном канале, где разделяется на большую нёбную артерию (a. palatine major) и малые нёбные артерии (aa. palatinae minores), выходящие, соответственно, через большое и малые нёбные отверстия на нёбо. Малые нёбные артерии идут к мягкому нёбу, а большая распространяется кпереди, кровоснабжает твердое нёбо и оральные поверхности десен. Анастомозирует с восходящей нёбной артерией.
Клиновидно-нёбная артерия (a. sphenopalatina) идет через одноименное отверстие в носовую полость и разделяется на задние носовые латеральные артерии (aa. nasalis posteriors laterales) и задние перегородочные ветви (rr. septales posteriors). Кровоснабжает задние ячейки решетчатого лабиринта, слизистую оболочку боковой стенки носовой полости и перегородки носа; анастомозирует с большой нёбной артерией (табл. 13).
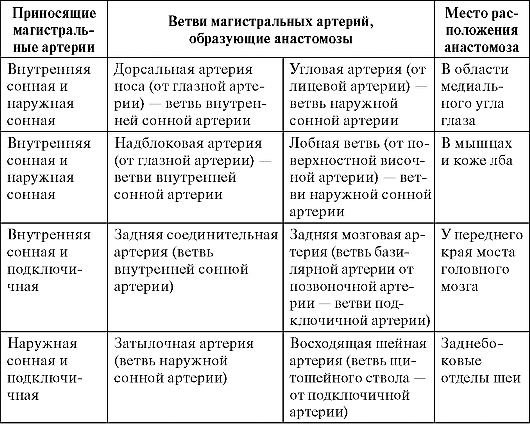
Таблица 13. Межсистемные анастомозы артерий головы и шеи
Вопросы для самоконтроля
1. Какие ветви отходят от подключичной артерии в каждом из отделов?
2. Какие ветви позвоночной артерии вы знаете? С какими артериями она анастомозирует?
4. Какие части топографически различают во внутренней сонной артерии?
5. Какие ветви отходят от каждой части внутренней сонной артерии?
6. Какие артерии кровоснабжают содержимое глазницы?
7. Какими артериями образуется артериальный круг большого мозга?
8. Как можно представить себе топографию наружной сонной артерии?
9. Какие передние ветви наружной сонной артерии вам известны?
11. Какие артерии отходят от лицевой артерии? Какие анастомозы имеет лицевая артерия?
12. Какие артерии отходят от верхнечелюстной артерии в каждой ее части?
13. Какие вы знаете анастомозы верхнечелюстной артерии?
Рекомендации по лечению гигантоклеточного артериита французской группы по изучению васкулитов крупных сосудов
Гигантоклеточный артериит (старое название – височный артериит) – это самый распространенный системный васкулит, который развивается у людей пожилого и старческого возраста. В статье приводятся основные положения французских рекомендаций по диагностике и лечению гигантоклеточного артериита, а также их критический анализ.
Гигантоклеточный артериит (ГКА) – это самый распространенный системный васкулит в мире. В некоторых северно-европейских странах распространенность ГКС достигает 10-20 случаев на 100 000 населения. Данных о заболеваемости ГКА в нашей стране нет, однако можно предположить, что это заболевание часто остается недиагностированным у пожилых людей с «необъяснимым» повышением СОЭ, лихорадкой неясного генеза или впервые возникшей головной болью. За последние 3 года в мировой медицинской литературе отмечается информационный бум, связанный с появлением большого количества исследований, касающихся различных аспектов ГКА. Одним из знаковых событий информационной волны стали рекомендации французской группы по изучению васкулитов крупных сосудов (GEFA), которые остаются современными и хорошо освещают актуальную для многих специалистов (ревматологов, терапевтов, офтальмологов, неврологов) проблему ГКА [1]. Еще одним важным событием стала регистрация тоцилизумаба для лечения ГКА в США (май 2017 г.) и Европе (сентябрь 2017 г.) на основании результатов крупного международного исследования GiACTA [2], которые были опубликованы уже после выхода в свет рекомендаций GEFA.
Мы хотели бы познакомить читателя с рекомендациями GEFA по диагностике и лечению ГКА, а также прокомментировать некоторые позиции наших французских коллег и обсудить возможности биологической терапии у пациентов с ГКА.
Терминология
В прошлом ГКА часто именовали «височным» или «краниальным» артериитом, однако в настоящее время эти названия неактуальны. Термин «болезнь Хортона» (по имени американского невролога, который описал этот васкулит в 1932 г.) нередко используется в Европе, особенно Франции. Однако сегодня наиболее популярен (почти 70% публикаций) термин «ГКА», который был одобрен на Международной согласительной конференции в Чапел-Хилле, а также указан в классификации васкулитов Американской коллегии ревматологов. Этот термин можно использовать не только в случае морфологической верификации диагноза. Он является синонимом «болезни Хортона» даже в тех случаях, когда при биопсии височной артерии не было выявлено типичных для ГКА изменений.
Номенклатура и классификация
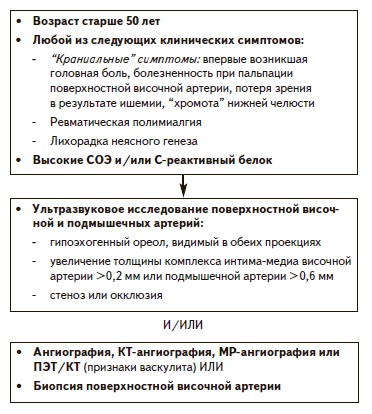
ГКА относится к васкулитам, поражающим крупные сосуды, в том числе аорту и отходящие от нее ветви, преимущественно внешние сонные и позвоночные артерии и, в отличие от артериита Такаясу, развивается в возрасте старше 50 лет. Ревматическая полимиалгия отличается от ГКА отсутствием клинических и гистологических признаков поражения краниальных сосудов и органа зрения. В соответствии с критериями Аме риканской коллегии ревматологов системный васкулит может быть классифицирован как ГКА при наличии «краниальной» симптоматики (новые головные боли, пальпаторные изменения височных артерий или положительные результаты биопсии). Эти критерии позволяют дифференцировать ГКА от других системных васкулитов с чувствительностью 94% и специфичностью 91% [3].
Комментарий авторов рекомендаций: при отсутствии верифицированного васкулита классифицировать болезнь как ГКА затруднительно. Определенное диагностическое значение имеют косвенные признаки, такие как ответ на лечение глюкокортикостероидами и течение болезни.
Клинический диагноз
Существуют достаточно специфичные для ГКА признаки. По данным мета-анализа [4], самыми сильными предикторами гистологического подтверждения диагноза были «хромота» нижней челюсти (34% больных) и диплопия (9%). В другом исследовании было показано, что вероятность гистологически подтвержденного ГКА значительно увеличивалась при наличии головной боли (86%), «хромоты» нижней челюсти (42%) и пальпируемой височной артерии (44%) [5]. Сочетание ревматической полимиалгии с «новой» головной болью, «хромотой»нижней челюсти и изменениями височных артерий (по данным осмотра) позволяло установить диагноз с точностью 97%, а начало болезни после 70 лет увеличивало предсказательное значение положительного результата до 100%, однако такое сочетание отмечали только у 27% больных с ревматической полимиалгией [6].
Комментарий: некроз языка или волосистой части головы, а также острые нарушения зрения, вероятно, также имеют высокое диагностическую значение, хотя оно не доказано результатами исследований.
Биопсия височной артерии
Диагноз ГКА может быть подтвержден при биопсии височной артерии. К характерным гистологическим признакам данного васкулита относятся воспалительный инфильтрат, содержащий гигантский клетки, в мышечной оболочке артерии, а также эластофагия [7], хотя оба указанных признака наблюдаются не всегда [8]. Изолированный воспалительный инфильтрат вокруг адвентиция или васкулит мелких сосудов, окружающих височную артерию (редко некротизирующий), встречаются реже и могут быть признаком вовлечения в патологический процесс височной артерии при другом системном васкулите.
Диагноз ГКА подтверждается результатами биопсии височной артерии у 49-85% больных 9. Значи тельная вариабельность результатов, возможно, отражает различия в клинических и гистологических определениях ГКА, а также технические особенности проведения биопсии. Повысить диагностическую информативность исследования позволяет использование биоптатов длиной не менее 0,5–1 см, а также скольких образцов. При односторонней биопсии височной артерии диагностируют 88% случаев ГКА, верифицированных гистологически [13]. Значение допплеровского ультразвукового сканирования для выбора места биопсии остается спорным. Гистологические изменения можно выявить в течение по крайней мере 15 дней после начала лечения глюкокортикоидами. Осложнения биопсии височной артерии встречаются редко [14].
Комментарий: в настоящее время не существует единых гистологических критериев диагноза ГКА.
Визуализация височной артерии
Визуализацию височной артерии, прежде всего с помощью допплеровского ультразвукового сканирования линейным датчиком, считают возможным методом подтверждения диагноза ГКА. При наличии гипоэхогенного ореола (гало) чувствительность ультразвукого исследования составляет 68%, а специфичность достигает 91% [15], особенно если указанные изменения определяются с двух сторон. Чувствительность повышается, если ореол исследуют в подмышечных и общих сонных артериях [16]. Роль магнитно-резонансной томографии (МРТ) в диагностике ГКА изучена в меньшей степени. Диагноз ГКА позволяют предположить утолщение сосудистой стенки с накоплением контраста в средней оболочке и сужением просвета [17]. В самых крупных исследованиях, в которых учитывали поражение височных и затылочных артерий, чувствительность составляла 78%, а специфичность – 90% [18]. По информативности допплеровское ультразвуковое сканирование и МРТ существенно не отличались.
Комментарии: визуализация височной артерии является менее надежным методом диагностики ГКА по сравнению с биопсией. Учитывая вариабельность результатов исследований и их зависимость от навыка специалиста, практическое значение допплеровского ультразвукового сканирования оценить достаточно трудно. Во Франции этот метод используется ограничено. МРТ изучена еще в меньшей степени, а также существенно дороже и менее доступна, чем ультразвуковое исследование.
Роль визуализации аорты и ее ветвей в диагностике ГКА
Выявление аортита или артериита ветви аорты с помощью КТ-ангиографии, МР-ангиографии или позитронно-эмиссионной томографии с использованием 18-фтордезоксиглюкозы (ПЭТ) позволяет предположить диагноз ГКА. Признаком аортита считают равномерное кольцевидное утолщение стенки ≥2 или 3 мм по данным КТ-ангиографии, накопление гадолиния в сосудистой стенке при МР-ангиографии или 18-фтордезоксиглюкозы при ПЭТ. Частота аортита по данным КТ-ангиографии или МР-ангиографии составляет от 33 до 65%. По данным 2 мета-анализов, чувствительность и специфичность ПЭТ в диагностике аортоартериита при ГКА составили 80-89% и 90-98%, соответственно [19]. По чувствительности ПЭТ незначительно превосходила МРТ, а также КТ-ангиографию. При допплеровском сканировании можно выявить гало в общих сонных, подмышечных, подвздошных и бедренных артериях.
Комментарии: данные литературы неоднозначны, однако они свидетельствуют о том, что визуализация аорты и ее ветвей менее специфична в диагностике ГКА, чем биопсия височной артерии. Не вполне понятно диагностическое значение небольшого увеличения толщины стенки или незначительного накопления контрастного вещества.
Биомаркеры
Увеличение СОЭ ≥50 мм/ч (по методу Вестергрена) является одним из классификационных критериев Американской коллегии ревматологов. Воспалительные маркеры почти всегда повышены в дебюте ГКА, при этом среднее значение СОЭ составляет 93 мм/ч, концентрации С-реактивного белка (СРБ) – 94 мг/л [20]. Также может повышаться уровень других воспалительных белков – фибриногена, гаптоглобина, орозомукоида. Анемия отмечается у 55% больных, тромбоцитоз – у 49% [20]. Тем не менее, у 11% больных СОЭ не превышает 50 мм/ч [21], а нормальные уровни воспалительных маркеров не исключают диагноз ГКА. Описана связь между небольшим повышением cодержания воспалительных маркеров и развитием ишемических поражений органа зрения [22].
Комментарии: в настоящее время не существует специфических для ГКА биомаркеров, позволяющих определить вариант болезни и прогнозировать ее течение.
Аневризма аорты при ГКА
Аневризма аорты, особенно в восходящем отделе грудной аорты, развивается у пациентов с ГКА чаще, чем в популяции, и ассоциируется со снижением выживаемости [23]. По данным когортных исследований, частота аневризмы и/или расслоения стенки аорты у больных ГКА составляет 19 на 1000 в год [24,25]. Аневризма может быть выявлена спустя несколько лет после установления диагноза ГКА, однако у 15% пациентов с аортитом аневризма или дилатация грудного отдела аорты отмечается уже при установлении диагноза [26].
Комментарии: в настоящее время не установлены факторы риска развития аневризмы аорты у пациентов с ГКА и не определены возможности скрининга (способ визуализации, частота исследований). При КТ и МРТ для оценки диаметра аорты контрастирование медии не требуется, однако оно позволяет оценить состояние сосудистой стенки и просвет сосуда. Возможности обычной рентгенографии органов грудной клетки в диагностике патологии аорты крайне ограничены.
Глюкокортикоистероиды в лечении неосложненного ГКА (без поражения органа зрения, аорты и ее ветвей)
Глюкокортикоиды остаются «золотым стандартом» лечения ГКА. Начальная доза у пациентов с неосложненным ГКА составляет от 0,3 до 1 мг/кг/сут в пересчете на преднизолон. В некоторых исследованиях показано, что дозы 0,5-0,7 мг/кг/сут обычно достаточно для подавления активности болезни, при этом они удовлетворительно переносятся. В рандомизированных клинических исследованиях пульс-терапия метилпреднизолоном (15 мг/кг/сут) до назначения пероральных глюкокортикостероидов обеспечивала дополнительное снижение частоты обострений и оказывала стероидосберегающее действия [27]. Прием препарата в стартовой дозе продолжают в течение 2-4 недель в зависимости от скорости разрешения воспалительных изменений. Снижение дозы глюкокортикоcтероидов начинают быстро, чтобы достичь дозы 15-20 мг/сут за 6-10 недель. Проспективные и ретроспективные исследования показали, что примерно у половины пациентов удается снизить дозу до 7,5-10 мг/сут за 6 месяцев [28]. В то же время прекращение приема глюкокортикостероидов через 6 мес в 77% случаев сопровождалось развитием обострений в течение последующего года [29]. Медиана длительности лечения в когортных исследованиях составляла около 24 мес, однако она варьировалась в широких пределах и иногда достигала нескольких лет.
Комментарии: в настоящее время нет общего мнения по поводу выбора стартовой дозы глюкокортикостероидов у пациентов с неосложненным ГКА. Пульс-терапия у пожилых людей или пациентов с сопутствующими заболеваниями может быть рискованной.
Лечение ГКА с поражением органа зрения
Поражение органа зрения – наиболее частое тяжелое осложнение ГКА, которое в 13-19% случаев приводит к необратимому снижению остроты зрения или слепоте вследствие окклюзии ветвей зрительной артерии или, реже, инсульта в бассейне задней затылочной артерии. В трети случаев отмечается поражение обоих глаз. У 95% пациентов нарушение зрения развивается до начала лечения глюкокортикоидами, а у 20% больных представляет собой первое проявление васкулита. У небольшой части больных терапия глюкокортикостероидами, начатая в течение первых 72 ч после ухудшения зрения, позволяет добиться частичного его восстановления. Лучших результатов удавалось добиться при назначении преднизолона внутрь в дозе как минимум 60 мг/сут [30,31] или метилпреднизолона в дозе 500 мг внутривенно [32,33]. По данным двух ретроспективных исследований высказано предположение, что низкие дозы аспирина позволяют предотвратить ишемические поражения органа зрения и центральной нервной системы [34,35], хотя этот вопрос остается спорным, учитывая отсутствие адекватных исследований.
Комментарии: в настоящее время недостаточно данных проспективных или контролируемых клинических исследований, чтобы определить оптимальный режим глюкокортикоидной терапии или целесообразность использования низких доз аспирина для лечения ГКА с поражением органа зрения.
Лечение ГКА с поражением аорты и ее ветвей
Воспаление аорты или ее ветвей может осложниться развитием дилатации, аневризмы или расслоения стенки аорты, а также стенозом или окклюзией ее крупной ветви. В ретроспективных или проспективных исследованиях эффективность различных режимов терапии глюкокортикоидами или стероидосберегающих препаратов при ГКА с поражением крупных артерий не изучалась. Аортит или поражение подключичных артерий, независимо от тяжести, может ассоциироваться с повышенным риском обострения, стероидной зависимости и смертности от сердечно-сосудистых событий [36,37], хотя это убедительно не доказано [38]. Аневризма или расслоение стенки аорты (но не стеноз ее крупной ветви) сопровождаются повышенной сердечно-сосудистой смертностью [23]. Эмпирически пациентам с признаками ишемии конечностей назначают преднизолон в дозе 1 мг/кг/сут. Эндоваскулярные или хирургические вмешательства по поводу аневризмы аорты проводят по тем же принципам, что и пациентам без ГКА. Острое расслоение стенки аорты – это неотложное хирургическое состояние.
Комментарии: остается открытым вопрос о том, требуется ли пациентам с ГКА и бессимптомным аортоартериитом более интенсивное медикаментозное лечение.
Применение иммуносупрессивных препаратов
Целесообразность присоединения иммуносупрессивных препаратов к лечению глюкокортикостероидами с целью достижения стероидосберегающего эффекта или снижения риска обострений в настоящее время яв ляется предметом исследований. Эффективность метотрексата изучалась в 3 рандомизированных плацебо-контролируемых исследованиях [29,39,40] и метаанализах [41,42]. По данным одного мета-анализа, применение метотрексата внутрь в дозе 7,5-15 мг/нед снижало риск обострения и кумулятивную дозу глюкокортикоидов [41]. В небольшом плацебо-контролируемом исследовании у пациентов с ГКА или ревматической полимиалгией азатиоприн (150 мг/сут) также оказывал стероидосберегающее действие через 12 мес [43]. В то же время рандомизированные клинические исследования не подтвердили пользу назначения циклоспорина, гидроксихлорохина или дапсона. Данные неконтролируемых ретроспективных исследований свидетельствуют о возможной эффективности циклофосфамида, лефлуномида и микофенолата мофетила у пациентов с активным ГКА.
Комментарии: в настоящее время у нас нет достаточных данных в пользу назначения какого-либо дополнительного иммуносупрессивного или иммуномодулирующего препарата, кроме метотрексата. Эффективность метотрексата представляется невысокой.
Генно-инженерные биологические препараты
В трех рандомизированных исследованиях у пациентов с ГКА не была подтверждена эффективность ингибиторов фактора некроза альфа, в том числе инфликсимаба, этанерцепта и адалимумаба 46, хотя в одном из них применение этанерцепта привело к снижению кумулятивной дозы глюкокортикоидов в течение 12 мес [46]. Другие генно-инженерные препараты изучались в неконтролируемых исследованиях у пациентов с обострением или рефрактерным течением ГКА, обычно после использования метотрексата. Наиболее перспективным препаратом представляется тоцилизумаб (см. ниже результаты исследования GiACTA). Также сообщалось об эффективности анакинры и ритуксимаба у нескольких пациентов с ГКА.
Аспирин, антикоагулянты и статины
Увеличение риска острых ишемических поражений органа зрения, центральной нервной и сердечно-сосудистой систем у пациентов с ГКА как в ближайшем, так и отдаленном периоде ставит вопрос о необходимости профилактики сосудистой патологии. Данные нескольких когортных и ретроспективных исследований, а также мета-анализа [47] свидетельствуют о том, что у пациентов с ГКА, принимающих глюкокортикоиды, низкие дозы аспирина (≤100 мг/cут) снижают риск острых мозговых или зрительных ишемических событий, а также в целом риск сердечно-сосудистых катастроф. Другое ретроспективное исследование продемонстрировало протективный эффект низких доз аспирина в отношении риска обострений системного васкулита [48]. Возможные преимущества антикоагулянтной терапии не доказаны. В 3 ретроспективных когортных исследованиях 50 статины не оказывали стероидосберегающее действие, в то время как обсервационное популяционное исследование показало способность статинов снижать продолжительность лечения глюкокортикостероидами [52].
Комментарии: профилактическое назначение низких доз аспирина и статинов должно соответствовать текущим рекомендациям по профилактике осложнений атеросклероза.
Лечение обострений и рецидивирующего ГКА
Несмотря на достигнутую ранее медикаментозную ремиссию, как минимум у трети пациентов с ГКА отмечаются обострения или рецидивы заболевания. Некоторые авторы различают обострение, которое развивается на фоне лечения, и рецидив, который происходит через некоторое время после отмены стероидной терапии. Для выявления обострения обычно недостаточно изолированного повышения уровня воспалительных маркеров. В контролируемых исследованиях тактика ведения пациентов с обострением или рецидивом ГКА не изучалась. Результаты мета-анализа пациентов с впервые установленным ГКА, участвовавших в 3 рандомизированных плацебо-контролируемых исследованиях, показали, что метотрексат существенно снижает риск обострений, в то время как возможная польза других препаратов, таких как циклофосфамид, лефлуномид или микофенолата мофетил у пациентов с ГКА, требующим применения высоких доз глюко кортикостероидов, или рецидивирующим течением васкулита показана только в неконтролируемых исследованиях.
Комментарии: подходы к лечению ГКА рецидивирующего течения определены недостаточно, в частности остается неясным, следует ли назначать дополнительные иммуносупрессивные препараты в таких случаях.
Обсуждение
Особенностью рекомендаций GEFA является несколько консервативный взгляд на ключевые проблемы диагностики и лечения ГКА. Как это принято в последние годы, данные рекомендации были построены на анализе многочисленной информации, полученной в результате самых разных по дизайну исследований, и голосования экспертов по ключевым позициям. На наш взгляд, эти рекомендации не только представляют собой результат огромной аналитической работы, но и предполагает поиск разумного баланса между традиционными взглядами и новой информацией по проблеме ГКА. По мере накопления новых данных некоторые положения будут обновляться. В чем заключается консерватизм данных рекомендаций?
Сохранение концепции биопсии поверхностной височной артерии как «золотого стандарта» диагностики ГКА. Несмотря на высокую чувствительность биопсии височной артерии (49-85%) в диагностике ГКА, которую указывают авторы данных рекомендаций, нужно помнить, что в реальной клинической практике информативность биопсии может быть значительно ниже, в особенности в тех медицинских центрах, где эта процедура «не поставлена на поток» и нет достаточного опыта в выборе участка биопсии, техники биопсии и морфологического исследования. В настоящее время редко публикуются исследования, демонстрирующие низкую частоту обнаружения морфологически измененной височной артери у пациентов с предполагаемым ГКА, но тем не менее они имеются [53,54]. В этих исследованиях чувствительность биопсии височной артерии при ГКА составляла около 18-30%.
Классификационные критерии Американской коллегии ревматологов 1990 г. сохранили свою актуальность. Прошло уже более 25 лет с момента разработки классификационных критериев ГКА Американской коллегией ревматологов. За этот срок накопился большой опыт использования различных методов визуализации, помогающих в диагностике этого заболевания. Речь идет не только об ультразвуковом исследовании, но и КТангиографии, МР-ангиографии и позитронно-эмиссионной томографии. До настоящего времени ревматическая полимиалгия не рассматривалась как один из возможных диагностических критериев ГКА, хотя включение ее в классификационные критерии ГКА в исследовании GiACTA позволяет обсуждать эту позицию для реальной клинической практики. Важно помнить, что текущие критерии ГКА были разработаны для классической (краниальной) формы ГКА, помимо которой существуют так называемые генерализованные (Такаясу-подобные или LVV-GCA) формы заболевания без краниальной симптоматики, артериит, ассоциированный с ревматической полимиалгией, изолированный аортит у пожилых людей. Пока мы будем опираться на критерии Американской коллегии ревматологов 1990 года, эти формы васкулитов крупных сосудов у пожилых людей будут оставаться за рамками диагностической (и лечебной) концепции ГКА.
Низкие дозы метотрексата для лечения ГКА. Данные, подтверждающие эффективность метотрексата в лечении ГКА, ограничены и отчасти противоречивые. Без сомнения, все исследования, на которых основываются рекомендации по использованию метотрексата в дозе 10-15 мг/нед, относятся к эре «низких доз метотрексата в ревматологии». Нам представляется возможным обсуждать использование метотрексата в дозах 15-20 мг/нед и возможно выше в тех случаях, когда это клинически оправдано.
Ограничение использования аспирина и статинов при ГКА. На наш взгляд, утверждение о целесообразности применения аспирина только в группе пациентов с поражением органа зрения весьма спорное. Офталь мологические проблемы имеют ишемический генез и могут быть связаны как с васкулитом, так и тромбозом, которые нередко сочетаются друг с другом. У ряда пациентов подобные осложнения возникают внезапно, поэтому если рекомендовать назначать антиагреганты только по факту свершившихся офтальмологических осложнений, то это может привести к увеличению риска тромбозов мелких сосудов глаз и головного мозга. Более того у некоторых пациентов даже без краниальной симптоматики наблюдается латентное поражение височной артерии [55]. В нашей клинической практике мы используем антиагреганты (аспирин в дозе 75-150 мг/сут) у всех пациентов с краниальной симптоматикой и у пациентов с генерализованными формами ГКА без краниальных проявлений в первые 6-12 месяцев терапии (при отсутствии противопоказаний). В дальнейшем целесообразность продолжения антиагрегантной терапии зависит от соотношения польза и риска у конкретного пациента.
Антигиперлипидемическая терапии у пациентов в возрасте старше 80 лет с дислипидемией, вызванной длительным приемом преднизолона, вероятно, не улучшит общую выживаемость, однако у пациентов более молодого возраста лечение статинами нам представляется оправданным. Более того, в последнее время во французских же популяционных исследованиях был описан положительный эффект статинов у пациентов с ГКА [56].
Новые и клинически значимые рекомендации. На не ко торых аспектах рекомендаций хотелось бы остановиться подробнее и подчеркнуть их важность.
Применение ультразвукового исследования, КТ-ангиографии, МР-ангиографии и ПЭТ. В рекомендациях впервые были упомянуты дополнительные (к «золотому стандарту», которым авторы считают биопсию поверх ностной височной артерии) методы диагностики ГКА, а именно ультразвуковое исследование, КТ-ангиографию, МР-ангиографию и ПЭТ, что, несомненно, создает основу для изменения текущих классификационных критериев ГКА. В конце 2016 г. были опубликованы данные крупного британского исследования, продемонстрировавшего большое диагностическое значение ультразвукового метода у пациентов с ГКА [57]. Нередко в реальной клинической практики именно результаты визуализации стенки аорты и ее ветвей дают клиницисту необходимую информацию для своевременной постановки диагноза ГКА.
Стратифицированный подход к начальной терапии ГКА и отсутствие необходимости всегда проводить пульс-терапию. Следует обратить особое внимание на дифференцированный подход к выбору начальной дозы глюкокортикостероидов у пациентов с ГКА. В реко мендациях подчеркивается необходимость избегать злоупотребления сверхвысокими дозами глюкокортикостероидов, в том числе в виде пульс-терапии. Необходимо также подчеркнуть, что через 3 мес после начала терапии следует стремиться снизить дозу преднизолона до 15-20 мг/сут с дальнейшим последующим снижением.
Не злоупотреблять цитостатиками при ГКА. Целе со образность использования циклофосфамида, азатио прина, микофенолата мофетила и других иммуносупрессантов (за исключением метотрексата) при ГКА остается под большим вопросом с учетом недоказанной эффективности и сомнительного профиля безопасности у людей пожилого и старческого возраста.
Не применять ингибиторы ФНО-α при ГКА. В рекомендациях GEFA подчеркивается неэффективность ингибиторов ФНО-α (инфликсимаба, этанерцепта и адалимумаба) в лечении ГКА. Поэтому применять их не имеет смысла даже в качестве стероидосберегающих средств.
Тоцилизумаб в лечении ГКА. В настоящее время самым перспективным лекарственным средством из группы генно-инженерных биологических препаратов для лечения ГКА является тоцилизумаб (антитела к рецептору интерлейкина-6), который был зарегистрирован по этому показанию в США и Европейском Союзе. Рекомендуемая схема лечения предполагает еженедельное подкожное введение препарата в дозе 162 мг. Эффективность и безопасность тоцилизумаба у пациентов с ГКА были установлены в 12-месячном рандомизированном, плацебо-контролируемом исследовании GiACTA (Giant-Cell Arteritis Actemra), которое проводилось в разных странах Европы и США [2]. Пациентов, включенных в это исследование (n=251), рандомизировали на 4 группы (2:1:1:1). В первые двух группах больные получали тоцилизумаб подкожно в дозе 162 мг еженедельно или через неделю в сочетании с глюкокортикостероидами, которые постепенно отменяли в течение 26 недель. Пациенты двух других групп получали плацебо подкожно в сочетании с глюкокортикостероидами, которые также отменяли в течение 26 или 52 недель. Примерно у половины пациентов имелся впервые диагностированный ГКА, а у половины – рецидив системного васкулита. Около половины пациентов принимали глюкокортикостероиды в дозе ≥30 мг/сут, а остальные – в более низкой дозе.Через 52 недели стойкая ремиссия ГКА была отмечена у 53-56% больных групп тоцилизумаба и только 14-18% групп плацебо (p 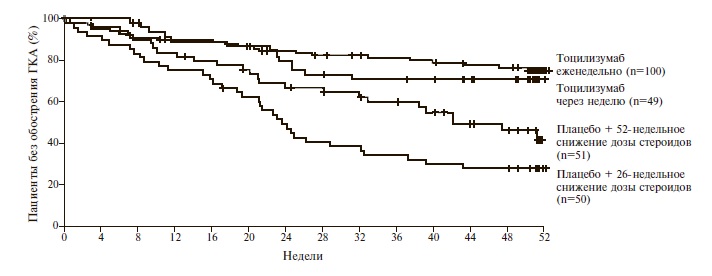
Тоцилизумаб фактически стал первым иммуносупрессивным препаратом, эффективность которого (включая выраженное стероидосберегающее действие) в профилактике рецидивов ГКА была столь убедительно доказана в рандомизированном плацебо-контролируемом исследовании. При применении тоцилизумаба следует соблюдать осторожность и учитывать риск развития нежелательных явлений. Несомненный интерес представляют отдаленные результаты лечения тоцилизумабом, которые в настоящее изучаются в рамках 2-летнего наблюдения пациентов, включенных в исследование GiACTA.
Заключение
Диагноз ГКА, развивающегося у людей пожилого и старческого возраста, нередко устанавливают с опозданием, что может привести к тяжелым последствиям, в частности потере зрения. В связи с этим французские рекомендации по диагностике и лечению этого заболевания имеют важное значение для врачей различных специальностей, в том числе ревматологов, терапевтов, офтальмологов и неврологов. Следует отметить, что подходы к диагностике и лечению ГКА постепенно меняются. Сегодня многие эксперты признают возможность использования ультразвукового сканирования и других неинвазивных визуализирующих методов как альтернативы биопсии височной артерии, которая в нашей стране проводится значительно реже, чем в зарубежных клиниках. Например, в исследовании GiACTA признаки васкулита крупной артерии, выявленные при ангиографии, КТ- или МР-ангиографии или ПЭТ/КТ, служили самостоятельным критерием диагноза ГКА (т.е. в этом случае не требовалось его подтверждение при гистологическом исследовании). Возможный алгоритм диагностики ГКА, разработанный на основе исследования GiACTA и мнения авторов данной статьи, приведен на рис. 2. Основой лечения ГКА остаются глюкокортикостероиды, однако с учетом результатов исследования GiACTA можно ожидать расширения показаний к назначению тоцилизумаба пациентам с этим системным васкулитом (тяжелое или рецидивирующее течение, серьезные осложения, например, потеря зрения, сохранение активности несмотря на лечение глюкокортикостероидами, осложнения глюкокортикостероидной терапии, требующие применения стероидосберегающих препаратов).