Что лучше левомицетин или метронидазол при диарее
Первая помощь при острой диарее
До вызова «скорой» или в первые сутки заболевания необходимо:
Если причина поноса – отравление, необходимо промыть желудок: выпить 0,5 л воды, можно чуть подсоленной или с содой, вызвать рвоту.
Принять средства для восполнения объема жидкости (3 л в сутки для взрослых).
Регидрон: выпить 0,5 л теплой воды, можно чуть подсоленной, вызвать рвоту;
Пить часто и маленькими глотками.
Принять энтеросорбенты (вбирают и выводят токсины):
Средства от рвоты и диареи (если большая часть токсина уже вышла с рвотой и калом):
противорвотные средства: Мотилиум, Церукал;
против поноса: Лоперамид, Имодиум, Тримедат.
Нельзя применять при подозрении на инфекционную диарею, язвенный колит, колит после приема антибиотиков, внутреннее кровотечение, детям до 6 лет!
Средства от вздутия и диареи:
При подозрении на кровотечение уложить больного, на живот поместить холод, вызвать «скорую».
Лечение диареи у взрослых
Общее в лечении всех видов диареи заключается в приеме препаратов, улучающих состояние тонкого кишечника:
энтеросорбентов: Смекта, Активированный уголь и др.;
вяжущих средств: Де-нол;
пробиотиков: Бификол, Линекс, Пробифор;
обволакивающих средств: Алмагель, Фосфалюгель.
Выбор дополнительных средств от поноса зависит от причины, его вызвавшей.
Этиотропное лечение экссудативной диареи
Для лечения бактериальной кишечной инфекции показаны противомикробные препараты:
При амебной дизентерии:
Лечение болезни Крона, язвенного колита: глюкокортикостероиды, иммуносупрессоры, препараты 5-аминосалициловой кислоты.
Этиотропное лечение секреторной диареи
При воспалении кишечника и холере для снижения гиперсекреции воды и солей назначается Гидрасек.
При хологенной (печеночной) диарее:
желчегонные средства: Гепабене;
связывающие желчные кислоты: Холестирамин;
спазмолитики;
сорбенты: Энтеросгель, Неосмектин;
гепатопротекторы: Фосфоглив, Эссенциале.
Для лечения нейроэндокринных опухолей – Сандостатин.
Этиотропное лечение осмотической диареи
Элиминационная диета – исключение пищевых аллергенов, непереносимых продуктов.
Ферментные препараты – восполняют недостаток ферментов при хронических заболеваниях пищеварительной системы:
Для лечения лямблиоза:
Для лечения ротавирусной инфекции: энтеросорбенты, ферментные препараты, средства для восполнения жидкости, пробиотики. Антибиотики неэффективны.
Этиотропное лечение моторной диареи
Психотропные препараты применяются для устранения психогенного фактора в возникновении синдрома раздраженного кишечника.
Средства от диареи в дорогу
Расстройства стула столь часто возникают у путешествующих, что получили официальное название «диареи путешественников».
Вызвать диарею могут инфекционные возбудители (кишечная палочка), попадающие внутрь через немытые руки, пищу, питьевую воду, купание в бассейне, мясные блюда, постельное белье.
Рекомендуется взять с собой аптечку путешественника, в которую входят:
Применяются при хорошем самочувствии и жидком стуле до 2-х раз в сутки. Если чаще, добавить прокинетики.
Прокинетики: Лоперамид, Имодиум.
При лихорадке, кровавом поносе Лоперамид не применять!
Если понос держится более 2 суток, добавить антимикробные препараты.
Средства от обезвоживания: Регидрон и аналоги.
Ферментные препараты (при переедании, непривычной пище).
Диета при диарее у взрослого
При острой диарее рекомендуется отварной рис, овсяная каша, белые сухарики, бананы, картофельное пюре, зеленый чай, печеные яблоки. Эти продукты помогают закрепить понос.
При непереносимости продуктов (целиакия, лактазная недостаточность) – исключение их из рациона.
При вздутии живота нельзя потреблять продукты, усиливающие брожение: бобовые, жирные сорта мяса, свежая выпечка, сладости, сырые овощи и фрукты.
Во всех случаях исключается жирная, жареная, острая, чрезмерно соленая пища.
КИШЕЧНЫЙ ДИСБАКТЕРИОЗ
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Нормальная микробная флора кишечника
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
Клинические особенности дисбактериоза
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Основным симптомом псевдомембранозного колита является обильная водянистая диарея, началу которой предшествовало назначение антибиотиков. Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
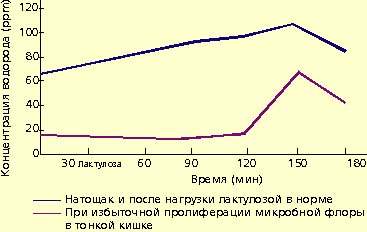 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
 |
Лечение
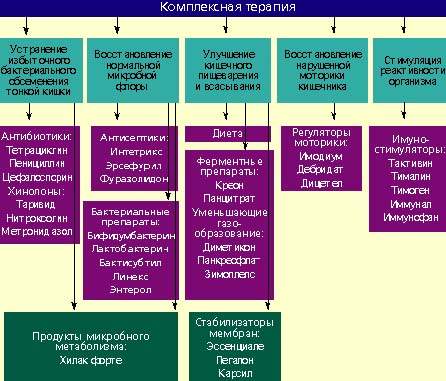
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Антибактериальная терапия инфекционных диарей у детей
Рассмотрены подходы к терапии острых кишечных инфекциях у детей. Широкий спектр антибактериального действия, практически полное отсутствие влияния на нормальную микрофлору, высокую безопасность, позволяет рекомендовать кишечный антисептик нифуроксазид для
Инфекционные диареи в настоящее время занимают второе место в структуре инфекционной заболеваемости детей, уступая только острым респираторным инфекциям. Уровень заболеваемости острыми кишечными инфекциями (ОКИ) у детей в 2,5–3 раза выше, чем у взрослых, при этом более половины регистрируемых случаев инфекционных диарей приходится на долю детей раннего возраста. По данным Всемирной Организации Здравоохранения (ВОЗ) (2008), в мире ежегодно регистрируется до 2 млрд диарейных заболеваний и около 5 млн детей ежегодно умирают от кишечных инфекций и их осложнений. В Европе ежегодно регистрируется от 0,5 до 1,9 эпизодов инфекционных диарей у каждого ребенка младше 3 лет [1]. У детей инфекционная диарея по-прежнему является одной из основных причин смертности, причем не только в развивающихся странах [2, 3].
В настоящее время в России отсутствуют согласованные подходы к терапии ОКИ у детей, причем частота назначения антимикробных препаратов остается на высоком уровне, особенно у госпитализированных пациентов [4]. По этой причине представляется актуальным освещение вопросов антимикробной терапии ОКИ на современном этапе. Прежде чем начать терапию ОКИ, необходимо установить патогенетический тип диареи (инвазивный, секреторный, осмотический или смешанный), определить синдром поражения желудочно-кишечного тракта (ЖКТ) (гастрит, гастроэнтерит, энтерит, гастроэнтероколит, энтероколит, колит, дистальный колит), кроме этого, необходимо диагностировать развившиеся осложнения ОКИ (синдром дегидратации, инфекционно-токсический шок, гемолитико-уремический синдром и т. д.) и оценить преморбидный фон пациента (есть ли у больного пищевая аллергия, синдром мальабсорбции, иммунодефицитное состояние и т. д.) [5].
Основные принципы терапии ОКИ у детей предполагают целенаправленное воздействие, в первую очередь, на макроорганизм, обуславливающее коррекцию возникших водно-электролитных расстройств, а также и элиминацию возбудителя. При остром гастроэнтерите ВОЗ считает абсолютно доказанной эффективность двух терапевтических мероприятий: регидратации и диетотерапии (2006). При этом не следует забывать, что более 70% всех инфекционных диарей у детей вызываются вирусными агентами [3, 6, 7], а при вирусных инфекциях антибактериальная терапия не только не показана, но и наносит значительный вред макроорганизму [8, 9].
Наиболее дискутабельным остается вопрос о целесообразности использования антимикробных средств в лечении бактериальных ОКИ у детей. Назначая антибиотик в этих случаях, врач ожидает: уменьшения выраженности клинических симптомов; сокращения продолжительности заболевания; снижения частоты развития осложнений; прекращения выделения возбудителя; предупреждения дальнейшего распространения инфекции [10].
В то же время доказано, что использование антибиотиков при бактериальной диарее далеко не всегда эффективно и безопасно. При энтерогеморрагическом эшерихиозе, вызванном как E. coli О157: Н7, так и E. coli O104: H4, применение антибиотиков приводит к массивному высвобождению шигаподобного токсина, следовательно, увеличивает риск развития гемолитико-уремического синдрома (ГУС). При этом включение в терапию фторхинолонов и триметоприм/сульфаметоксазола сопровождалось высоким риском развития ГУС, а наиболее безопасным и эффективным оказалось использование карбапенемов, макролидов и рифаксимина [11].
Назначение антимикробных препаратов при бактериальных диареях в значительном проценте случаев не только не приводит к санации макроорганизма от возбудителя, но и, наоборот, способствует продолжительной персистенции бактериального агента в ЖКТ, вследствие не только подавляющего влияния на нормальную микрофлору кишечника, но и прямого иммуносупрессивного действия [12, 13]. По данным отечественных и зарубежных исследователей, затяжное реконвалесцентное бактериовыделение сальмонелл формируется у значительного числа пациентов, получавших антибиотики в острую фазу инфекции, по сравнению с лицами, получавшими исключительно патогенетическую терапию [14, 15]. По нашим собственным данным, бактериовыделение сальмонелл в периоде реконвалесценции отмечено в среднем у 37% детей, лечившихся системными антимикробными средствами. Влияние антимикробной терапии на иммунный ответ было показано авторами при шигеллезе, причем комбинированная антибактериальная терапия приводила к выраженной супрессии как гуморального иммунного ответа, так и показателей фагоцитоза [16].
Самым серьезным недостатком широкого использования антибактериальных препаратов при лечении инфекционных диарей является быстрое развитие у представителей семейства Enterobacteriaceae резистентности к антимикробным препаратам [17]. Так, отечественными авторами зафиксирован неуклонный рост числа штаммов Salmonella enteritidis, устойчивых к большинству стартовых антимикробных препаратов. Например, к налидиксовой кислоте в настоящее время резистентно до 60% циркулирующих штаммов сальмонелл [14]. Все чаще выявляются штаммы кампилобактерий, обладающие широкой антибиотикорезистентностью, в том числе к макролидам и фторхинолонам [14, 18]. Параллельно с ростом антибиотикорезистентности отмечено снижение клинической эффективности стартовой антибактериальной терапии при назначении налидиксовой кислоты, она уменьшилась к 2009 г. по сравнению с 2000–2005 гг. с 61% до 48,3%, а при использовании амикацина — с 53,9% до 31,7% [14, 15].
Кроме того, применение противомикробных препаратов нередко обуславливает развитие аллергических реакций, вплоть до анафилактического шока, а также назначение антибиотиков может привести к развитию не только идиопатической антибиотикоассоциированой диареи, но и тяжелых антибиотикоассоциированных колитов, обусловленных токсинообразующими штаммами Clostridium difficile [6, 10].
Проведенные в России немногочисленные фармакоэпидемиологические исследования показали, что у детей, болеющих ОКИ, в большинстве случаев в стационаре используется антибактериальная терапия (72–100% госпитализированных), причем минимум у трети больных отсутствуют какие-либо показания к ее назначению, при этом во многих стационарах используются малоэффективные или токсичные препараты (хлорамфеникол, естественные пенициллины, рифампицин) [4, 19, 20].
В практическом здравоохранении отмечаются не только ошибки в выборе антимикробного препарата для лечения инфекционных диарей, но и часто встречаются как недостаточные, так и избыточные дозы назначаемых препаратов, неадекватный способ введения, неправильный выбор интервалов между введениями, необоснованное сочетание двух и более антибактериальных средств [13]. Если доза антибиотика недостаточна и не обеспечивает в крови и тканях концентрации, превышающие минимально подавляющие концентрации основных возбудителей инфекции, то это не только становится одной из причин неэффективности лечения, но и создает предпосылки для формирования антибиотикорезистентности микроорганизмов. В современной ситуации, при наличии высокоэффективных антимикробных препаратов широкого спектра действия для лечения ОКИ, показания к комбинированной антибактериальной терапии практически отсутствуют и приоритет в лечении остается за монотерапией [6, 18, 21].
Кроме этого, до настоящего времени при инфекционных диареях проводится необоснованно длительная антибактериальная терапия со сменой 3–4 лекарственных средств, реже имеет место неоправданно короткая антимикробная терапия [4].
В силу вышесказанного в настоящее время показания к использованию антибиотиков в лечении ОКИ являются строго ограниченными и определяются типом диареи и этиологией заболевания, формой тяжести инфекционного заболевания, возрастом и состоянием преморбидного фона пациента [6, 9, 21].
Антимикробный препарат, предназначенный для лечения инфекционных диарей у детей, должен отвечать следующим критериям: иметь высокую активность в отношении основных циркулирующих возбудителей бактериальных ОКИ; обладать бактерицидным действием; иметь высокую биодоступность действующего вещества и создавать высокую концентрацию в ЖКТ. Необходимо, чтобы уровень штаммов, имеющих резистентность к препарату, был низким. Немаловажную роль в педиатрии играют профиль безопасности (количество и характер токсических эффектов), фармакоэкономические характеристики (соотношение эффективности, безопасности и стоимости) препарата, удобная для детей форма выпуска (суспензия) и режим дозирования лекарственного средства [1, 5–7].
Ю. Б. Белоусовым и С. М. Шатуновым (2001) было предложено разделить антимикробные препараты для лечения кишечных инфекций на две группы. Первая — препараты, которые после перорального приема не абсорбируются (т. е. имеют низкую биодоступность) и обеспечивают антимикробный эффект только в кишечнике, не оказывая системного действия (так называемые кишечные антисептики — нитрофураны, нефторированные хинолоны и хинолины, некоторые сульфаниламиды и др.); вторая — антибиотики, хорошо всасывающиеся в тонкой кишке, которые оказывают системное действие, но одновременно обеспечивают низкие терапевтические концентрации в стенке кишечника (фторхинолоны, хлорамфеникол, тетрациклины, макролиды, нитроимидазолы и др.) [22].
Высокие концентрации препаратов первой группы в пищеварительном тракте являются важной характеристикой для лечения инфекционных диарей, но в случае генерализации инфекции эти антимикробные средства оказываются неэффективными, так как не обеспечивают терапевтических концентраций в крови и паренхиматозных органах [22–24]. В последние годы при лечении бактериальных ОКИ широко применяются невсасывающиеся антимикробные препараты. Их преимуществами по сравнению с системными антибиотиками являются: возможность непосредственного воздействия на бактериальный агент при низком риске развития резистентности штаммов; практически полное отсутствие негативного влияния на нормальную микрофлору; незначительная частота развития системных побочных реакций; отсутствие лекарственного взаимодействия, так как они не оказывают влияния на ферменты системы цитохрома Р450 [25–28].
В соответствии с рекомендациями ВОЗ, антимикробная терапия при инфекционных диареях показана только при следующих нозологических формах: холере, брюшном тифе, шигеллезе и амебиазе [1].
По мнению ведущих отечественных инфекционистов, показаниями к назначению антимикробной терапии у детей с острыми кишечными инфекциями являются развитие (угроза развития) генерализованных форм (тифоподобных, септических) заболеваний; тяжелые формы инвазивных диарей, а также среднетяжелые формы инвазивных ОКИ у детей групп риска. К пациентам групп риска относятся дети с тяжелыми хроническими заболеваниями (первичные иммунодефициты, злокачественные новообразования, воспалительные заболевания кишечника, корригированные оперативным путем врожденные пороки сердца, ювенильные артриты и т. д.) и дети раннего возраста (первые 6–12 месяцев жизни) [6, 7, 21]. Кроме вышеперечисленных лиц, антибактериальная терапия является обязательной для пациентов с иерсиниозами.
Принципы рациональной антибактериальной терапии ОКИ у детей предусматривают своевременное назначение препарата (период разгара болезни); разделение используемых антимикробных препаратов на стартовые, альтернативные и препараты резерва; учет антибиотикочувствительности выделенных штаммов; использование оптимального способа, дозы, кратности введения и курса терапии, а также учет индивидуальных особенностей пациента (возраста, преморбидного фона и т. д.).
Большинство зарубежных источников препаратами выбора для терапии инфекционных диарей у детей, протекающих с клиникой гемоколита, считают цефтриаксон и азитромицин, а у взрослых пациентов — фторхинолоны и азитромицин [1, 18]. Длительность назначения антимикробных препаратов не превышает 5 суток, а во многих случаях ограничивается 24–48 часами. Для терапии шигеллезов сохраняют актуальность ампициллин, налидиксовая кислота, триметоприм/сульфаметоксазол, нитрофураны [18, 29].
Стартовые препараты антибактериальной терапии ОКИ целесообразно использовать в ранние сроки заболевания при среднетяжелых формах инвазивных диарей и отсутствии индивидуальной непереносимости препаратов. Преимущество отдается препаратам с широким спектром действия, которые обладают бактерицидным или бактериостатическим действием, плохо всасываются из кишечника и не оказывают подавляющего влияния на аутохтонную микрофлору. К таким препаратам относятся производные оксихинолина, нитрофураны, аминогликозиды I–II поколения. Так как выбор антибактериального препарата в острый период инфекционной диареи осуществляется эмпирически, то при необходимости следует корригировать терапию в соответствии с антибиотикочувствительностью выделенного возбудителя [13, 22].
Эффективность антибактериальной терапии, основными критериями которой являются нормализация температуры тела, купирование или уменьшение выраженности интоксикации и диарейного синдрома, оценивается в течение 48–72 часов после начала лечения. При отсутствии положительной клинической динамики или прогрессировании симптомов заболевания, а также на поздних сроках заболевания как альтернатива стартовым антибиотикам могут использоваться иные антибиотики: защищенные аминопенициллины, нефторированные хинолоны (налидиксовая кислота), хлорамфеникол, макролиды II поколения, цефалоспорины II–III поколения, аминогликозиды II–III поколения (амикацин, нетилмицин), нитроимидазолы. При тяжелых формах ОКИ целесообразно начинать терапию с парентерального введения антимикробных препаратов, а по достижении клинического эффекта возможен переход на пероральный прием антибиотика до завершения полного курса терапии.
Антибиотики резерва используются исключительно в условиях стационара, обладают широким спектром действия и высокоэффективны в отношении практически всех возбудителей ОКИ, в том числе и устойчивых к антибактериальным препаратам стартовой и альтернативной терапии. Показаниями к назначению таких препаратов являются генерализованные и септические формы ОКИ, тяжелое течение ОКИ у детей с неблагоприятным преморбидным фоном, подозрение на нозокомиальную природу заболевания, а также неэффективность вышеназванных групп антибиотиков. К препаратам резерва относятся цефалоспорины III–IV поколения, карбапенемы, аминогликозиды II–III поколения, фторхинолоны (у детей можно использовать только по жизненным показаниям) [8, 21, 22].
При выборе этиотропной терапии необходимо учитывать не только предполагаемого возбудителя ОКИ, но и быстро формирующуюся резистентность циркулирующих энтеробактерий к традиционно применяемым антибактериальным средствам. В этой связи рекомендации по выбору оптимального антибактериального средства должны обязательно основываться на региональных данных по структуре антибиотикорезистентности.
В детской практике имеются сложности в антимикробной терапии инфекционных диарей, особенно это касается пероральных форм лекарственных средств и связано в первую очередь с возрастными ограничениями по применению препаратов в педиатрии. Так, налидиксовая кислота разрешена к применению с 2-летнего возраста (а по некоторым источникам с 18 лет); рифаксимин с 12-летнего возраста, а Интетрикс в настоящее время вообще не разрешен в педиатрии.
Следовательно, основным стартовым препаратом в детской инфектологии в последние годы является нифуроксазид. Нифуроксазид относится к нитрофурановым препаратам, антибактериальная активность которых обусловлена продукцией нитроанионов. Нитрофурановые препараты являются акцепторами ионов водорода при переносе электронов с флавиновых ферментов на цитохром, тем самым нитрофураны блокируют энергообразование в бактериальной клетке. Кроме этого, нифуроксазид блокирует активность альдолаз, дегидрогеназ, транскетолаз и синтез макробелковых комплексов. В результате этих взаимодействий нитрофуранов с бактериальными агентами нарушаются процессы роста и деления бактериальных клеток. Доказано, что нифуроксазид в среднетерапевтических дозах оказывает бактериостатический, а в высоких дозах — бактерицидный эффект [23, 24, 30].
Нифуроксазид относится к местным антисептикам и практически не всасывается в кровь из ЖКТ, не влияет на эндогенную микрофлору, практически не приводит к формированию антибиотикорезистентных штаммов [30, 31].
В России и за рубежом имеется обширный положительный опыт использования нифуроксазида при шигеллезе, сальмонеллезе, ОКИ, вызванных условно-патогенными возбудителями [15, 31, 32]. В 2013 году в РФ зарегистрирован нифуроксазид под торговым названием Стопдиар, причем у данного препарата есть две лекарственные формы — таблетки, 100 мг, покрытые пленочной оболочкой, разрешены с 6-летнего возраста и форма суспензии для пациентов с 2-месячного возраста. Данная лекарственная форма является комплексной, так как в ее составе кроме нифуроксазида (5 мл = 220 мг) содержится симетикон. Симетикон — это поверхностно-активное пеногасящее средство, уменьшающее газообразование в кишечнике. Содержание симетикона в суспензии Стопдиара особенно актуально для детей раннего возраста, которые страдают от повышенного газообразования на фоне инфекционных диарей.
Таким образом, рост и изменение лекарственной чувствительности штаммов возбудителей инвазивных диарей требует строгих подходов к назначению антимикробных препаратов при ОКИ у детей, целесообразно использовать режим ступенчатой терапии, что определяется высокой клинической эффективностью и уменьшением психотравмирующего влияния на маленького пациента. Учитывая широкий спектр антибактериального действия, практически полное отсутствие влияния на нормальную микрофлору, высокий профиль безопасности и наличие суспензионной лекарственной формы, кишечный антисептик нифуроксазид можно считать стартовым препаратом при лечении инфекционных диарей у детей.
Литература
ФГБУ НИИДИ ФМБА России, Санкт-Петербург
