Что лучше мовалис свечи или мовалис таблетки
Мовалис – юбилей в семействе НПВП. Эффективность, безопасность, перспективы применения
НПВП в современной клинической практике
Врачи различных специальностей регулярно назначают нестероидные противовоспалительные препараты (НПВП) в клинической практике. Широкий спектр действия (противовоспалительный, обезболивающий, жаропонижающий эффект) и внушительный список показаний для применения (простудные заболевания, заболевания, сопровождающиеся воспалением, болью, и др.) обеспечивают НПВП популярность и среди врачей, и среди пациентов. Такая востребованность НПВП имеет как положительные, так и отрицательные последствия.
С одной стороны, значение НПВП сложно переоценить. Количество клинических исследований эффективности и безопасности тех или иных НПВП огромно. Доход от реализации НПВП сопоставим с бюджетами некоторых стран.
С другой стороны, эти препараты лидируют и по неадекватному применению. Каждый из практикующих врачей имеет свои предпочтения среди НПВП, свой взгляд на их эффективность и безопасность, а также на длительность их приема. Однако мнение врача не всегда соответствует истине и формируется под влиянием публикаций в научной прессе или работы медицинских представителей. Допускаются ошибки при определении дозы, длительности приема, выборе лекарственной формы, назначении НПВП в комбинации с другими лекарственными средствами. Это снижает эффективность лечения и повышает риск развития разнообразных нежелательных явлений.
Отдельно следует обозначить проблему бесконтрольного приема НПВП пациентами, в том числе применение НПВП в детском возрасте без рекомендации врача. Во многом это обусловлено навязчивой рекламой безрецептурных НПВП в средствах массовой информации, которая толкает пациентов к так называемому ответственному самолечению. Кроме того, рецептурные НПВП на практике назначаются врачами в виде устных рекомендаций и отпускаются в аптеке без рецептов. Отметим, что НПВП подразделяются на безрецептурные и рецептурные формально, не по механизму действия, а в зависимости от дозировок, форм выпуска, потенциальной простоты и кратности приема.
НПВП: мифы и реальность
История применения противовоспалительных средств в терапии боли насчитывает несколько тысячелетий, уходя корнями в Древний Египет и времена Гиппократа. Противовоспалительные средства прошли путь от листьев и коры ивы, экстракта коры ивы до хинина, салицина и уже более современных препаратов, таких как феназон (антипирин), аминофеназон (пирамидон, амидопирин), аспирин.
В XX в. разработка новых противовоспалительных препаратов и их лекарственных форм резко ускорилась. Накапливался опыт применения НПВП, оценивалась не только эффективность препаратов, но и частота возникновения побочных реакций, степень выраженности которых останавливала то или иное направление развития НПВП. Уже тогда в связи с востребованностью эффективных лекарственных средств стали появляться подделки, произведенные кустарным способом с нарушением технологии производства, малым количеством действующего вещества и большой долей балластных веществ, что усложняло контроль нежелательных явлений, сопутствующих приему оригинальных препаратов [1].
По мере того как накапливались научные знания и практический опыт применения НПВП, рос и «снежный ком» неадекватных и неправильных представлений о действии, побочных явлениях и формах введения препаратов. Подобное искаженное восприятие – отчасти следствие личного опыта врачей и влияния пациентов и врачей друг на друга, отчасти итог образовательных лекций и мероприятий. Слушатели часто воспринимают информацию о различных побочных реакциях и возможных осложнениях не как результат механизма действия конкретного лекарственного средства, а в целом, для всей группы НПВП.
К сожалению, представления врачей о статистической вероятности развития осложнений не соответствуют частотным характеристикам. Среди врачей и пациентов распространены мифы о том, что скорость развития эффекта и выраженность побочных явлений связаны с путем введения препарата. Так, в представлениях врачей инъекционным формам введения соответствует «более быстрое развитие эффекта» и, как следствие, незначительная выраженность побочных явлений. Сторонники инъекционных форм зачастую забывают о потенциальных рисках любых инъекций, а также о стоимости лечения подобных осложнений. Распространен еще один миф – таблетированные пероральные формы «действуют медленнее» и «хуже влияют на желудок». Таких недостатков, по мнению многих, лишены ректальные формы, что, конечно, не соответствует действительности.
Таким образом, каждый метод введения препарата имеет помимо физиологических характеристик еще и психологический аспект, во многом зависящий от изначальных убеждений пациентов и врачей. Это частично связано с плацебо-эффектом или схожим действием, усиливающим эффект реального препарата. Пациенты, не воспринимая разумные доводы, остаются верны своему мнению и с большей долей вероятности поменяют врача, чем убеждения. В некоторой степени подобная «ригидность» пациентов объясняется крайней неоднородностью мнения врачей по данному вопросу, что, естественно, смущает больных [2].
Осенью 2015 г. на нашем сайте отделениеболи.рф (paindept.ru) проводился опрос, в котором участвовали как врачи, так и пациенты (n = 177). На вопрос: «Что действует на вас лучше и быстрее?» были получены следующие ответы:
Надо сказать, что среди респондентов доминировали врачи. Вопрос был сознательно сформулирован некорректно, были указаны только формы введения без упоминания конкретных лекарственных средств. Подавляющее большинство ошибочно посчитало, что эффективность лечения зависит от формы введения, а не от действующего вещества.
Мовалис: эффективность, безопасность, фармакокинетические характеристики
Значимым этапом в изменении представлений о безопасности применения НПВП стало появление селективных ингибиторов циклооксигеназы (ЦОГ) 2. Первым представителем селективных, позже названных умеренно селективными, ингибиторов ЦОГ-2 стал оригинальный препарат мелоксикам, известный в нашей стране как Мовалис, а за рубежом – под названием Mobic, компании Boehringer Ingelheim.
Наиболее крупными исследованиями эффективности мелоксикама были MELISSA (Meloхicam Large Scale International Study Safety Assessment) и SELECT (Safety and Efficacy Large scale Evaluation of COХ inhibiting Therapies) [3–5]. В этих двух испытаниях приняли участие почти 20 тысяч больных остеоартрозом (9323 и 8656 пациентов соответственно). Мелоксикам (7,5 мг/сут) по клинической эффективности был эквивалентен диклофенаку (100 мг/сут) и пироксикаму (20 мг/сут) [4, 5]. Отмена препаратов в связи с низкой эффективностью в группах диклофенака, пироксикама и мелоксикама не превышала 1,7% [6].
В настоящее время в Российской Федерации доступны таблетированная форма Мовалиса с возможным режимом дозирования 7,5 и 15 мг, суспензия с определением дозы мерными ложками (7,5 мг в 1 мл), изначально позиционировавшаяся как форма для детей и молодых пациентов с ревматическими болезнями. Кроме того, имеются инъекционные формы для внутримышечного введения № 3, № 5 и форма для госпитальных закупок № 50. За пределами России существует также форма для внутривенного введения.
Биодоступность таблетированной формы Мовалиса приближается к 100% и практически достигает значений инъекционной формы. Максимальная концентрация в плазме при парентеральном введении достигается через 60 минут, при однократном пероральном введении препарата – через пять-шесть часов. Стабилизация фармакокинетических показателей происходит на третий – пятый день приема препарата. Во внутрисуставные ткани Мовалис проникает в 50%-ной концентрации от концентрации в плазме крови. Почему так важно знать фармакокинетические характеристики препарата? Дело в том, что в клинической практике врачи нередко назначают НПВП без учета фармакокинетических особенностей, вследствие чего препараты не могут продемонстрировать оптимальный эффект. В результате неадекватного применения пациенты утрачивают веру в лечение, падает авторитет и препарата, и врача, и лечебного учреждения.
Например, врач, определяя продолжительность лечения Мовалисом, может руководствоваться количеством ампул для инъекций № 3 и назначить препарат на сверхкороткий срок – всего на три дня. В действительности же не следует ограничивать лечение трехдневным курсом инъекций, парентеральное введение должно быть начальным этапом ступенчатой терапии с переходом на прием препарата перорально. Учитывая недостаточную мотивацию врачей к повышению уровня знаний и не всегда правильное понимание патофизиологии воспаления и боли, не исключено, что общие (класс-специфические) побочные явления воспринимаются без учета степени ингибирования ЦОГ. Видимо, врачи, рекомендующие короткий курс лечения, опасаются ульцерогенного действия, свойственного неселективным ингибиторам ЦОГ. Этим же объясняется и нередкое назначение НПВП под прикрытием препаратов из группы ингибиторов протонной помпы. Таким образом, врачи не принимают во внимание данные по профилю безопасности препарата и не знают, что Мовалис можно назначать на длительный срок. Между тем в описанных исследованиях MELISSA и SELECT сроки лечения Мовалисом составляли от нескольких недель до нескольких месяцев и соответствовали показателям безопасности.
Преимущества оригинальных препаратов
С учетом ценовой категории Мовалиса и активно проводимой Минздравом России политики взаимозаменяемости лекарственных средств, исходя только из международного непатентованного наименования, актуальным становится вопрос выбора между оригинальным препаратом и дженериком. Однако далеко не все врачи и тем более пациенты понимают, в чем заключается разница между оригинальными и дженерическими препаратами, помимо цены. Почему многие врачи, призывая с особым вниманием относиться к выбору препарата, настаивают на использовании оригинального средства? Обеспечит ли оригинальный препарат 100%-ный эффект? Этого никто обещать не может. Разберемся, может ли дать какие-либо гарантии препарат-дженерик.
В состав лекарственного препарата кроме основного действующего вещества – так называемого международного непатентованного наименования входят еще и балластные вещества. Значительную роль играет также технология производства, соблюдение которой обеспечивает ряд показателей, не всегда становящихся достоянием общественности.
В США и странах Европы в отличие от России при введении в клиническую практику дженериков учитывается такой параметр, как клиническая эквивалентность – результат длительного сравнения эффективности дженерического препарата и оригинала. В нашей стране обязательным является лишь наличие биоэквивалентности. Однако и эти данные не всегда предоставляются конечным пользователям – врачам, выбирающим наиболее доступное и эффективное средство для своих пациентов.
Качество препарата-оригинала и препарата-дженерика также может различаться. Сегодня в средствах массовой информации высказывается множество мнений о сертификации отечественных фармацевтических производителей по стандартам GMP (надлежащей производственной практики). В то же время на нашем рынке представлены многие лекарственные средства-дженерики не только из России, но и из Юго-Восточной Азии. Неизвестно, соблюдается ли в этих странах технология производства таких препаратов, какие применяются балластные вещества, как это влияет на фармакокинетические и фармакодинамические показатели.
Производители дженерических препаратов часто не проводят собственные клинические исследования, ссылаясь на доступные данные, полученные на оригинальных препаратах. Экономия затрат на проведение клинических исследований, построение дизайна, соответствующего критериям доказательной медицины, оплату самого исследования, конечно, позволяет снизить цену на итоговый продукт. Результаты ряда исследований, в которых сопоставляется эффективность, а также фармакокинетические и фармакодинамические показатели оригинальных препаратов и препаратов-дженериков, доступны в научной прессе. Например, сопоставление оригинального диклофенака и диклофенака-дженерика показало значимые отличия в фармакокинетических показателях, в том числе низкую биодоступность дженерика, что, безусловно, ставит под сомнение наличие терапевтической эквивалентности [7].
Перспективы применения Мовалиса
В течение двадцати лет активного применения в России Мовалис ассоциировался с выбором безопасной терапии хронической боли. Для терапии острой боли по умолчанию подразумевалось использование неселективных ингибиторов ЦОГ, несмотря на то что они вызывают известные побочные реакции. Понятие выбора не только эффективного, но и безопасного препарата при острой боли в данном контексте не рассматривалось. Подобный компромисс «эффективное обезболивание с сопутствующими нежелательными явлениями» – стандартная ситуация для нашей страны, поскольку в России отсутствует как таковой расчет стоимости рисков лечения побочных эффектов. Между тем выбор обезболивающего препарата при оперативном вмешательстве или НПВП при острой боли также должен осуществляться с учетом соотношения фармакологических характеристик (фармакодинамики и фармакокинетики), риска развития побочных явлений и фармакоэкономических показателей.
В этой связи большой интерес представляют публикации о новой нише, которую может занять Мовалис, – об использовании препарата в премедикации и при острой боли, а именно в периоперационном обезболивании при манипуляциях в челюстно-лицевой области.
T. Aoki и соавт. на 114 пациентах продемонстрировали преимущество премедикации Мовалисом (Mobic) в дозе 10 мг по сравнению с пироксикамом 27 мг и плацебо [8]. M.A. Isidoria-Espinoza и соавт. на 50 пациентах показали более эффективное обезболивание Мовалисом в дозе 15 мг по сравнению с трамадолом 50 мг (препараты вводились за 50 минут до манипуляции при удалении зуба мудрости) [9]. E. Selimović и соавт. на 60 пациентах сравнивали эффективность мелоксикама в дозе 15 мг, глюкокортикоидов (метилпреднизолона) и их сочетания при удалении зуба мудрости, преимущество имела комбинированная терапия [10]. По результатам E.W. Weber и соавт., использование Мовалиса 15 мг в отличие от неселективных НПВП при оперативном вмешательстве не дает существенного увеличения кровопотери [11].
Эти данные позволяют по-новому взглянуть на давно знакомый пациентам и практикующим врачам препарат Мовалис. Возможно, для лучшего понимания эффективности и безопасности Мовалиса потребуется проведение дополнительных исследований на более крупной популяции пациентов со сравнением с другими препаратами, применяемыми в премедикации и лечении острой боли. Однако даже имеющиеся данные уже сейчас позволяют смело использовать Мовалис в хирургической и стоматологической практике.
Оценка эффективности Мовалиса (ректальные свечи) при болевом синдроме в малом тазу у женщин в амбулаторной гинекологической практике
Опубликовано в журнале:
«Российский вестник акушера-гинеколога», 2009, №3, с. 78-82
Evaluation of the efficacy of movalis (as rectal suppositories) in women with small pelvic pain syndrome in outpatient gynecological practice
E.S. AKARACHKOVA, I.A. ZAKHAROVA
Эффективность и безопасность применения селективного нестероидного противовоспалительного препарата (НПВП) — мовалиса в форме ректальных свечей были исследованы у 50 амбулаторных гинекологических больных от 20 до 52 лет с болевым синдромом в малом тазу (11 больных после хирургического вмешательства на органах малого таза, 24 — с двусторонним сальпингоофоритом, 8 — с овуляторным синдромом, 7 — с дисменореей). Все пациентки, помимо мовалиса, получали стандартную комплексную терапию, зависящую от вида патологии. Установлено, что включение в комплексную терапию гинекологических больных с болевым синдромом мовалиса в форме ректальных свечей в качестве НПВП позволяет уменьшить интенсивность боли в первые 2—3 дня лечения с последующим полным ее купированием при хорошей переносимости и отсутствии побочных эффектов у пациенток.
Ключевые слова: амбулаторные гинекологические больные, болевой синдром в малом тазу, нестероидные противовоспалительные препараты, мовалис.
The efficacy and safety of the selective nonsteroidal anti-inflammatory drug (NSAID) movalis as rectal suppositories were studied in 50 gynecological outpatients aged 20 to 52 years who had small pelvic pain syndrome (11 patients after surgical intervention into the small pelvis; 24 patients with bilateral salpingo-oophoritis, 8 with ovulatory syndrome, and 7 with dysmenorrhea). All the patients received, in addition to movalis, the standard complex therapy depending on the type of pathology. Inclusion of movalis as rectal suppositories as a NSAID into the complex therapy in patients with pain syndrome was ascertained to diminish the intensity of pain in the first 2—3 days of treatment with its further complete relief, with the agent being well tolerated and causing no adverse reactions in the patients.
Key words: gynecological outpatients, small pelvic pain syndrome, nonsteroidal anti-inflammatory drugs, movalis.
Боль является наиболее частой жалобой пациентов, обращающихся к врачам различных специальностей. Большую часть гинекологического амбулаторного приема составляют пациентки с жалобами на боли в животе различной интенсивности, как правило, сильные (более 5—6 баллов по визуальной аналоговой шкале — ВАШ) острые боли, впервые возникшие или являющиеся результатом обострения хронического заболевания органов малого таза. Важно, что практически все подобные боли возникают в результате раздражения болевых рецепторов (ноцицепторов). Среди причин, вызывающих подобные ноцицептивные боли, можно отметить послеоперационные состояния, воспалительные процессы придатков, болезненные менструации (дисменореи), а также овуляторный синдром. Поэтому нестероидные противовоспалительные препараты (НПВП) оказываются эффективными и широко применяются в комплексном лечении этих пациенток. Применение их способствует снижению проницаемости капилляров и, соответственно, улучшению микроциркуляции, а также угнетению миграции лейкоцитов в пораженные участки тканей, повышению стабильности лизосомальных клеточных мембран. Поэтому НПВП, наряду с анальгетическим эффектом, оказывают довольно широкий спектр воздействий, среди которых выраженное противовоспалительное, антиагрегантное, капилляро-протекторное и, в связи с этим, в определенной степени, и гемостатическое действие [3]. Пациенток с хроническими длительными разлитыми болями в малом тазу после тщательного гинекологического и урологического обследования и исключения гинекологических и урологических заболеваний наблюдают в основном врачи-неврологи, а нередко и психиатры. И часто диагноз хронической боли в малом тазу при отсутствии или минимальной выраженности соматической патологии (т.е. имеющиеся соматические изменения не могут объяснить клинических проявлений боли) является диагнозом исключения. В комплексной терапии подобных пациенток с хроническими тазовыми болями применяют антидепрессанты: трициклические и селективные ингибиторы обратного захвата серотонина и норадреналина. Последние являются приоритетными, так как обладают высокой эффективностью в купировании болевого и дисфорического компонентов боли, а также лучше переносятся больными (лишены многих побочных эффектов трициклических антидепрессантов) [2, 7].
В настоящее время врачу предоставлен значительный арсенал НПВП. Особое внимание заслуживают препараты, обладающие мощным фармакологическим профилем, удачно сочетающие в себе эффективность и безопасность, а также имеющие различные формы выпуска. Это существенно расширяет терапевтические возможности врача, позволяет подобрать адекватное лечение с оптимальным соотношением пользы и риска и максимально его индивидуализировать.
Наиболее важный механизм, определяющий как эффективность, так и токсичность НПВП, связан с подавлением активности циклооксигеназы (ЦОГ) — фермента, регулирующего биотрансформацию арахидоновой кислоты в простагландины (ПГ), простациклин и тромбоксан. Наряду с медиаторной ролью ПГ могут быть модуляторами воспаления, угнетая агрегацию тромбоцитов и таким образом способствуя высвобождению из них через систему циклических нуклеотидов гистамина и серотонина [6]. Согласно принятой современной концепции фермент ЦОГ в разных тканях представлен разными изоформами (ЦОГ-1, ЦОГ-2, ЦОГ-3). ЦОГ-1 — фермент, выполняющий в организме важные физиологические функции. Провоспалительная активность присуща ЦОГ-2, а противовоспалительные свойства — ЦОГ-3. ЦОГ-3 тоже участвует в синтезе простагландинов и играет роль в развитии боли и лихорадки. Однако в отличие от ЦОГ-1 и ЦОГ-2, ЦОГ-3 не принимает участия в развитии воспаления. Поэтому ингибиция ЦОГ-2 рассматривается как один из ведущих механизмов противовоспалительной активности НПВП, а ЦОГ-1 — развития побочных эффектов (поражение желудочно-кишечного тракта, нарушение агрегации тромбоцитов, функции почек, негативное влияние на систему кровообращения и др.). Наиболее широко распространенные НПВС («традиционные», «стандартные») — диклофенак, индометацин, фенилбутазон, ибупрофен, напроксен и другие — в одинаковой степени подавляют активность обеих изоформ ЦОГ, т.е. не обладают селективностью. Открытие двух изоферментов ЦОГ и последующее внедрение в практику селективных ингибиторов ЦОГ-2 открыло новые перспективы в плане высокой безопасности лечения НПВП [1, 4—6].
Мовалис (мелоксикам) относится к группе селективных НПВП с преимущественным угнетением ЦОГ-2. Выпускается препарат в трех формах — таблетки, ампулы, ректальные суппозитории. Для достижения клинического эффекта рекомендуется однократное введение любой из форм препарата. Благодаря высокой эффективности и хорошей переносимости мовалис на протяжении 15 лет с успехом используется врачами терапевтами, неврологами, ревматологами, хирургами, травматологами и др.
Как уже отмечалось, в гинекологии НПВП применяются в комплексной терапии болевого синдрома различной этиологии.
Цель исследования — установление эффективности и безопасности применения мовалиса в форме свечей в комплексной терапии пациенток с болевым синдромом в малом тазу в амбулаторной гинекологической практике.
Материал и методы исследования
На протяжении марта—апреля 2008 г. было проведено амбулаторное обследование 50 пациенток в возрасте от 20 до 52 лет, обратившихся к врачам-гинекологам с жалобами на боли внизу живота.
Средний возраст больных составил 33±9 лет. Подавляющее большинство их было замужем (68%). 30% пациенток были незамужними и 2% вдов. 78% женщин являлись служащими, 10% были студентками, 10% — домохозяйками и 2% — рабочими.
Методы исследования включали:
Задачами исследования явились: определение степени выраженности боли по ВАШ, динамика боли на фоне 10-дневной терапии.
Критерии включения — наиболее частые модели болевого синдрома в амбулаторной гинекологической практике:
При этом пациентки с болями на фоне спаечного процесса, остеохондроза позвоночника и другими болями смешанного происхождения не были включены в исследование.
Дизайн работы: пациентки обследовались до 10-дневной стандартной комплексной терапии, характерной для каждой модели, в которую входил в качестве анальгетика и противовоспалительного средства мовалис 15 мг (свечи) 1 раз в день.
Результаты исследования и обсуждение
При изучении особенностей менструальной функции установлено, что у всех женщин менструации установились в среднем в 12,7±1,2 лет. Длительность менструального кровотечения варьировала от 4 до 7 дней при средней продолжительности менструального цикла — 29±3 дня. Анализ репродуктивной функции показал, что одну беременность и более имели 68% больных, из них роды в анамнезе установлены у 88% женщин, аборты — у 6%. От нежелательной беременности предохранялись 45 женщин, среди которых 71% использовали презерватив, 13% — прерванный половой акт, 10% — внутриматочную контрацепцию, 4% — оральные контрацептивы («Ярина»), 2% — спермициды (фарматекс).
Гинекологические воспалительные заболевания матки и/или ее придатков отмечались в 18 (36%) наблюдениях. Миома матки — у 9 (18%) женщин.
Соматических заболеваний, по поводу которых пациентки могли принимать медикаментозные препараты, отмечено не было.
Исходно средний уровень боли у пациенток составил 6,6±1,3 балла. Через 10 дней после начала проведения комплексной терапии боль пациенток не беспокоила.
31 женщина оценила эффект от проведенного лечения как «очень хороший», 19 женщин — «хороший». Врачи также ставили оценку проведенному лечению: «очень хорошую» оценку результата терапии они отметили у 27 женщин и «хорошую» — у 23.
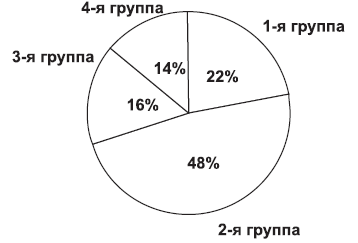
Вошедшие в исследование женщины были объединены в 4 группы в зависимости от причины болевого синдрома (см. рисунок).
Рисунок. Распределение пациенток в зависимости от причин болевого синдрома
1-ю группу составили 11 (22%) больных после хирургических вмешательств на органах малого таза (9 пациенток после надвлагалищной ампутации матки без придатков по поводу миомы матки — НАМ, 1 женщина после хирургического лечения абсцесса бартолиновой железы, 1 больная после удаления кисты яичника).
Во 2-ю группу вошли 24 (48%) пациентки с двусторонним сальпингоофоритом (18 — с обострением хронического аднексита и 6 — с впервые выявленным).
В 3-ю группу были объединены 8 (16%) женщин с овуляторным синдромом.
В 4-ю группу — 7 (14%) пациенток с дисменореей.
В дальнейшем анализ полученных результатов мы проводили внутри каждой группы, а также сравнивали эффективность терапии между группами (табл. 1).
Таблица 1. Характеристика обследованных женщин с учетом причин возникновения болевого синдрома
| Показатель | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| Средний возраст, годы | 43±6 | 32,3±7,4 | 28±6 | 25,7±8,7 |
| Длительность заболевания | 7,4±2,6 года (миома), 3 года (киста), 2 года (абсцесс) | 5±2,8 года (хронический сальпингоофорит), 8,3±4,8 дня (острый сальпингоофорит) | 6±2 мес (овуляторный синдром) | 8,9±4 года (дисменорея) |
| Длительность болевых ощущений, дни | 11±5 | 7,7±3,9 | 4±3 | — |
| Интенсивность боли внизу живота по ВАШ, баллы | 6,6±1,4 | 6,5±0,9 | 7,1±1 | 7,7±0,8 |
| Постоянные, % | 70 | 100 | 100 | 86 |
| Спонтанные, % | 30 | 14 | ||
| Интенсивность боли в пояснице по ВАШ, баллы | 3,9±1,5 | 4,1±1,8 | 5±0,8 | 5,5±1,75 |
| Число больных с болями в пояснице, %: | ||||
| — нет боли | 10 | 25 | 50 | 43 |
| — постоянные | 30 | 11 | 37 | 43 |
| — спонтанные | 60 | 64 | 13 | 14 |
| Характер боли, %: | ||||
| — ноющие | 90 | 90 | 100 | 67 |
| — стреляющие | 36 | 38 | 38 | 43 |
| — сжимающие | 27 | 48 | 63 | 57 |
| — жгучие | 55 | 21 | — | 29 |
| Иррадиация боли, %: | ||||
| — в прямую кишку | 64 | 54 | 75 | 57 |
| — анус | 36 | 25 | — | 14 |
| — промежность | 18 | 46 | 25 | 86 |
| — внутреннюю поверхность бедра | 18 | 15 | 50 | — |
| Факторы, усиливающие боль, %: | ||||
| — половой акт | — | 79 | 88 | — |
| — переохлаждение | 27 | 67 | 25 | 14 |
| — длительное сидение | 91 | 75 | 50 | 43 |
| — длительное стояние | 73 | 71 | 100 | 43 |
| — эмоциональный стресс | 27 | 13 | 25 | 71 |
| Гинекологический статус | Тело матки оперативно удалено, культя матки ограниченно подвижна, болезненна, отечна, придатки болезненны, отечны или не определяются, выделений нет | Тело матки безболезненно, плотное, чувствительно, подвижно, придатки болезненны, отечны, исходно увеличены, выделений нет | Тело матки нормальной величины, безболезненно, подвижно, придатки справа (или слева) пальпируются, увеличены, умеренно болезненны, придатки слева (или справа) безболезненны, выделений нет | Матка умер. болезненна или безболезненна, яичники без особенностей, выделений нет |
| Бактериоскопическое исследование вагинального содержимого | Лейкоциты до 25 в поле зрения | Лейкоциты от 5 до 25 в поле зрения | Лейкоциты до 10 в поле зрения | Лейкоциты до 5 в поле зрения |
| Трансвагинальная эхография | Тело матки оперативно удалено, шейка матки средних размеров, структура обычная, цервикальный канал линейный, яичники обычных размеров, жидкости в малом тазу нет | Тело матки обычных размеров, миометрий однородный, М-эхо 6—7 мм, увеличение одного или обоих яичников, контуры нечеткие, небольшое скопление жидкости в позадиматочном пространстве | Тело матки обычных размеров, миометрий однородный, М-эхо 6—7 мм, увеличение одного или обоих яичников, контуры четкие, УЗИ-признаки кисты желтого тела | Без особненностей или седловидная матка |
| Назначенная терапия | Юнидокс-солютаб, 1 табл 2 раза в день 7 дней, амоксиклав 1000 мг 2 раза, микосист 1 табл 150 мг, вобэнзим 2 капс 3 раза в день 1 мес, мовалис 15 мг (свечи) 1 раз в день, тампоны с мазью Вишневского | Юнидокс-солютаб, 1 табл 2 раза в день 7 дней, доксициклин 100 мг 1 табл. 2 раза в день 7 дней, микомакс №3 150 мг, трихопол 2 табл. 2 раза 5 дней, мовалис 15 мг (свечи) 1 раз в день, физиотерапия, магнитотерапия | Мовалис 15 мг (свечи) 1 раз в день, вит. Е 400 мг, ременс 30 кап. 2 раза в день 3 мес, дицинон 1 табл. 3 раза 5 дней | Бускопан при боли ректально, дюфастон 1 табл. 2 раза в день с 16-го по 25-й день цикла, мовалис 15 мг (свечи) 1 раз в день за 3 дня до ожидаемой менструации и до окончания выделений |
Разделение пациенток на группы позволило выявить клинические особенности болевого синдрома. Так, в 1-ю группу вошли женщины, средний возраст которых был достоверно выше, чем у женщин других групп. Пациентки 4-й группы оказались самыми молодыми. Больные различались по длительности болевых ощущений. Женщины 1-й группы — это были пациентки, испытывавшие средней интенсивности боли внизу живота и неинтенсивные боли в пояснице через 10—14 дней после хирургического вмешательства. По характеру боли были преимущественно ноющими с иррадиацией в область прямой кишки и усиливались при длительном стоянии и сидении.
Половина женщин 2-й группы не могла указать причин возникновения боли, другая половина считала, что боли возникли в результате переохлаждения. Пациентки в среднем обращались за помощью на 7—8-й день обострения заболевания. У всех них были постоянные интенсивные боли в животе ноющего и сжимающего характера с иррадиацией в прямую кишку и промежность, усиливались при половом акте, переохлаждении, длительном сидении и стоянии. Эти боли также могли сочетаться с неинтенсивными спонтанными болями в пояснице.
Женщины с овуляторным синдромом (3-я группа) в среднем обращались на 4-й день возникновения болей, однако они не могли назвать причин, которые могли их вызвать. Это были интенсивные ноющие и сжимающие боли в животе, в половине случаев сочетавшиеся с постоянными или спонтанными болями в пояснице, с иррадиацией в область прямой кишки и внутреннюю поверхность бедра и усилением при половом акте, длительном стоянии или сидении.
Пациентки с дисменореей (4-я группа) на момент обращения боли не испытывали. Молодые женщины приходили на прием в среднем на 11,9±3-й день цикла. Они жаловались на возникающие в первые три дня менструации интенсивные ноющие и сжимающие боли в животе с иррадиацией в прямую кишку и промежность, которые могли усиливаться при эмоциональном стрессе и сопровождаться умеренной болью в пояснице.
При объективном исследовании выявлялись характерные для каждой группы проявления (см. табл. 1).
Пациенткам в зависимости от группы назначалось комплексное специфическое лечение, в качестве обезболивающего и противовоспалительного препарата назначался 10-дневный курс лечения мовалисом в форме ректальных свечей. Пациенткам 4-й группы, у которых боли возникали в первые дни менструаций, мовалис в комплексной терапии назначался за 3—5 дней до менструации и во время нее.
На фоне терапии имела место положительная динамика болевого синдрома. Через 10 дней лечения боли женщин не беспокоили. В табл. 2 и 3 представлена динамика интенсивности боли у пациенток разных групп.
Таблица 2. Динамика интенсивности боли на фоне терапии у обследованных женщин в зависимости от причин возникновения болевого синдрома
| ВАШ, баллы | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| Исходно | 6,4±1,4 | 6,5±0,9 | 7±1 | 7±1,8 |
| 1-й день | 5,7±1,8 | 5,8±1,8 | 6,8±1* | 4,4±2,9 |
| 2-й день | 4,7±2,7 | 5,4±1,9↓* | 5,8±1↓* | 1,7±2,2↓ |
| 3-й день | 3,7±2,5↓* | 4,7±1,9↓* | 4,6±1↓* | 0,7±1,3↓ |
| 4-й день | 3,3±2,8↓* | 4,2±1,8↓* | 4±1↓* | 0,4±1,1↓ |
| 5-й день | 2,9±2,8↓* | 3,6±1,6↓* | 2,9±1,9↓* | 0↓ |
| 6-й день | 2±2,4↓* | 2,9±1,4↓* | 1,8±1,7↓* | 0↓ |
| 7-й день | 1,5±2↓ | 2,2±1,4↓* | 1,1±1,5↓ | 0↓ |
| 8-й день | 1±1,3↓ | 1,3±1↓* | 0,6±1↓ | 0↓ |
| 9-й день | 0,5±0,8↓ | 0,5±0,6↓* | 0,1±0,4↓ | 0↓ |
| 10-й день | 0↓ | 0↓ | 0↓ | 0↓ |
Примечание. ↓ — различие показателей в группах по сравнению с исходным уровнем достоверно (p
Таблица 3. Степень снижения интенсивности боли на фоне терапии
| Снижение боли по сравнению с исходным уровнем, % | 1-я группа | 2-я группа | 3-я группа | 4-я группа |
| 1-й день | –10 | –11 | –5 | –35 |
| 2-й день | –27* | –18↓* | –19↓* | –77↓ |
| 3-й день | –42 ↓* | –29* | –36* | –91 |
| 4-й день | –49* | –37* | –42* | –95 |
| 5-й день | –55* | –45* | –61* | –100 |
| 6-й день | –69* | –56* | –76* | |
| 7-й день | –76* | –67* | –85 | |
| 8-й день | –85* | –80* | –92 | |
| 9-й день | –91 | –92* | –98 | |
| 10-й день | –100 | –100 | –100 |
Примечание. ↓ — день, когда отмечалось достоверное снижение интенсивности боли (p
Терапия мовалисом в составе комплексного лечении способствовала полной редукции болевого синдрома.
У большинства женщин интенсивность болевого синдрома достоверно снижалась, начиная со 2-го дня терапии:
у пациенток 2-й группы на 18% (с 6,5±0,9 до 5,4±1,9 баллов),
у пациенток 3-й группы на 19% (с 7±1 до 5,8±1 балл),
у пациенток 4-й группы на 77% (с 7±1,9 до 1,7±2,2 балла).
У пациенток 1-й группы достоверное снижение интенсивности боли отмечалось с 3-го дня терапии на 42% (с 6,4±1,4 до 3,7±2,5 балла).
Следует отметить, что уменьшение боли на 50% и более (т.е. более, чем в 2 раза) раньше всего отмечалось у пациенток с дисменореей. У них уже со 2-го дня лечения боли снижались на 77%. У больных 1-й группы — с 5-го дня на 55%, 2-й группы — с 6-го дня на 56%, 3-й группы — с 5-го дня на 61%.
Во время лечения побочные эффекты и отказы от назначенного лечения выявлены не были. Все пациентки хорошо перенесли рекомендованный им курс терапии.
Выводы
1. Включение в комплексную терапию болевого синдрома различного генеза в качестве НПВП мовалиса 15 мг (свечи) 1 раз в день позволило уже в первые 2—3 дня лечения достоверно уменьшить интенсивность боли.
2. Такой препарат, как мовалис в виде ректальных свечей, обладающий хорошим спектром эффективности и переносимости, рекомендуется к применению в составе комплексной терапии болевого синдрома в гинекологической практике у пациенток с преимущественным ноцицептивным компонентом боли различного генеза.