Что лучше оланзапин или рисперидон
Влияние рисперидона и оланзапина на пациентов с шизофренией, шизоаффективным расстройством, большой депрессией или биполярным расстройством
Влияние рисперидона и оланзапина на прибавку в весе, физическое здоровье и исход в выборке пациентов с тяжелыми и стойкими заболеваниями в сообществе
В этом двенадцатимесячном открытом исследовании рассматривается влияние риспердала (рисперидона) по сравнению с Зипрекса (оланзапин) на увеличение веса, физическое здоровье и исходы в популяции с диагнозом шизофрения, шизоаффективное расстройство, большая депрессия или биполярное расстройство с психотическими особенностями. В этом исследовании оценивается реакция на симптомы, а также общее состояние здоровья. показатели, такие как индекс массы тела, уровни глюкозы, пролактина и холестерина на исходном уровне, месяц (M) 1, M3, M6 и M12.
| Общий статус | Завершенный | ||||
|---|---|---|---|---|---|
| Дата начала | 2000-02-01 | ||||
| Дата завершения | 2007-06-01 | ||||
| Дата первичного завершения | 2007-06-01 | ||||
| Фаза | N / A | ||||
| Тип исследования | Интервенционный | ||||
| Первичный результат |
| ||||
| Вторичный результат |
| ||||
| Регистрация | 300 |
Тип вмешательства: Препарат, средство, медикамент
Описание: Участники должны быть рандомизированы для приема оланзапина или рисперидона. Антипсихотические препараты будут вводиться ежедневно в соответствии с инструкциями на упаковке в течение двенадцати месяцев исследования.
Атипичные антипсихотики
Современными лекарственными средствами, используемыми для терапии шизофрении, считаются атипичные антипсихотики.
Свое название они получили вследствие ошибочной точки зрения, заключающейся в том, что антипсихотическое действие типичных нейролептиков обусловлено их влиянием на экстрапирамидную систему. Поскольку новые препараты, особенно первые из этого класса антипсихотиков — амисульпирид и клозапин, оказывали слабое влияние на моторику больного, их и назвали атипичными.
Если взять за основу только отсутствие экстрапирамидных эффектов, при достаточно выраженном антипсихотическом действии, то тогда к атипичным антипсихотикам следует отнести обычно причисляемый к традиционным нейролептикам перазин, поэтому, вместо термина атипичные антипсихотики, современные препараты в англоязычной литературе все чаще называют «новые антипсихотики» («novel antipsychotics») или «нейролептики второго поколения» («second-generation antipsychotics»).
В США типичные антипсихотики практически не используются. В Европе частота их применения зависит от уровня экономического развития страны.
К группе атипичных антипсихотиков, наиболее часто используемых в нашей стране, можно отнести: клозапин (лепонекс), рисперидон (рисполепт), оланзапин (зипрекса), кветиапин (сероквель), зипрасидон (зелдокс), сертиндол (сердолект), арипипразол (абилифай) (таблица 24). Некоторые психиатры относят к атипичным антипсихотикам производные бензамида: сульпирид (эглонил) и амисульпирид (солиан), однако с этой точкой зрения согласны не все авторы. В последнее время синтезировано еще два новых антипсихотика: азенапин и бифепрунокс, однако клинические испытания этих препаратов еще не закончены.
Таблица 24. Атипичные антипсихотики
Международное непатентованное название
Торговая марка
Год
выпуска
Средняя дозировка
Эффективность
Основные побочные эффекты
Высокая эффективность по отношению к позитивной, негативной и когнитивной симптоматике шизофрении, даже в случае ее резистентного течения
Выраженная седация, гиперсаливация, колебание артериального давления, тахикардия, запоры, судорожный синдром, нейтропения, агранулоцитоз, миокардит
Умеренно выраженная эффективность, отсутствие эффекта при резистентной шизофрении
Умеренно выраженная седация, в зависимости от дозы экстрапирамидная симптоматика
Умеренно выраженная эффективность, с несколько более заметным эффектом по сравнению с классическими антипсихотиками, эффективен в плане профилактики рецидивов шизофрении
Гиперпролактинеми, судорожный синдром, на начальном этапе возможны головная боль, тошнота, ажиатация
Высокая эффективность в отношении позитивных, негативных и аффективных симптомов, сомнительная эффективность в отношении резистентной шизофрении, заметное преимущество перед классическими антипсихотиками
Седация, усиление аппетита, увеличение веса, сахарный диабет, редкие случаи нейтропении и поздней дискинезии, возможны кратковременные изменения активности ферментов печени
Эффективность, аналогичная классическим антипсихотикам, эффективен по отношению к позитивным, негативным и аффективным симптомам, обладает анксиолитическим эффектом, не влияет на резистентную шизофрению
Умеренно выраженная седация пролонгация сегмента QT, редко, в зависимости от дозы, экстрапирамидная симптоматика и поздняя дискинезия
Умеренно выраженная эффективность, возможно, небольшое преимущество перед классическими антипсихотиками
Гиперпролактинеми, слабо выраженная острая экстрапирамидная симптоматика
Умеренно выраженная, аналогичная обычным антипсихотикам, эффективность в отношении негативных и позитивных симптомов, не эффективен при резистентной шизофрении
Умеренно выраженная седация, инициальная ортостатическая гипотензия, тахикардия, увеличение веса, возможны нарушения углеводного обмена и пролонгация сегмента QT
Высокая эффективность при купировании рецидива шизофрении и маниакального синдрома, эффективен как средство профилактики шизофрении. Слабая эффективность при резистентной шизофрении
На начальном этапе терапии возможны: тошнота, рвота, ажиатация,, нарушение сна, нейтрален в отношении пролактина, увеличения веса и углеводного обмена, в редких случаях развивается экстрапирамидная симптоматика
Атипичные антипсихотики применяют не только для терапии шизофрении, но и также для лечения других психозов: органически обусловленных и аффективных, интоксикационных и инфекционных, синдромов отмены и сенильных.
Возможные показания к терапии атипичными антипсихотиками
Несколько реже они применяются при лечении психомоторного возбуждения неясного генеза, синдромах помрачения сознания и наряду с традиционными препаратами в небольших дозах при расстройстве сна, аутизме, обсессивно-компульсивном расстройстве, частой рвоте, хроническом болевом синдроме (в последнем случае классические нейролептики используются чаще, чем атипичные антипсихотики).
Атипичные антипсихотики являются фармакологически гетерогенной группой, психотропный профиль их существенно варьирует.
В работах, финансируемых фармацевтическими компаниями, эти препараты часто объявляются более эффективными по сравнению с традиционными антипсихотики, подчеркивается, что они редко вызывают экстрапирамидных расстройства, более эффективны по отношению ко многим проявлениям шизофрении и, в частности, при лечении когнитивных, негативных и депрессивных симптомов, состояний, резистентных к терапии.
В большинстве исследований, построенных на основе метаанализа, амисульпирид, клозапин, оланзапин, рисперидон демонстрируют более высокую эффективность в отношении острой психотической симптоматики по сравнению с традиционными нейролептиками. Такие атипичные антипсихотики, как зотепин, арипипразол, сертиндол, кветиапин, зипразидон и ремоксиприд (ремоксиприд в 1993 году был снят с рынка из-за его способности вызывать серьезные нарушения картины крови), по эффективности купирования острой психотической симптоматики практически равны классическим нейролептикам.
К сожалению, фарминдустрия нередко диктует свои требования к исследованиям сравнительной эффективности новых и старых антипсихотиков. Для доказательства эффективности первых, в группу больных, получавших традиционные нейролептики, включаются длительно страдающие шизофренией пациенты, с частыми рецидивами этого психического расстройства. Во многих исследованиях не говорится о предыдущем лечении, его продолжительности и даже времени манифестации шизофрении.
Некоторые авторы ставят под сомнение превосходство атипичных антипсихотиков в связи с наличием у многих из них достаточно серьезных метаболических нарушений.
В исследовании J. Davis et al., (2003) было показано, что некоторые современные атипичные антипсихотики (амисульпирид, клозапин, оланзапин, рисперидон) эффективнее, чем традиционные антипсихотики, но другие атипичные антипсихотики (арипипразол, кветиапин, зипрасидон), напротив, менее эффективны, чем классические нейролептики.
В литературе встречается, на наш взгляд, неправомерная точка зрения, согласно которой все антипсихотики обладают одинаковой эффективностью при лечении шизофрении, различаясь между собой в основном уровнем дозировок, вызывающих эквивалентный антипсихотический эффект, а также профилем побочных эффектов (Tamminga C., 2000).
Некоторые психиатры считают, что атипичные антипсихотики кажутся более эффективными потому что сравниваются с более высокими дозами классических нейролептиков, другие полагают, что высокие дозы последних применяются в связи с тем, что они сравниваются с высокоэффективными атипичными антипсихотиками. По мнению некоторых исследователей, достаточно убедительных данных о влиянии атипичных антипсихотиков на первичную негативную симптоматику и когнитивные нарушения у больных шизофренией в настоящее время нет (Цыганков Б.Д., Агасарян Э.Г., 2006).
Интересно отметить, что некоторые свойства атипичных антипсихотиков, особенно в отношении воздействия на рецепторы серотонина и дофамина, демонстрировал тиоридазин.
Возможно одним из первых антипсихотиков следует считать сульпирид — препарат, появившийся во Франции в последней четверти ХХ столетия. Производный бензамидов-сульпирид обладал в относительно небольших дозах растормаживающим эффектом. Позже оказалось, что этот препарат можно использовать для лечения шизофрении.
В конце годов был синтезирован еще один препарат — клозапин. Эффект этого медикамента был необычен, в отличие от традиционных нейролептиков при его приеме практически не появлялась экстрапирамидная симптоматика. И тем не менее он купировал обострение шизофрении, оказывал терапевтический эффект при ее резистентных формах и заметно смягчал негативную симптоматику этого заболевания.
Некоторые исследователи, говорили о том, что отсутствие неврологического эффекта было скорее исключением, чем правилом. Однако данный медикамент подобно некоторым нейролептикам (левомепразин) вызывал выраженные изменения со стороны вегетативной нервной системы.
Современные атипичные антипсихотики это вещества с различной химической структурой и различном профилем чувствительности по отношению к рецепторам нейротрансмиттеров.
Большинство из этих препаратов проявляют комбинированный антагонизм по отношению к рецепторам D2/ 5HT2, но амисульпирид считается селективным антагонистом D2/D3-рецепторов. Большинство исследователей считает, что профиль психотропной активности атипичных антипсихотиков не всегда зависит от характеристик профиля блокирования рецепторов, тем более что последний окончательно неясен.
Профиль чувстительности атипичных антипсихотиков по отношению к рецепторам в настоящее время лучше исследован в плане побочных эффектов препаратов, чем в связи с особенностью их психотропной активности. Это можно проиллюстрировать на примере влияние атипичных антипсихотиков на рецепторы гистамина (H1). При этом некоторые авторы полагают, что исследование адаптивных процессов в пострецепторных окончаниях нервных терминалей приблизят нас к пониманию психотропной активности этих медикаментов.
В первую очередь атипичные антипсихотики отличаются фармакологически от антипсихотиков первого поколения более слабым сродством к дофаминовым D2-рецепторам и большим тропизмом к другим нейрорецепторам, включая серотониновые и норадренергические. У многих атипичных антипсихотиков (исключая арипипразол) механизм действия все же включает в себя ослабление «дофаминергической активности нейронов».
В основе механизма действия атипичных антипсихотиков лежит блокада центральных рецепторов дофамина и серотонина. Причем для этих препаратов характерна блокада не только рецепторов дофамина D2, но и аффинитет к серотониновым рецепторам 5НТ2А. Предполагают, что позитивный спектр эффективности атипичных антипсихотиков обусловлен в числе прочего большим блокирующим действием на 5НТ2, чем на DA-рецепторы, особенно если речь идет о негативной симптоматике шизофрении или о когнитивных нарушениях, отмеченных при этом заболевании (Meltzer, 1999).
Позитронно-эмиссионная томография — сканирование с использованием меченого раклаприда для связывания с рецепторами дофамина D2 или N-метил-спиперона для маркирования рецепторов дофамина D2, расположенных в хвостатом ядре, и рецепторов серотонина, находящихся в коре головного мозга, позволяет уточнить, какова должна быть блокада рецепторов D2 и рецепторов 5HT2 в процессе лечения шизофрении.
Отметим, что дофаминергические нейроны вентральной тегментальной области играют важную роль в реализации антипсихотического эффекта нейролептиков, тогда как дофаминергические нейроны нигростриарной области, возможно, принимают участие в развитии экстрапирамидных симптомов.
Существует точка зрения, согласно которой атипичные антипсихотики не влияют на серотониновые рецепторы или другие нейротрансмиттеры, а оказывают действие только на рецепторы дофамина D2. При этом данные препараты в отличие от традиционных нейролептиков быстро отходят от рецепторов D2 (быстрая диссоциация), тем самым вызывая своеобразный эффект. Считается, что чем быстрее происходит диссоциация, тем менее выражена экстрапирамидная симптоматика в процессе лечения. Кроме того, относительно низкий риск возникновения экстрапирамидной симптоматики при приеме атипичных антипсихотиков может быть связан с наличием у некоторых препаратов (клозапин, оланзапин) антихолинергического эффекта (Baldessarini R., Tarazi F., 2001).
Исследования показали, что для купирования острого психоза — шизофрении, необходимо, чтобы психотропный препарат блокировал более 65% рецепторов дофамина (D2). Большинство традиционных (типичных) нейролептиков уже при использовании их в терапевтических дозах обладает более выраженным антагонизмом в отношении данных рецепторов структур мозга. Они блокируют существенно большее количество рецепторов дофамина (D2). Последнее обстоятельство ведет к развитию побочных эффектов. Так, после блокады 72% и более D2-рецепторов начинается повышение уровня пролактина, 78%-появляются экстрапирамидные расстройства. Как отмечалось выше, в процессе лечения шизофрении необходимо находиться в «окне терапевтической безопасности», т.е. между 65 и 72% заблокированных D2 рецепторов.
В то же время большинство атипичных антипсихотиков блокируют менее 60% D2-рецепторов, что может оказаться недостаточным для купирования психоза. Существует точка зрения, согласно которой недостаточный уровень блокады D2-рецепторов атипичными антипсихотиками, компенсируется антагонистическим воздействием этих препаратов на 5НТ2-рецепторы, что и обеспечивает возможность купирования психоза. Однако последнее предположение вызывает сомнения в связи с тем, что представитель атипичных антипсихотиков-кветиапин (сероквель) обладает низкой аффинититетом к 5НТ2-рецепторам (Gardner D. et al., 2005).
Таблица 25. Интенсивность связывания антипсихотиков с рецепторами
Психиатрия Психиатрия и психофармакотерапия им. П.Б. Ганнушкина
№04 2004
Оланзапин: сравнение с рисперидоном (обзор исследований) №04 2004
Исследование 1. Двойное слепое сравнение оланзапина и рисперидона при терапии шизофрении и других психотических расстройств
Эффективность
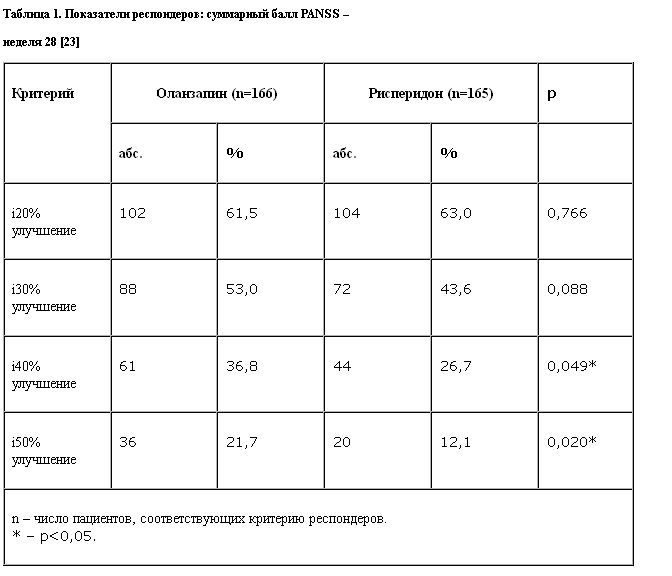
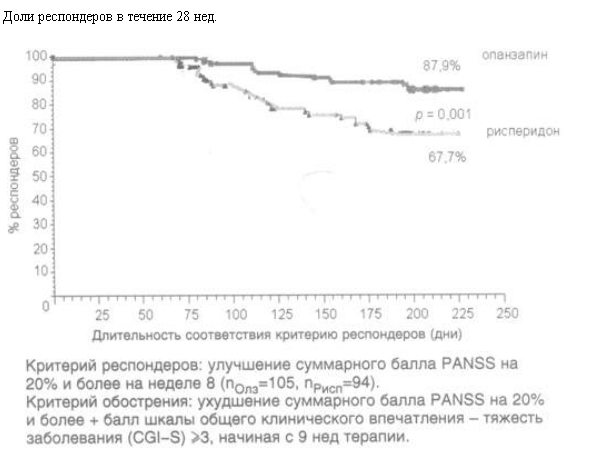
Tran и соавт. [23] опубликовали результаты двойного слепого контролируемого сравнительного исследования оланзапина и рисперидона по безопасности и эффективности. В этом 28-недельном исследовании участвовали 339 пациентов, состояние которых соответствовало критериям DSM-IV для шизофрении, шизоаффективного или шизофреноформного расстройства. До лечения состояние пациентов квалифицировалось как умеренное или тяжелое (средние суммарные исходные баллы шкалы оценки позитивного и негативного синдрома – PANSS – равнялись: оланзапин – 96,3, рисперидон – 95,7. Методом рандомизации пациентам назначали оланзапин (10–20 мг в сутки) или рисперидон (4–12 мг в сутки). Средние модальные дозы составили 7,2±2,7 и 17,2±3,6 мг/сут для рисперидона и оланзапина соответственно. На момент окончания терапии в обеих группах – оланзапина и рисперидона – отмечено статистически достоверное улучшение исходных показателей позитивной, негативной и общей психопатологической симптоматики.
При терапии оланзапином наблюдали достоверно более выраженную редукцию негативных расстройств по шкале оценки негативных симптомов – SANS (оланзапин – 4,3, рисперидон – 2,9, p=0,020), а также депрессивной симптоматики по показателю аффективных нарушений шкалы PANSS (оланзапин – 1,1, рисперидон – 0,78; p=0,004).
При использовании в качестве критерия эффективности снижения исходного суммарного балла PANSS минимум на 20% были получены сопоставимые доли респондеров в группах оланзапина и рисперидона (табл. 1).
Исследование 2. Оланзапин в сравнении с рисперидоном при терапии шизофрении: рандомизированное двойное слепое исследование в Австралии и Новой Зеландии
Эффективность
Gureje и соавт. [24] сообщили результаты многоцентрового двойного слепого сравнительного исследования оланзапина и рисперидона по безопасности и эффективности, а также показателям фармакоэкономики. В исследовании участвовали 65 пациентов из Австралии и Новой Зеландии, соответствовавших критериям DSM-IV для шизофрении, шизофреноформного или шизоаффективного расстройства. После отмены предыдущей антипсихотической терапии (длительность периода отмены до 9 дней) 62 пациента были рандомизированы для терапии оланзапином, 10–20 мг/сут (n=3 2 ), или рисперидоном, 4–8 мг/сут (n=30), в течение 30 нед.
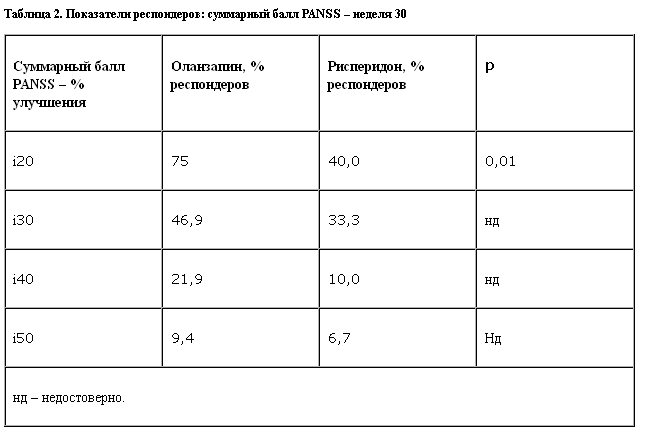
В целом исходную тяжесть состояния оценивали как умеренную (средний исходный суммарный балл PANSS был равен 94,7 в группе оланзапина и 88,9 в группе рисперидона). Средние модальные дозы составили 17,2 мг/сут для оланзапина и 6,7 мг/сут для рисперидона. Достоверное улучшение баллов PANSS – суммарного позитивных симптомов и общих психопатологических симптомов, а также суммарного балла шкалы краткой психиатрической оценки (BPRS) наблюдали в обеих группах. Через 30 нед лечения в группе оланзапина отмечено достоверно более выраженное улучшение исходного суммарного балла BPRS (оланзапин – 19,5, рисперидон – 12,7; p=0,042) и балла общей психопатологии PANSS (оланзапин – 34,1, рисперидон – 24,5; p=0,049) в сравнении с группой рисперидона.
В группе оланзапина также было больше респондеров с улучшением суммарного балла PANSS минимум на 20% в сравнении с группой рисперидона при p=0,01 (табл. 2).
На момент окончания терапии в группе оланзапина выявлено статистически достоверное улучшение исходных баллов шкалы качества жизни при шизофрении – суммарного балла, а также баллов по 3 из 4 подшкал (интрапсихический базис, межличностные отношения, общие объекты и активность). В группе рисперидона, напротив, не наблюдали улучшения ни одного из этих показателей качества жизни. Достоверные различия в улучшении исходных баллов в пользу оланзапина выявлены по одной подшкале – интрапсихический базис (p=0,014).
Безопасность
Ни одно из зарегистрированных нежелательных явлений не развивалось достоверно чаще в группе оланзапина в сравнении с рисперидоном. В свою очередь в группе рисперидона достоверно чаще отмечено 3 нежелательных явления: сонливость, ринит и запоры (p экстрапирамидными симптомами была больше в группе рисперидона как по показателям шкалы акатизии Барнса (16,7% против 6,3%), так и шкалы Симпсон–Ангус (20,0% против 6,3%). Однако эти различия между оланзапином и рисперидоном не достигали уровня статистической достоверности (p=0,200 и p=0,100 соответственно).
В обеих группах наблюдали статистически достоверное увеличение средней исходной массы тела на момент окончательной оценки (оланзапин 4,9 кг, рисперидон 4,5 кг), но без статистически достоверных различий между терапевтическими группами. Наконец, ни в одной из групп не зарегистрировано клинически значимых аномалий в лабораторных параметрах и показателях витальных функций.
Исследование 8. Изменения в клиническом статусе и побочные эффекты у пациентов, получавших терапию оланзапином или рисперидоном
Эффективность
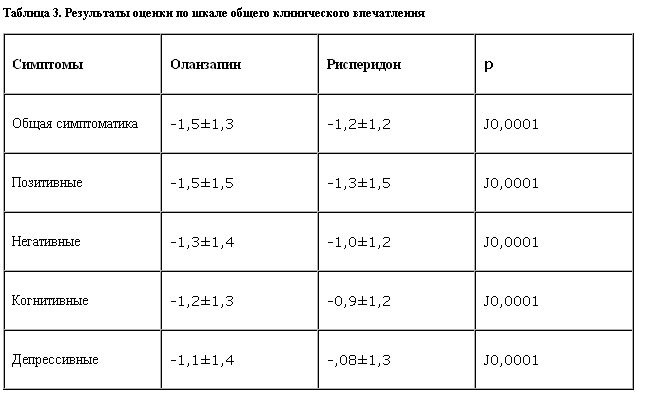
Dossenbach и соавт. [30] опубликовали в форме краткого сообщения данные за первые 6 мес 3-летнего наблюдательного исследования, в котором проводится сравнение оланзапина и рисперидона по показателям эффективности и безопасности в терапии больных шизофренией. Для оценки изменений исходных показателей общей психопатологической симптоматики, а также позитивных, негативных, когнитивных и депрессивных симптомов через 6 мес лечения использовали шкалу общего клинического впечатления (CGI). Из включенных в исследование 7655 пациентов 51% получали оланзапин и 20% – рисперидон (остальные пациенты получали какую-либо другую антипсихотическую терапию). Результаты измерений по шкале CGI приведены в табл. 3.
По всем параметрам оценки улучшение исходных показателей было достоверно более выраженным в группе оланзапина в сравнении с группой рисперидона.
Безопасность
У пациентов, получавших оланзапин, отмечали более выраженную редукцию степени тяжести имевших место до начала исследования поздней дискинезии (p=0,0445) и экстрапирамидных симптомов (p либидо 19 и 11%, импотенция 13 и 7% соответственно, p
Заключение
В клинических исследованиях оланзапина и рисперидона показано, что оба антипсихотика обеспечивают эффективный контроль над психотическими расстройствами, включая позитивные и негативные симптомы. Проведен целый ряд прямых сравнительных исследований этих двух препаратов при терапии пациентов с шизофренией, шизоаффективным или шизофреноформным расстройством. В результате некоторых из них помимо сходств были выявлены и существенные различия в профилях эффективности и безопасности оланзапина и рисперидона, что может представлять определенное практическое значение и помощь врачу в выборе той или иной терапевтической стратегии.
Оланзапин
В настоящее время многие исследователи считают оланзапин (Zyprexa) наиболее эффективным и одновременно безопасным препаратом для лечения шизофрении. Это медикамент появился на фармацевтическом рынке в 1996 г.
Химическая группа: тиенобензодиазепин.
Форма выпуска: таблетки 2,5, 5, 7,5, 10, 15, и 20 мг; выпускается в растворимой форме (зидис) в таблетках 5, 10, 15 и 20 мг, растворах для инъекций — 10 мг.
Фармакокинетика: период полувыведения — 31 час, пик концентрации — 6 часов, стабилизация концентрации достигается в течение 7 дней, биодоступность — 60%.
Режим дозирования: диапазон доз для взрослых колеблется от 5 до 20 мг, однако на практике, к сожалению, максимально допустимые дозы препарата нередко превышают рекомендуемый уровень. Детям оланзапин назначается из расчета 0,12 — 0,2 мг на кг веса обычно раза в день, для лиц пожилого возраста рекомендуемый диапазон доз — в день.
Показания: Оланзапин приводит к выраженной редукции психопатологических симптомов шизофрении и дольше других принимается больными без отказа при необходимости длительного назначения (Lieberman J. et al., 2005).
Согласно данным некоторых исследователей, отчетливо выраженное антипсихотическое действие оланзапина наблюдается (через 2 — 3 недели) прежде всего у больных приступообразно-прогредиентной шизофренией с острой параноидной симптоматикой (Ешимбетова С.З., 2005). Терапевтический эффект острого эпизода шизофрении при лечении оланзапином составляет (Морозова М.А. с соавт., 2000), причем общая редукция психоза опережает уменьшение выраженности бреда и галлюцинаций (Морозова М.А., Жаркова Н.Б., Бениашвили А.Г., 2000).
При переходе с типичных нейролептиков на внутримышечные инъекции оланзапина, при параноидной шизофрении, в литературе встречаются указания на возможное обострение состояния. Вследствие вышесказанного в данном случае желателен постепенный переход с одного препарата на другой. Возможно кратковременное назначение транквилизаторов бензодиазепинового ряда. После инъекций оланзапина больные становятся более доступными для общения с медицинским персонала.
По данным некоторых авторов (Козырев В.Н. с соавт., 2005), галлюцинаторно-бредовая симптоматика на фоне внутримышечного введения оланзапина редуцируется значительно медленнее, чем возбуждение, злобно-напряженный аффект, тревога и страх.
Лечение оланзапином шизофрении позволяет в течение двух недель снизить выраженность общей психопатологической симптоматики при этом заболевании на 52,46%, продуктивной симптоматики на 47,73%, негативной — на 13,33%. Заметно улучшаются параметры нейропсихологических нарушений: вербальной памяти на 13%, зрительной памяти на 10%, рабочей памяти и внимания — на 5%, исполнительской функции — на 1%. При дальнейшей терапии в течение недель значительно редуцируется негативная (на 46,67%) и в меньшей степени позитивная симптоматика (25,05%), продолжают улучшаться показатели вербальной памяти (на 10%) и рабочей памяти (на 8%), значительно повышаются показатели зрительной памяти и исполнительских функций (на 2%). (Панина А.Н., Говорин Н.В., 2005).
Исследования показали, что когнитивные нарушения у больных шизофренией связаны с психопатологическими расстройствами позитивного и негативного спектра, причем их редукция в процессе лечения оланзапином происходит неравномерно.
При терапии резистентной шизофрении отмечен более позитивный эффект оланзапина неделя лечения), чем клозапина (Оленева Е.В., Цукарзи Э.Э., Мосолов С.Н., 2005).
Препарат по сравнению с клозапином и рисперидоном обладает большей способностью устранять проявления депрессии при шизофрении, тем самым снижая риск суицида (Meltzer H., 1999).
Механизм действия: оланзапин обладает выраженным антагонизмом по отношению к рецепторам 5НТ2A, 5HT2C (увеличение веса?), 5HT3, 5НТ6 и менее выраженным антагонизмом в отношении D2-рецепторов (3: 1) (D2/D3 > D1/D3/D4). Кроме того, данный препарат обладает заметной чувствительностью к М1 и М5 (антихолинергические побочные эффекты), средним тропизмом к Н1 (сомноленция) рецепторам и слабо влияет на альфа1-адренорецепторы.
По спектру своего фармакологического эффекта оланзапин из всех антипсихотиков нового поколения наиболее близок к клозапину, но в отличие от последнего слабее действует на серотонинергические, на альфа2-адренорецепторы и холинорецепторы. Оланзапин, так же как и клозапин, имеет более высокое сродство к НТ2А-рецепторам, чем к дофаминовым рецепторам типа D2.
Показания к терапии шизофрении оланзапином
Оланзапин (зипрекса) назначают в дозе однократно внутрь на ночь. На второй день терапии дозу можно увеличить до 15 мг При отсутствии в течение двух-трех недель эффекта дозу повышают до 20 мг в сутки. Средние дозы оланзапина при лечении шизофрении составляют средняя поддерживающая доза — 12,5 мг
Длительность лечения оланзапином при его внутримышечном введении составляет от 1 до 7 дней (в среднем 3 дня). Первая инъекция препарата назначается в дозе 10 мг, вторая через 2 часа, третья при необходимости — через 4 часа (максимальная суточная доза 30 мг). При патологии печени и почек, при сочетании факторов, снижающих период полувыведения препарата (пожилые женщины, некурящие), число инъекции ограничивается — (Козырев В.Н. с соавт., 2005).
Перевод с внутримышечных инъекций на пероральный прием рекомендуется при дозе последнего, равной в сутки.
Помимо приема препарата в форме таблеток, используется внутримышечная форма оланзапина, обладающая седативным свойством и предложенная для купирования психомоторного возбуждения при шизофрении.
Парентеральное введение препаратов в процессе лечения шизофрении показано для быстрого купирования психомоторного возбуждения, неудовлетворительного сотрудничества больного с врачом, при наличии гастроэнтерологических заболеваниях.
Побочные эффекты: к побочным эффектам оланзапина относят сонливость, головокружение и прибавку в весе. В литературе встречаются работы, свидетельствующие о способности препарата вызывать агранулоцитоз, отмечены редкие случаи рабдомиолиза.
Побочные эффекты оланзапина
Увеличение веса при приеме оланзапина более выражено, чем при приеме других атипичных антипсихотиков. Это осложнение терапии тяжело переносится пациентами, особенно женщинами, и может повлечь за собой не только соматические, но и невротические расстройства. Профилактикой данного осложнения является низкокалорийная диета и продуманные программы физических упражнений.
Диета представляет собой уменьшенные порции приема пищи, предпочтение овощей и фруктов, сокращение калорийных продуктов до минимума и прием не менее 8 стаканов воды ежедневно.
В разное время для лечения этого осложнения предлагались такие препараты, как низатидин, амантадин, топирамат, сибутрамин и др. Однако эффект приема этих препаратов и механизм их действия в отношение снижения веса больных в большинстве исследований оказался слабовыраженным.
В настоящее время предпринимаются попытки ограничить прибавку веса, вызванную приемом оланзапина, бупропионом антидепрессанта, обладающим норадренергическим и дофаминергическим эффектом. Бупропион является относительно слабым ингибитором обратного захвата норэпинефрина и практически не оказывает влияние на центральные серотонинергические нейроны (Gadde K. et al., 2006).
Бупропион можно принимать совместно с оланзапином без негативного взаимодействия этих препаратов. Однако требуется некоторая осторожность приема бупропиона в плане возникновения маниакального синдрома, у лиц, имевших в анамнезе его проявления. Кроме того, прием бупропиона способствует более быстрой редукции негативной симптоматики шизофрении.
Замечено, что курс терапии этим антидепрессантом в среднем снижает вес за этот период почти на 3 кг, также фиксируется снижение уровня холестерина в крови, при этом уровень холестерола, липопротеидов, триглицеридов и глюкозы в крови практически остается неизменным.
Первоначальная потеря веса сохраняется после прекращения приема бупропиона не протяжение почти трех месяцев.
Сканирование тела с использованием рентгеновского метода абсорптиометрии (DXL) показало, что снижение веса в процессе лечения бупропионом, происходит за счет потери жировой ткани туловища. При этом снижение веса не сопровождается изменением плотности и минерального состава костей. Отметим, что при наличии булимии или анорексии прием бупропиона противопоказан.
Более редкими побочными эффектами оланзапина считаются тошнота, ортостатическая гипотония, брадикардия, отеки, антихолинергические эффекты и экстрапирамидная симптоматика.
При приеме оланзапина возможно повышение уровня трансаминаз печени (АСТ и АЛТ), однако практически оно не имеет клинического значения. Крайне редко наблюдаются обратимое снижение нейтрофилов и судороги. Согласно нашему наблюдению, последнее осложнение встречается в 0,5% случаев и чаще у детей и подростков.
Прием оланзапина может вызвать гиперлипедемию, увеличение концентрации в крови гликолизированного гемоглобина, гиперинсулинемию и устойчивость к инсулину (Melkersson K. et al., 2000). Рекомендуется в процессе лечения данным препаратом следить за уровнем глюкозы и липидов в крови, а также контролировать изменение плотности костных минералов организма.
Пролактинемия при приеме оланзапина отмечается редко.
Противопоказания к приему оланзапина: лейкопения, глаукома, гиперплазия простаты. Требуется соблюдать осторожность при лечении пациентов с заболеваниями печени и купировании интоксикационных психозов.
Взаимодействие с медикаментами: при совместном назначении с бензодиазепинами возможно возникновение ортостатической гипотензии и синкопальных состояний. Карбамазепин снижает уровень концентрации оланзапина в плазме крови; флувоксамин, циметидин и курение, напротив, снижают его.