Что лучше роаккутан или профайла
Лучшая Клиника Косметологии в Подольске
+7 (499) 409-03-28
+7 (962) 941-46-20
UNIMED+ Клиника Лазерной Косметологии
БОТОКС
ИЗБАВЛЕНИЕ ОТ ЦЕЛЛЮЛИТА
ПЛАЦЕНТАРНОЕ ОМОЛОЖЕНИЕ
ЛАЗЕРНАЯ ШЛИФОВКА КОЖИ
Что эффективнее – Сотрет или Роаккутан?
Что эффективнее – Сотрет или Роаккутан?
В чём разница?
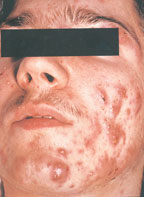
Акне – патология, 
В подавляющем проценте случаев она тяжело поддается терапии, требуя поиска и апробирования различных методик.
Иногда для избавления пациента от проблемы дерматологам приходится прибегать к крайним мерам – назначению системных медикаментов.
И если дерматологический диагноз – тяжелое течение акне, то такими системными лекарствами становятся препараты ретиноидов – производных витамина A, которые разные производители выпускают под различными коммерческими названиями.
Как же сделать свой выбор между Сотретом и Роаккутаном?
Что содержат препараты
Сотрет – препарат, производимый фармкомпанией Ranbaxy, Индия.
Он выпускается в форме капсул, содержащих главного действующего вещества – изотретиноина – по 10 и 20 миллиграмм.
Дополнительными ингредиентами таблеток являются:
Роаккутан поставляется компанией Roche из Швейцарии. Капсула может включать как 10, так и 20 миллиграмм изотретиноина. В качестве стабилизаторов используется соевое масло, но в большем, чем в Сотрете, количестве; желатин – в чуть меньшем, а пчелиный воск желтый, а не белый. Дополнительно Роаккутан содержит крахмал и многоатомные спирты, которых нет в составе Сотрета.
Действие препаратов
Основное действующее 
Абсорбируясь энтероцитами, изотретиноин поступает в кровеносное русло. На 99% связывается плазменным альбумином.
Выводится желчью и почками в равном объеме. Биодоступность увеличивается при синхронном приеме капсулы и богатой жирами пищи.
Действие метаболитов направлено на приведение себоцитов к условиям их физиологичной дифференциации, ингибирует повышенную пролиферацию выстилающих выводные протоки gl.sebaceae эпителиоцитов, разжижает детрит желез, что облегчает его выведение.
Это подавляет продукцию кожного сала, способствует лучшему дренированию желез и нормализации pH их содержимого. В результате воспалительный процесс вокруг gl.sebaceae стихает, уменьшается колонизация их бактериями.
И Роаккутан, и Сотрет:
Показания к применению Сотрет
Сотрет, как и Роаккутан, назначаются при акне конглобатных и узелковых, кистозных и форм смешанных, при опасности осложнений деформирующими постакне-рубцами.
Сотрет в форме мази показан в терапии себореи, розацеа, угрей папуло-пустулезных, периорального дерматита.
Дозировка
Инструкции к обоим препаратам рекомендуют начать прием с суточной дозы в 500 мкг/кг, при неэффективности можно увеличить ее до 1 mg/кг веса. Максимально возможной нетоксичной сывороточной концентрации можно добиться при приеме 2 mg/кг в сутки.
Как правильно принимать Сотрет?
Как Сотрет, 
Нельзя принимать ни одно из средств с другими ретинол-содержащими средствами – это только усилит токсические эффекты.
При сочетанном приеме с антибактериальными аминогликозидными средствами может развиваться внутричерепная гипертензия.
Использование местных кератолитических и эксфолиативных средств будет сильно усилено изотретиноином.
Нужно при назначении как Роаккутана, так и Сотрета учитывать, что их одновременный прием с прогестероном в микродозах взаимно ослабят свойства друг друга. В результате контрацептивные свойства КОК и мини-пили будут снижены, а это опасно ввиду опасности развития большого количества тератогенных эффектов, если при приеме изотретиноина произойдет зачатие.
Единовременный прием любого из медикаментов – Сотрета или Роаккутана – одновременно с терапией, проводимой препаратами тестостерона (особенно 19-нортестостерона), не рекомендован: это ведет к обострению или развитию эндокринологических и гинекологических патологий.
Особые указания
Назначается как Сотрет, так и Роаккутан только врачом, который должен выписать рецепт на его приобретение; у женщин, планирующих в дальнейшем беременеть, 1 рецепт выдается для покупки месячного курса медикамента.
Во время перорального применения медикаментов необходим ежемесячный контроль гемограммы, показателей печеночных проб, мочевины и креатинина, липидограммы, глюкозы крови, концентрации в ней ретинола. О старте приема Сотрета или Роаккутана дерматолог также решает после такого лабораторного обследования.
Старт терапии не стоит назначать на теплое время года или пациентам, кому показано частое лечение лучами ультрафиолета: избыточная инсоляция усиливает фотосенсибилизацию.
Противопоказания к применению Сотрет
Оба препарата противопоказаны для приема:
Препараты и беременность
Сотрет и Роаккутан, употребленные в период формирования и вынашивания плода, оказывают значительный тератогенный эффект.
Так, под их влиянием может развиться менинго- и миелоцеле, гидроцефалия, микроцефалия, микроофтальмия, дефекты развития костей черепа и трубчатых костей, «волчья пасть», тетрада Фалло, аномалии развития gll.parathyreoideae, аномалии наружного слухового аппарата, гипоплазия тимуса. Подобные пороки развития возникают, если Сотрет или Роаккутан принимала женщина: у мужчины спермальная концентрация изотретиноина неспособна запустить тератогенез.
Поэтому врач, назначающий Роаккутан или Сотрет, дает строгие рекомендации дамам фертильного возраста:
Ретиноиды проникают в грудное молоко, что оказывает токсичные эффекты на младенца. Поэтому Сотрет и Роаккутан запрещены как терапия у лактирующих женщин.
Побочные эффекты
В инструкциях к применению описаны следующие побочные симптомы препаратов изотретиноина:
Мнение специалистов
Если от пациентов можно увидеть и положительные, и отрицательные отзывы на оба препарата (приблизительно в одинаковом количестве), то дерматовенерологи высказывают такое мнение:
Важно! Хотим отметить тот факт, что врачи-дерматологи нашей Клиники не применяют в своей практике лечения акне препараты изотретиноина – Сотрет и Роаккутан, используя для терапии безопасные и более эффективные фармпрепараты.
Более подробно о методиках лечения акне вы сможете узнать во время очной консультации.
АКНЕ: патогенез и современные методы лечения
Угревую болезнь (акне) относят к числу часто встречающихся в практике врача-дерматолога заболеваний кожи. Дебют заболевания обычно проявляется у девочек в возрасте от 12 до 14 лет, у мальчиков — в 14–15 лет.
Угревую болезнь (акне) относят к числу часто встречающихся в практике врача-дерматолога заболеваний кожи. Дебют заболевания обычно проявляется у девочек в возрасте от 12 до 14 лет, у мальчиков — в 14–15 лет. В этом возрасте возможны два варианта течения заболевания — «физиологические» акне и «клинические» акне, наблюдаемые у 15% пациентов, которые требуют назначения лечения. У 7% пациентов возможно развитие поздних акне, возникающих после 40 лет [1, 3, 5].
Угревая болезнь нередко является одним из осложнений жирной или смешанной форм себореи. У значительной части больных угревая болезнь склонна к хроническому течению, частым рецидивам и нередко оказывается резистентной к проводимой терапии.
Патоморфологически вульгарные угри представляют собой гнойное воспаление сальной железы и перигландулярной ткани. Принято различать несколько клинических разновидностей этого заболевания. К более легким и относительно благоприятно протекающим формам относят вульгарные или юношеские, папулезные и пустулезные угри. Они легче поддаются лечению и обычно не оставляют после себя грубых рубцовых изменений на коже. Напротив, индуративные, сливные, флегмонозные и конглобатные угри в связи с резистентностью к проводимой терапии, частыми рецидивами и возникновением при этих формах грубых косметических дефектов представляют для врача и больного сложную медицинскую и социально-психологическую проблему [3].
Психоэмоциональные расстройства выявляются у 40–50% пациентов с угревой болезнью, ведущим является нозогенная депрессия невротического уровня, чаще протекающая по астено-тревожному и тревожному типам. Наибольшая частота психоэмоциональных расстройств наблюдается при II–III степени тяжести акне, при этом характерна обратная зависимость выраженности психоэмоциональных расстройств от степени тяжести и длительности болезни [2].
Поэтому важным для практического врача является ранняя диагностика, правильная клиническая оценка, своевременное назначение эффективных и безопасных препаратов в зависимости от клинической формы заболевания, что позволяет избежать состояния дисморфофобии, неудач в лечении и улучшить качество жизни больных.
Патогенез акне является мультифакторным. На сегодняшний день выделяют четыре ведущих фактора в этиологии заболевания: фолликулярный гиперкератоз, увеличение количества Propionibacterium acnes, изменение продукции кожного сала и воспаление.
Начальным этапом формирования заболевания является появление микрокомедонов, которые в дальнейшем колонизируются Propionibacterium acnes. Микрокомедоны являются результатом развития двух процессов — гиперпролиферации кератиноцитов акроворонки волосяного фолликула и избыточной продукции кожного сала, что в сочетании приводит к закупорке фолликула и формированию открытых и закрытых комедонов. Для кератиноцитов характерно увеличение тонофиламентов и десмосом, повышенное количество кератинов К6 и К16 [9].
Propionibacterium acnes являются анаэробными резидентными представителями микрофлоры кожи человека, способными проявлять свои патогенные свойства только в определенных условиях. Propionibacterium acnes участвуют в развитии воспаления в очаге заболевания, способствуя освобождению хемотаксических факторов и цитокинов, а также превращению триглицеридов кожного сала в свободные жирные кислоты.
В механизме развития акне важными являются следующие компоненты патогенеза — относительный недостаток линолевой кислоты, действие андрогенов и свободных жирных кислот. На продукцию кожного сала огромное влияние оказывают андрогены, которые в большом количестве начинают поступать в кожу в пубертатном периоде, определенное значение имеет гормон роста, инсулиноподобный фактор роста и вещества, активирующие образование пероксисом [8].
Мишенями действия половых гормонов в коже являются эпидермис, волосяные фолликулы, сальные железы, фибробласты. На продукцию кожного сала влияют гормоны тестикулярного или овариального (свободный тестостерон) и надпочечникового (дегидроэпиандростерон, андростендион) происхождения. Подобное действие оказывает и предшественник тестостерона, эстрогенов и адренокортикостероидов — прогестерон, обладающий андрогенным и антиэстрогенным воздействием на секрецию сальных желез. Этим объясняется повышение салоотделения и усиление образования акне в предменструальный период.
Важное значение имеет не только повышение уровня андрогенов, но и повышенная чувствительность клеток-мишеней, в частности клеток сальной железы, к андрогенам, циркулирующим в крови.
В патогенезе угрей важная роль отводится дефициту цинка, который регистрируется у 80% больных. На фоне цинкдефицитного состояния возрастает темп экскреции кожного сала, а тяжесть течения болезни коррелирует со степенью снижения цинка в организме больного. Цинк снижает активность 5a-редуктазы, что способствует нормализации соотношения гормонов и ведет к уменьшению салоотделения.
Наружная терапия является первой линией лечения акне у новорожденных, в детском возрасте, при дебюте акне и юношеских угрях. Назначение только наружной терапии показано при легких воспалительных и невоспалительных формах акне, невоспалительных формах акне средней тяжести. Во всех остальных случаях назначается комбинированная терапия с системными препаратами.
Препараты для наружной терапии назначаются длительно, минимальный курс лечения составляет 3 мес, после окончания курса необходимо назначение лекарственных средств с профилактической целью для предотвращения обострения заболевания.
В 2002 г. разработаны рекомендации и алгоритм патогенетического лечения различных форм акне (XX Всемирный конгресс по дерматологии, Париж, 2002), в которых препаратами первого выбора врача при лечении акне являются местные ретиноиды. Топические ретиноиды влияют на процессы ороговения (кератинизацию и десквамацию), снижают салоотделение, усиливают пролиферацию эпителиоцитов кожи и обладают определенным противовоспалительным действием. Наиболее перспективным является адапален (дифферин), обладающий хорошей переносимостью, отсутствием фотосенсибилизирующего действия, высокой эффективностью при комедональных и папуло-пустулезных акне [6]. Адапален применяется после очищения кожи 1 раз в сут на ночь, стойкое клиническое улучшение наблюдается через 3 мес, в поддерживающем режиме препарат наносят 2–3 раза в неделю.
Бензоила пероксид (базирон АС, окси-5, окси-10) после нанесения на кожу приводит к освобождению активных форм кислорода, уменьшению синтеза свободных жирных кислот и образования микрокомедонов. Препарат обладает выраженным влиянием на P. acnes, St. epidermidis, Malassezia furfur и снижает риск развития резистентности при комбинировании с антибиотиками. Выпускается бензоил пероксид в виде геля 2,5 –10% и 5–10% лосьона. Бензоил пероксид наносят на кожу 2–3 раза в день в течение 1–3 мес. Побочными эффектами препарата являются раздражающее действие, особенно при применении высоких концентраций, а также повышение фоточувствительности за счет истончения рогового слоя. Препарат способен обесцвечивать волосы, поэтому рекомендуется его применение при сочетании акне и гипертрихоза. Противопоказанием является повышенная чувствительность к компонентам препарата.
Широко применяется для наружного лечения акне азелаиновая кислота (скинорен), обладающая способностью нормализовать процессы кератинизации фолликула, антимикробным и противовоспалительным действием, способная уменьшать пигментацию кожи [6]. Препарат выпускают в виде 20% крема и 15% геля. Наносят его на всю поверхность лица или другие пораженные участки кожи утром и вечером, лечение продолжают до достижения терапевтического эффекта. Специфических противопоказаний к препарату нет.
Топические антибиотики. Назначение показано при папуло-пустулезных акне легкой и средней тяжести в комбинации с топическими ретиноидами или бензоил пероксидом. Среди антибиотиков для наружного применения на первом месте стоят эритромицин, клиндамицин, фузидиевая кислота. Монотерапия местными антибиотиками не даст желательного эффекта, так как не оказывает достаточного влияния на основные патогенетические факторы, кроме колонизации P. acnes.
Эритромицин выпускается в комбинации с препаратом цинка (зинерит). Лосьон наносят на кожу 2 раза в день в течение 12 нед. Побочное действие — сухость, жжение, дерматит.
Клиндамицин выпускается в виде 1% геля или лосьона, который при нанесении на кожу гидролизуется в выводных протоках сальных желез. Несмотря на минимальное всасывание, препарат может вызывать нарушения со стороны желудочно-кишечного тракта, аллергические реакции. Наносят препарат 1–2 раза в день в течение 3 мес.
Фузидиевая кислота выпускается для наружного применения в виде 2% крема (фуцидин), обладает способностью хорошо проникать через неповрежденную кожу и оказывает выраженное бактерицидное действие [7]. Крем применяют 2 раза в день в течение 7 дней. Не отмечено системного действия препарата и индивидуальной непереносимости.
Местные формы антибиотиков обычно хорошо переносятся, аллергический контактный дерматит развивается редко. Длительное наружное применение антибиотиков может привести к развитию бактериальной резистентности P. acnes.
α-гидроксикислоты (АНА) — яблочная, тартаровая, цитрусовая, молочная, гликолевая — обладают комедолитическим свойством. При концентрации АНА 30–70% (гликолевый пилинг) лечение проводится утром 1 раз в день, в вечернее время назначают ретиноиды. Препараты с концентрацией кислоты 10–15% (эксфолиак, крем 10; эксфолиак, крем 15) назначают пациентам с акне ежедневно в течение 8 нед. При низких концентрациях АНА лекарственные средства назначаются в межрецидивный период и для профилактики осложнений угревой болезни (рубцов и пигментации).
β-гидроксикислоты — салициловая кислота, резорцин — влияют на фолликулярный гиперкератоз, так как являются слабыми кератолитиками и обладают противовоспалительными свойствами. Применяются в различных лекарственных формах, чаще — растворах (салициловая кислота 0,5%–5%, резорцин 1–3%).
Гиалуроновая кислота в сочетании с цинком (куриозин, гель) используется как профилактическое средство после разрешения клинических проявлений акне. Гиалуроновая кислота способствует формированию косметических рубцов. Препарат наносят 2 раза в сут до достижения клинического эффекта. Побочными реакциями являются жжение, чувство стягивания кожи, легкая гиперемия, которые самостоятельно исчезают при продолжении терапии.
Системная терапия акне показана для лечения больных с акне средней или тяжелой формы, особенно в случаях образования рубцов, дисхромий или значительных психосоциальных расстройств. Системная терапия может быть необходима при непереносимости или неэффективности местного лечения.
Наиболее эффективным препаратом для лечения акне среднетяжелой и тяжелой форм является изотретиноин (роаккутан), который при системном применении вызывает длительные ремиссии или излечение у большинства больных. Препарат является ретиноидом, рекомендуемым для системного применения, влияет на процессы дифференцировки и кератинизации клеток эпидермиса, в том числе сальных желез, обладает выраженным себостатическим и противовоспалительным действием. Оптимальная суточная доза изотретиноина составляет 0,5–1,0 мг на 1 кг массы тела больного. Стандартная начальная терапевтическая доза 0,5 мг/кг. Обычные сроки лечения составляют 4–8 мес. После достижения выраженного терапевтического эффекта (чаще к концу 2-го месяца) начальная суточная доза снижается (с 1,0 до 0,5 мг/кг; с 0,5 до 0,2–0,3 мг/кг) и используется до излечения пациента. При флегмонозных и конглобатных угрях снижение суточной дозы целесообразно проводить в более поздние сроки (через 3–4 мес после начала лечения) [3].
Роаккутан обладает тератогенным действием, что ограничивает его применение для женщин детородного возраста. До начала лечения обязательно исключается беременность, пациентки должны использовать эффективные контрацептивные средства за 1 мес до начала лечения, весь период лечения и в течение 1 мес после его прекращения.
Побочные реакции при приеме роаккутана многообразны и касаются различных органов и систем (сухость кожи и слизистых, хейлит, конъюнктивит, носовые кровотечения, ретиноидный дерматит, фотосенсибилизация кожи, мышечная скованность, гиперостоз, повышение активности трансаминаз, липидов крови и др.), кроме тератогенного эффекта остальные побочные реакции являются дозозависимыми. До начала и в процессе лечения необходим тщательный контроль состояния пациента. Пациенты с почечной и печеночной недостаточностью, сахарным диабетом, склонностью к нарушению обмена веществ (гиперлипидемия) не должны получать лечение этим препаратом.
Системные антибиотики. Наиболее часто применяют эритромицин и тетрациклин. Лечение антибиотиками проводят длительно, 6–8 нед и дольше. Назначаются дозы с 1 г в сутки циклами по 5–10 дней без перерывов, но со снижением суточной дозы в каждом последующем цикле на 0,1–0,2 г, доводя постепенно суточную дозу до 0,1–0,2 г [3]. Одновременно с антибиотиками необходимо назначать противогрибковые препараты для профилактики кандидозов и препараты цинка (сульфат или окись цинка 0,02–0,05 — 2–3 раза в день после еды). Противопоказаниями для назначения системных антибиотиков являются индивидуальная непереносимость, беременность и кормление грудью, наличие сопутствующих грибковых поражений кожи и слизистых, тяжелые заболевания печени и почек, лейкопении.
Оральные контрацептивы (диане-35) обладают фармакологическим действием, связанным с блокированием рецепторов андрогенов и уменьшением их эндогенного синтеза. В результате тормозится секреция сальных желез. Диане-35 содержит 2 мг ципротерона ацетата и 35 мкг этинилэстрадиола. Препарат назначают только женщинам, с 5-го дня менструального цикла ежедневно 1 драже в сутки в течение 21 дня, затем — 7-дневный перерыв. Противопоказаниями для назначения препарата являются беременность и лактация, тяжелые заболевания печени, тромбоэмболические процессы, сахарный диабет, нарушения липидного обмена, гипертоническая болезнь.
По степени влияния на основные факторы патогенеза действие препаратов проявляется так, что ретиноиды являются самыми эффективными средствами для контроля гиперкератинизации фолликула и предотвращения развития микрокомедонов. В меньшей степени на этот процесс влияют бензоил пероксид, азелаиновая и салициловая кислота. По влиянию на P. acnes на первом месте стоит бензоил пероксид, затем антибиотики и азелаиновая кислота и в меньшей степени изотретиноин. Уменьшению секреции кожного сала способствуют ретиноиды и гормональные препараты. Менее всего современные лекарственные средства влияют на процесс воспаления в области угревых элементов [8].
Ни один из современных методов лечения угрей не может гарантировать отсутствие рецидивов заболевания в будущем. Поэтому при достижении клинического выздоровления каждому пациенту следует рекомендовать комплекс лечебно-профилактических мероприятий, которые могут быть разделены на рекомендации по уходу за кожей и общие.
Среди общих рекомендаций важными являются санация очагов хронической инфекции, обследование органов желудочно-кишечного тракта и эндокринной системы, общее закаливание организма.
Диета с ограничением шоколада, кофе, углеводов, алкоголя должна рекомендоваться в тех случаях, когда употребление в пищу этих продуктов приводит к усилению жирности кожи лица и обострению заболевания.
Развитие акне не связано с недостаточностью ухода за кожей лица, как это часто считают пациенты, начиная лечение заболевания с посещения косметолога. В то же время выполнение ежедневных очищающих процедур косметического характера показано при любой тяжести заболевания. Рекомендуется ежедневное очищение кожи с использованием различных моющих средств, поддерживающих нейтральный или кислый рН кожи и обладающих антибактериальным действием. Пациент должен знать о необходимости исключения косметических средств, вызывающих закупорку протоков сальных желез (мази, жирные кремы), и скрабов.
Таким образом, располагая широким выбором средств для лечения акне и косметической продукцией для ухода за кожей, склонной к угревой болезни, врач в процессе лечения может переходить от направленного воздействия на одни механизмы патогенеза к препаратам, влияющим на его другие компоненты. При этом самым важным является регулярная коррекция назначенного лечения и длительное динамическое, диспансерное наблюдение за пациентом, даже после достижения клинической ремиссии.
Литература
И. Г. Сергеева, кандидат медицинских наук
Ю. М. Криницына, доктор медицинских наук
Новосибирский государственный университет, Новосибирск
Эффективность vs неэффективность системных ретиноидов при акне
Акне (вульгарные угри) считается одним из наиболее распространенных заболеваний кожи [1]. По разным данным, частота его встречаемости составляет 60–85%. Чаще патологией страдают подростки и лица молодого возраста. Акне занимает первое место среди заболеваний кожи в данной популяции.
Несмотря на обилие лекарственных средств, лечение акне остается сложной задачей.
Недостаточная эффективность лечения, ассоциированные с данной нозологией аффективные расстройства, такие как дисморфофобия и депрессия, существенно снижающие качество жизни больных и способствующие их социальной дезадаптации, обусловливают медико-социальную значимость проблемы.
Воспаление поддерживается липидными медиаторами: лейкотриенами, простагландинами и 15-гидроксиэтоксисатетраеновыми кислотами [2].
Синтез провоспалительных цитокинов осуществляется через NF-κβ или через Toll-подобные рецепторы (Toll-Like Receptors – TLRs). С помощью TLRs происходит высвобождение антимикробных пептидов (бета-дефенсинов) и металлопротеиназ, которые способствуют развитию воспаления и образованию рубцов при акне [3].
Кроме того, в многочисленных исследованиях установлено, что развитие акне происходит на фоне нескольких взаимосвязанных патогенетических процессов. Наиболее значимыми являются нарушение кератинизации, фолликулярный гиперкератоз, избыточная продукция жирового секрета, что сопровождается дисбалансом липидов и размножением микроорганизмов [4].
Усиление секреции кожного сала происходит за счет увеличения синтеза андрогенов или повышения чувствительности рецепторов к ним. Ранее установлено, что андрогены, такие как тестостерон, дегидроэпиандростерон сульфат и дигидротестостерон, регулируют гены, ответственные за рост сальных желез и выработку кожного сала. Фермент альфа-редуктаза катализирует превращение тестостерона в 5-альфа-дегидротестостерон, экспрессирующийся преимущественно в коже. У пациентов с акне выявлена более высокая активность 5-альфа-редуктазы 1-го типа [5].
Гиперандрогения приводит к изменению не только количественного, но и качественного состава себума. Концентрация альфа-линоленовой кислоты – регулятора дифференцировки кератиноцитов фолликула снижается. В результате нарушения последней развивается фолликулярный кератоз, приводящий к закупорке сальной железы.
В пубертатном периоде гипофиз секретирует гормон роста, который стимулирует выработку инсулиноподобных факторов роста. Себоциты содержат рецепторы к инсулиноподобным факторам роста, взаимодействие с которыми приводит к росту сальной железы. Эстрогены напрямую ингибируют секрецию тестостерона и участвуют в регуляции генов роста сальной железы. Нестабильный гормональный фон и низкий уровень эстрогенов также способствуют развитию акне.
Лечение акне зависит от степени его тяжести. Так, при легкой степени ограничиваются наружными средствами, при средней – назначают антибиотики.
Наиболее эффективными в терапии акне средней и тяжелой степени являются системные ретиноиды – изотретиноин. Изотретиноин показан пациентам с узловато-кистозными угрями и часто рецидивирующими воспалительными высыпаниями, у которых антибиотики оказались неэффективными, а также больным с тенденцией к разрешению акне в виде рубцов.
В последние годы спектр показаний для назначения изотретиноина расширяется, в том числе в отношении лечения единичных, но рецидивирующих высыпаний на лице. Ряду больных они доставляют много страданий. Прежде всего это относится к публичным лицам – артистам, танцорам, журналистам и т.д., которые хотят быстрого и стойкого эффекта.
Являясь комедонолитиком, системный изотретиноин воздействует на патологическую фолликулярную кератинизацию и функцию сальных желез. Несмотря на то что препарат не обладает прямым антибактериальным эффектом, он способен влиять на хемотаксис и фагоцитоз и таким образом уменьшать численность Cutibacterium [6]. Уже через две недели от начала лечения изотретиноином уменьшается продукция кожного сала. Как следствие, рост микроорганизмов и провоспалительных медиаторов резко сокращается.
На сегодняшний день изотретиноин является единственным препаратом, который эффективен в отношении большинства звеньев патогенеза акне. Это обусловлено молекулярными механизмами действия. Взаимодействуя с ядерными рецепторами, изотретиноин уменьшает дифференцировку клеток сальных желез, что способствует выраженному уменьшению размеров и активности себоцитов.
Изотретиноин назначается на шесть месяцев и более в дозе от 0,1 до 1,0 мг/кг в зависимости от тяжести заболевания. Обязательным условием является прием препарата во время еды.
К сожалению, из-за побочных эффектов, в первую очередь тератогенного действия, ряд врачей, прежде всего вследствие недостатка клинического опыта, ограничивают назначение изотретиноина.
Наиболее частыми нежелательными явлениями на фоне терапии изотретиноином считаются хейлит и сухость кожи. Иногда могут отмечаться ухудшение зрения в ночное время, конъюнктивит, повышенная фоточувствительность, транзиторная потеря волос, артралгия и миалгия, головная боль, транзиторное повышение печеночных трансаминаз, триглицеридов и холестерина. Однако частота развития перечисленных явлений крайне низка.
Ввиду тератогенного действия на центральную нервную систему и сердечно-сосудистую систему плода изотретиноин нельзя принимать во время беременности.
Бытует мнение, что после курса системных ретиноидов высока вероятность рождения ребенка с уродствами и планировать беременность следует только через два года по окончании лечения. Однако период полураспада изотретиноина в отличие от других ретиноидов (этретината и ацитретина) составляет 19 часов. Поэтому женщинам, получающим его, необходимо использовать средства контрацепции только в период терапии и еще в течение месяца по ее завершении. Чтобы минимизировать риск развития данного нежелательного явления, все пациентки детородного возраста перед началом лечения должны получить консультацию по поводу методов контрацепции.
Для лечения среднетяжелых и тяжелых форм акне уже несколько лет с успехом применяется Акнекутан, в производстве которого используется запатентованная технология Lidose® (Бельгия).
Как известно, изотретиноин относится к плохо растворимым соединениям и всасывается в пищеварительном тракте не полностью. Технология Lidose® предполагает добавление двух компонентов в состав каждой капсулы препарата Акнекутан (Гелюцира и Спана). Благодаря этому увеличивается растворенная фракция изотретиноина в капсуле и, как следствие, его абсорбция. Биодоступность увеличивается на 20% по сравнению с обычной формой изотретиноина. Это позволяет уменьшить количество изотретиноина в каждой капсуле, так как количество работающего вещества полностью соответствует таковому в оригинальном препарате (12 мг из 16 мг Акнекутана или 12 мг из 20 мг Роаккутана), а количество неактивного уменьшается на 50% (4 мг в Акнекутане и 8 мг в Роаккутане). В результате риск развития побочных эффектов снижается.
Необходимо отметить, что биодоступность Акнекутана в меньшей степени зависит от приема пищи, чем биодоступность обычной формы изотретиноина. Так, при приеме без пищи Акнекутан абсорбируется на 70%, препараты обычной формы изотретиноина – только на 38%.
Таким образом, применение изотретиноина в составе Акнекутана позволяет на 20% снизить количество принимаемого пациентом изотретиноина без ущерба для терапевтической эффективности, а также быть уверенным в том, что даже при неполном соблюдении пациентом правил по приему препарата с пищей курсовая доза изотретиноина будет набрана.
Рекомендуемая суточная доза Акнекутана составляет 0,4–0,8 мг/кг, курсовая – 100–120 мг/кг.
Под нашим наблюдением находилось 190 пациентов (105 (55,3%) женщин и 85 (44,7%) мужчин) в возрасте от 14 до 27 лет. Степень тяжести заболевания определяли с помощью дерматологического индекса акне (ДИА) путем подсчета воспалительных элементов – папул, пустул и узлов. У 114 (60%) больных диагностирована средняя степень тяжести, у 76 (40%) – тяжелая. Пациенты ранее применяли разные методы лечения многократными курсами: системные антибиотики, метронидазол, антиандрогены, наружные средства, плазмолифтинг, чистки, пилинги, мезотерапию, физиотерапевтические процедуры и др. Однако эффект был временный.
Акнекутан назначали после обследования, которое включало клинический и биохимический анализ крови, у женщин при наличии болезненных и обильных менархе – исследование гормонального профиля.
Способ применения Акнекутана – из расчета 0,4–0,8 мг/кг/сут во время приема пищи. Суточная доза зависела не только от массы тела, но и от выраженности клинических проявлений акне.
Для нивелирования проявлений ксероза и хейлита пациенты применяли крем для лица Перфэктоин и увлажняющие губные помады.
При достижении выраженного улучшения суточная доза Акнекутана постепенно снижалась.
Длительность лечения определялась сроками достижения кумулятивной дозы препарата – 100–120 мг/кг. В среднем она составила 32,4 ± 4,6 недели.
Лечение продолжали до достижения клинической ремиссии. Поэтому редукция показателей ДИА у всех пациентов составила 100% (рис. 1 и 2).
Нежелательные явления носили дозозависимый характер, наблюдались в первые три-четыре месяца и были представлены хейлитом (190 (100%) больных), ретиноевым дерматитом (180 (94,7%)), конъюнктивитом (17 (8,9%)), носовыми кровотечениями (7 (6,7%)), транзиторным повышением трансаминаз (75 (39,4%)), гиперлипидемией (38 (20%)), миалгиями и артралгиями (5 (2,6%)), головной болью (5 (2,6%)).
Побочные явления легко переносились пациентами и не были серьезными.
Нежелательные явления со стороны кожи и органов зрения легко купировались увлажняющими средствами, губными стиками, средствами искусственной слезы.
Изменения показателей клинического и биохимического анализа крови были незначительными и не превышали 20–30% от исходных значений.
При транзиторном повышении трансаминаз назначался гепатопротектор и снижалась суточная доза препарата.
Через один – три года после лечения рецидивы отмечены у девяти пациентов, из них восемь женщин и один мужчина. Эти пациенты были более тщательно обследованы гинекологом и эндокринологом. У шести выявлено повышение уровня тестостерона и дегидроэпиандростерона, у двух – поликистоз яичников по результатам ультразвукового исследования органов малого таза. В двух случаях отмечалось увеличение лютеинизирующего гормона и изменение соотношения «лютеинизирующий гормон/фолликулостимулирующий гормон» > 2. У всех пациенток в анамнезе нарушение менархе.
У двух пациентов (одна женщина и один мужчина) с повышенной массой тела диагностировано нарушение толерантности к глюкозе.
Полученные нами результаты свидетельствуют о высокой эффективности Акнекутана.
Необходимо отметить, что женщинам с рецидивирующими, устойчивыми к проводимой терапии вульгарными угрями и гормональными нарушениями, обусловленными прежде всего гиперандрогенией, рекомендуется лечение половыми гормонами. Прием пероральных гормонов уменьшает секрецию кожного сала, ингибирует эффекты андрогенов в сальных железах.
При угревой болезни используют три группы гормонов: эстрогены, которые подавляют овариальные андрогены, глюкокортикоиды, которые ингибируют надпочечниковые андрогены, и пероральные антиандрогены, которые действуют на периферическом уровне. Эстрогены в небольших дозах (35–50 мкг), применяемые в качестве пероральных противозачаточных средств, способны значительно снизить секрецию сала. Лечение антиандрогенами проводится после консультации с гинекологом-эндокринологом, при этом может потребоваться оценка гормонального профиля крови (уровня лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола, прогестерона, тестостерона, пролактина и дегидроэпиандростерона), ультразвуковое исследование органов малого таза и надпочечников, рентген/томография черепа/мозга.
При средней и тяжелой степени акне лечение гормональными препаратами может проводиться в комплексе с системными ретиноидами или антибиотиками.
Риск развития рецидивов после полноценного курса системных ретиноидов может быть обусловлен синдромом поликистозных (мультифолликулярных) яичников, аденомой гипофиза, опухолью надпочечников или врожденной гиперплазией коры надпочечников, заболеванием щитовидной железы, нарушением толерантности к глюкозе и др. Поэтому необходима консультация гинеколога и эндокринолога.
Другой важной причиной рецидивов является недостаточная суммарная доза изотретиноина или несоблюдение режима приема препарата. Вероятность рецидива при применении низких доз значительно возрастает, что требует более продолжительного курса лечения, чем при использовании стандартных схем [7]. А.L. Zaenglein и соавт. установили, что рецидивы при кумулятивной дозе более 150 мг/кг возникают реже, чем при дозе менее 120 мг/кг [8]. Наименьшая частота рецидивов отмечается при кумулятивной дозе 220 мг/кг [8].
В нашем наблюдении все пациенты получали адекватные дозы в зависимости от степени тяжести кожного процесса и массы тела.
Акнекутан является высокоэффективным и безопасным препаратом для лечения акне средней и тяжелой степени. Побочные эффекты незначительны, легко купируются и не требуют отмены препарата.
Как показал наш опыт, рецидивы при применении изотретиноина возникают при наличии сопутствующих эндокринных заболеваний и гормональных нарушений, поэтому лечение акне в таких случаях необходимо проводить совместно с другими специалистами – гинекологами и эндокринологами. Рецидивы могут быть обусловлены назначением неадекватной суточной и кумулятивной дозы препарата, а также нарушением режима его приема.