Что лучше таурин или лецитин
Лецитин. Чем помогает и как принимать
Порошковый лецитин считается одной из самых полезных добавок для здоровья. Но мало кто знает, насколько широка его сфера применения! О том, чем полезен, какой выбрать и как принимать лецитин пойдет речь ниже.
История появления лецитина
Впервые его открыл ученый из Франции Т. Гобли, который в 1845 году выявил схожесть в составе тканей мозга и яичного желтка. По его теории, которая вскоре была доказана, именно лецитин является объединяющим компонентом. Он на 75% состоит из фосфолипидов, триглицеридов, это жироподобное вещество. Именно фосфолипиды являются составляющими клеточных мембран, они содержаться в большинстве живых организмов и тканей. Так, их очень много в тканях мозга, печени, плазме крови, сердца, желчи.
Современные источники лецитина
Есть вопросы по препаратам?
Звоните, и наши консультанты ответят!
8 (800) 550-96-15 (звонок бесплатный)
Из чего состоит лецитин
В нем гармонично сочетаются 4 формы фосфолипидов:
Таким образом, лецитин это не один ингредиент, как думают многие. А целый комплекс, смесь ценных фосфолипидов, которые по-своему влияют на организм человека.
Общая полезность
Как уже было сказано, фосфолипиды составляют структуру клеточных мембран, участвуют в большинстве процессов в организме. Кроме того, лецитин очень полезен для печени, поскольку содержит фосфатидилхолин, составляющее печеночных клеток. Когда печень болеет, мембраны клеток разрушаются, а лецитин и ее компоненты восстанавливают их.
Кроме того, это вещество обладает хорошими антиоксидантными свойствами и действует на клетки печени как детокс. Важно! Лецитин, в большем или меньшем количестве, входит в состав большинства аптечных гепатопротекторов (Эссенциале форте Н, Доппельгерц и другие). Это еще одно доказательство полезности его для печени.
Полезность лецитина для сосудов и крови
Вот кому особенно показаны биодобавки с лецитином
Есть ли противопоказания у лецитина
Поскольку это натуральная добавка, которую производят из сои или семян подсолнечника, она почти не имеет противопоказаний. Но лецитин стоит принимать с осторожностью или под контролем врача в таких случаях:
Беременным и кормящим можно принимать это вещество, но только после консультации со своим врачом.
Лецитин в порошке, таблетках или гранулах
Как принимать порошковый лецитин? Очень просто и удобно! Берем 1-2 ст. ложки порошка и смешиваем с любой свежеприготовленной пищей (обычно это каша, йогурт). Можно также просто запивать порошок водой или разводить в воде и сразу выпивать. Оставшуюся смесь нужно хранить в плотно закрытой банке, желательно на дверце холодильника, без перепадов температур.
Какие побочные действия возможны?
Как правило, при правильном, регулярном приеме их не наблюдается. Но в начале приема возможны некоторые кратковременные расстройства:
Обращайте внимание на эти симптомы! Они должны пройти через 1-2 дня после начала приема препарата. Если этого не случилось, прекратите прием и обратитесь к врачу. Еще один возможный симптом: кожный зуд, насморк могут быть признаком аллергии на лецитин или другие компоненты. Прием в этом случае нужно прекратить.
Заключение
Целесообразность применения таурина в лечении неалкогольной жировой болезни печени
К.м.н. О.Н. ОВСЯННИКОВА, д.м.н., проф. Л.А. ЗВЕНИГОРОДСКАЯ
ЦНИИ гастроэнтерологии, Москва
Проведено двойное слепое плацебоконтролируемое сравнительное клиническое исследование, в котором оценивалась клиническая эффективность таурина (препарат Дибикор, производитель «ПИК-ФАРМА») у больных с неалкогольной жировой болезнью печени (НАЖБП) и сахарным диабетом 2 типа (СД 2 типа) в сравнении с плацебо. Результаты показали, что применение препарата Дибикор оказывает гиполипидемический и гепатопротективный эффект, улучшает показатели углеводного и жирового обмена, способствует снижению массы тела, улучшению самочувствия больных и может быть рекомендовано для коррекции и профилактики метаболических нарушений в терапии НАЖБП.
Впоследние годы неалкогольную жировую болезнь печени (НАЖБП) рассматривают как неотъемлемый компонент метаболического синдрома (МС). МС представляет собой комплекс связанных между собой факторов, включащих инсу-линорезистентность, нарушение углеводного обмена, абдоминально-висцеральное ожирение, артериальную гипертензию, ате-рогенную дислипидемию и др. Печень при МС является одним из основных органов-мишеней [1, 2]. Согласно данным ряда источников, частота патологии печени у больных с МС составляет от 37 до 64%.
НАЖБП: этиология, патогенез, задачи терапии
К этиологическим факторам развития НАЖБП относятся метаболические расстройства и эндокринопатии (инсулинорезистентность или СД, ожирение, подагра, гиперлипидемия, гипотиреоз, гипертиреоз, синдром Кушинга и др.); нарушение процессов пищеварения и всасывания (патология поджелудочной железы, тонкой кишки, синдром нарушенного всасывания, избыточное питание, голодание, парентеральное питание, синдром избыточного бактериального роста в кишечнике); действие лекарств, химических субстанций, фитотоксинов, токсинов грибов; инфекции; анемия, сердечно-сосудистая и дыхательная недостаточность и др. [3, 4]. НАЖБП имеет несколько стадий развития: от простого стеатоза до стеатогепатита, фиброза и цирроза печени. Симптомы, свойственные заболеваниям печени, отсутствуют у большинства больных, только некоторые из них отмечают незначительный дискомфорт или боль в правом верхнем квадранте живота [1]. У большей части пациентов НАЖБП протекает благоприятно, без значительных клинико-морфологических изменений. Поскольку возможность проведения пункции печени имеется далеко не всегда, истинная распространенность этого заболевания в популяции неизвестна. Чаще больные обращаются к врачам по другим причинам, например по поводу артериальной гипертонии (АГ), желчнокаменной болезни, ишемической болезни сердца (ИБС), заболеваний периферических сосудов и др. [5, 6]. В связи с этим лечение назначается только больным с высоким риском прогрессирования НАЖБП или при наличии выраженных изменений биохимических показателей печени (повышение активности алани-наминотрансаминазы (АЛТ) и ас-партатаминотрансаминазы (АСТ) в крови в 2-3 раза и более).
МС обусловливает чрезвычайно высокий риск развития СД 2 типа, ИБС и других заболеваний, связанных с атеросклерозом 7, а также жировой болезни печени [2]. Среди механизмов поражения печени необходимо выделить нарушение синтеза и экскреции желчи в гепатоцитах, активацию перекисного окисления липидов (ПОЛ), угнетение активности ретикуло-эндотели-альной системы печени. В литературе представлены многочисленные данные о возможных патогенетических механизмах повреждения печени при МС, а также о роли печени в развитии и прогрессировании МС. Печень является единственным органом, где осуществляется синтез желчных кислот. Накопление в печени свободных жирных кислот приводит к нарушению проницаемости клеточных мембран, в том числе для глюкозы, к нарушению утилизации глюкозы гепатоцитами, что способствует повышению резистентности тканей к инсулину и поддержанию гипергликемии. В условиях инсулинорезистент-ности происходит накопление ли-пидов в печени и синтез большого количества липопротеидов очень низкой плотности (ЛПОНП), которые быстро модифицируются в липопротеиды низкой плотности (ЛПНП) и, окисляясь под действием свободных радикалов, являются ведущим фактором развития атеросклероза [7, 10, 11]. Увеличение концентрации холестерина (ХС) в клетках приводит к изменению состава, физических свойств и функций клеточных мембран: рецепторно-опосредованного эндоцитоза, реактивности мемб-раносвязанных ферментов, проницаемости мембран для ионов и метаболитов. Сохранение определенной концентрации ХС плазматических мембран обеспечивает необходимое постоянство физических свойств и физического состояния бислоя мембран нормально функционирующей клетки, что лежит в основе холестеринового гомеостаза и поддерживается равновесием поступления и выведения ХС из организма.
Эта цель определяет основные задачи терапии: нормализацию массы тела с помощью диеты и физических нагрузок; отмену гепа-тотоксичных препаратов; нормализацию показателей углеводного, липидного и пуринового обмена; увеличение содержания в гепато-цитах аминокислот, необходимых для синтеза апопротеинов, и ко-ферментов для синтеза ЛПОНП; уменьшение эндотоксемии; нормализацию активности процессов ПОЛ; выведение токсических метаболитов; ингибирование воспаления в ткани печени и т.д.
Таблица 1. Динамика показателей биохимического анализа крови у больных первой группы (принимавших таурин (Дибикор))
Что такое таурин, преимущества его приема и побочные эффекты
Обнаружив таурин в ингредиентах своего энергетического напитка, вам может быть интересно, что это такое и для чего именно. В отличие от других ингредиентов в этой банке, это не какое-то страшное химическое вещество, а аминокислота.
Что такое таурин?
Откуда берётся таурин?
Таурин естественным образом присутствует в организме, но его также можно найти в обычных продуктах животного происхождения. Самый высокий уровень таурина в пище содержится в мясе, рыбе и молочных продуктах.
Считается, что таурин является незаменимы в рационе человека, организм поддерживает свои собственные запасы и пополняет их получая его из пищи. Плохое здоровье часто связано с низким уровнем таурина, что делает его ключевой аминокислотой. Его уровень также снижается с возрастом, что означает, что он может играть роль в старении.
Источники таурина
• Таурин в больших количествах содержится во многих мясных продуктах, таких как говядина, курица из темной птицы или индейка.
• Высокий уровень таурина содержится в некоторых моллюсках и морепродуктах, таких как гребешки, осьминоги и моллюски.
• Меньшее количество таурина содержится в других мясных продуктах, таких как свинина, а также в других видах рыбы и молочных продуктах.
• Он часто является ключевым ингредиентом энергетических напитков из-за его роли во многих физиологических процессах.
• Поскольку таурин естественным образом содержится во многих продуктах животного происхождения, его часто добавляют в веганские и вегетарианские диеты.
Что она делает?
Таурин играет роль во многих функциях мышечных клеток, связанных с перемещением ионов кальция, а также в процессе преобразования АТФ, молекул энергии клетки, которые преобразуются в энергию.
Он также помогает стабилизировать клеточные элементы против окисления (процесс защиты клеток от повреждения свободными радикалами), регулировать баланс жидкости и стимулировать гликолиз и гликогенез (энергетические процессы).
Проще говоря, таурин участвует во многих процессах, связанных с использованием энергии и функцией мышц. По этой причине ученые восхищены всеми возможными эффектами таурина на упражнения и работоспособность.
Преимущества таурина
Таурин влияет на здоровье.
Таурин считается нутрицевтиком из-за его различных эффектов для здоровья, включая лечение мышечной усталости и утомления, а также улучшение иммунной функции.
Может повлиять на мышцы и работоспособность.
Предлагаемые преимущества добавок таурина связаны с его влиянием на работоспособность и мышечную ткань. В одном исследовании изучалась эффективность бега с добавлением таурина, но значительного улучшения не наблюдалось. Однако повышенный уровень таурина после тренировки приводил к более быстрому восстановлению и снижению окислительного стресса в мышечной ткани.
Может улучшить эффективность тренировок.
Недавние исследования показали значительное улучшение показателей выносливости с помощью всего одной дозы таурина. Значит, что и бодибилдеры и спортсмены, занимающиеся тренировками на выносливость, после приема дозы таурина могут повысить свою производительность. Другое исследование показало, что мышцы способны выдерживать большую нагрузку перед сокращением, а значит выдерживать больший стресс в течение более длительных периодов времени.
Таурин обладает огромным потенциалом для восстановления после подъема тяжестей за счет снижения окислительного стресса после тренировки. Хотя вышеупомянутое исследование не показало значительного улучшения беговой производительности, испытуемые показали небольшое увеличение скорости и снижение частоты сердечных сокращений, что свидетельствует о том, что они работали более эффективно после приема добавок.
Действует как антиоксидант и улучшает регенерацию.
Таурин действует как мощный антиоксидант, который также улучшает реакцию организма на регенерацию. Таким образом, он может действовать двумя способами: предотвращать повреждения и стресс во время упражнений, а также ускорять восстановление мышц после. Поскольку таурин является обычным ингредиентом энергетических напитков, часто считалось, что таурин необходим для эргогенности в сочетании с кофеином, но исследование с использованием одного таурина все же показало положительный эффект.
Исследования в области добавок таурина все еще новы и ограничиваются исследованиями, в которых изучались разные группы спортсменов в разных дисциплинах и условиях. По этой причине следует более тщательно изучить многообещающие эффекты таурина, чтобы лучше посоветовать спортсменам, как сделать его еще более полезной добавкой.
Безопасность, дозировка и побочные эффекты добавок
Безопасность
Никакие исследования не показали отрицательных побочных эффектов от приема таурина, но любая добавка может повлиять на другие лекарства или ваше здоровье.
Перед приемом любой новой добавки лучше всего проконсультироваться с врачом.
Дозировка
В исследовании, которое показало пользу таурина на выносливость, были разные рекомендации, варьирующиеся от 1 до 6 граммов на дозу.
Из-за его присутствия во многих продуктах животного происхождения вегетарианцам или веганам может потребоваться в больших количествах. Таурин также может показать больший эффект у людей, которые функционируют с оптимальным уровнем таурина, а затем начинают его принимать.
Побочные эффекты
Побочные эффекты от приема таурина в рекомендуемых дозах неизвестны. Никакие отрицательные эффекты передозировки энергетических напитков не позволили выявить проблемы с таурином, потому что в этих напитках очень много других ингредиентов.
Резюме
Таурин в лечении неалкогольной жировой болезни печени
Л. А. Звенигородская, Т. В. Нилова
Московский клинический научно-практический центр Проведено двойное слепое плацебоконтролируемое клиническое исследование, в котором оценивалась клиническая эффективность таурина у больных с неалкогольной жировой болезнью печени (НАЖБП) и сахарным диабетом типа 2 (СД2).
Результаты показали, что препарат влияет на обмен липидов и углеводов, а также является типичным гепатопротектором.
Ключевые слова: неалкогольная жировая болезнь печени, таурин, комплексное медикаментозное лечение
Taurine in non-alcoholic fatty liver disease treatment
L. A. Zvenigorodskaya, T. V. Nilova
Moscow Clinical Scientific and Practical Center In double-blind, placebo-controlled clinical trial taurine clinical efficacy in patients with non-alcoholic fatty liver disease and diabetes mellitus type 2 was evaluated.
The results of this study have shown effects of taurine on lipid and carbohydrate metabolism and also that taurine is a typical hepatoprotector.
Key words: non-alcoholic fatty liver disease, taurine, complex conservative prevention
Патогенез неалкогольной жировой болезни печени. Подходы к лечению
Неалкогольная жировая болезнь печени (НАЖБП) в настоящее время признана самым распространенным в популяции заболеванием и представляет собой поражение печени, включающее жировую дистрофию с воспалением и повреждением гепатоцитов – неалкогольным стеатогепатитом (НАСГ) и фиброзом с возможностью перехода в цирроз. НАЖБП в 75 % случаев протекает на фоне ожирения, дислипидемии, артериальной гипертонии, сахарного диабета типа 2 (СД2) или нарушением толерантности к глюкозе [1–3]. Указанные патологические процессы являются факторами риска сердечно-сосудистых заболеваний и атеросклероза. В патогенезе немаловажную роль играет нарушение микрофлоры толстой кишки и, как следствие, повышение содержания продуктов жизнедеятельности микроорганизмов (короткоцепочечные жирные кислоты, эндотоксин, оксид азота) [4–6]. Биопсия печени – наиболее специфичный и чувствительный диагностический метод выявления заболевания; когда нет возможности провести пункционную биопсию печени, для раннего выявления воспаления при НАЖБП можно использовать определение маркеров воспаления – оксида азота и эндотоксина [7].
В настоящее время для лечения больных НАЖБП используют препараты, сочетающие в себе антиоксидантную защиту, стабилизацию мембран гепатоцитов, противовоспалительную терапию [8].
Терапия НАЖБП включает следующие группы препаратов:
Надо отметить, что в терапии НАЖБП недооцененным остается таурин. Между тем, представляя собой естественный метаболит, таурин обладает гепатопротекторным, антиоксидантным, гиполипидемическим и гипогликемическим эффектами.
Общие сведения
Таурин – жизненно необходимая сульфоаминокислота, являющаяся конечным продуктом обмена серосодержащих аминокислот (метионина, цистеина, цистеамина) [9, 10]. Молекула таурина состоит из 2 атомов углерода, сульфоновой группы (SO3H) и аминогруппы (NH2). Биологический синтез таурина недостаточен для поддержания у человека тех биохимических процессов, в которых он задействован. Основным источником таурина являются мясные и рыбные продукты. При дефиците таурина в питании или в результате каких?либо иных причин (ишемия, сахарный диабет, стресс, травма и др.) страдают все виды обмена веществ любой клетки любого органа. Например, недостаточность таурина в печени ведет к нарушению желчевыделения, образованию камней, изменению обмена холестерина и липидов. Известно, что таурин, соединяясь с холевой кислотой, участвует во всасывании жиров и жирорастворимых витаминов.
Таурин может соединяться с атомом хлора, источник которого – гипохлорная кислота нейтрофилов. В этом виде таурин служит окислителем и является компонентом в борьбе против бактериальной инфекции. В митохондриях хлораминотаурин влияет на сборку белков дыхательной цепи и проявляет свойства антиоксиданта. Это же соединение таурина с хлором уменьшает воспалительный сигнал в клетках животных через ингибирование активации нуклеарного фактора k-би. В свободном виде таурин также выполняет жизненно важные для животной клетки функции – регуляцию осмотического давления и ионов кальция.
Роль таурина в физиологии печени
Таурин участвует в регуляции желчевыделения. Как мы помним, первичные желчные кислоты (холевая и хенодезоксихолевая) синтезируются в гепатоцитах печени из холестерина. Вторичные желчные кислоты (дезоксихолевая, литохолевая, урсодезоксихолевая, аллохолевая и др.) образуются из первичных желчных кислот в толстой кишке. В желчи желчного пузыря желчные кислоты присутствуют главным образом в виде конъюгатов – парных соединений с глицином и таурином. Продуктом конъюгации желчных кислот с таурином являются таурохолевая, таурохенодезоксихолевая и тауродезоксихолевая кислоты. Конъюгация желчных кислот обеспечивает их устойчивость в отношении выпадения в осадок при низких значениях рН в желчных протоках и двенадцатиперстной кишке. Важнейшая роль желчных кислот в пищеварении заключается в том, что с их помощью происходит всасывание целого ряда гидрофобных веществ: холестерина, жиров, жирорастворимых витаминов, растительных стероидов. При отсутствии желчных кислот всасывание вышеперечисленных компонентов пищи практически невозможно.
Поступление в кишечник таурохолевой кислоты снижает количество E. coli в слепой кишке [11]. Кроме того, тауроконъюгаты желчных кислот обладают холеретическим действием и предупреждают холестаз в отличие от желчных кислот, конъюгированных с глицином [12, 13]. В эксперименте in vitro гликолитохолевая кислота легко осаждается кальцием, чего не наблюдается с тауролитохолевой кислотой [14]. Таким образом, таурин необходим для повышения текучести желчи, увеличения продукции желчных кислот и предупреждения холестаза [15, 16].
При диффузных заболеваниях печени таурин увеличивает кровоток, улучшает микроциркуляцию и уменьшает выраженность цитолиза [1]. Показана его эффективность в отношении влияния на углеводный и липидный обмен. Антиоксидантное, гипогликемирующее, детоксицирующее действие таурина и его способность к выведению холестерина дает возможность применять его для лечения НАЖБП. На фоне приема таурина при хронической сердечной недостаточности больные отмечают исчезновение одышки, чувствуют прилив сил, увеличение трудоспособности, улучшение общего состояния. У больных с артериальной гипертонией препарат умеренно снижает артериальное давление (АД), при сахарном диабете (CД) уменьшает инсулинорезистентность, защищает b-клетки поджелудочной железы, оказывает гипогликемическое действие, не вызывая при этом гипогликемии.
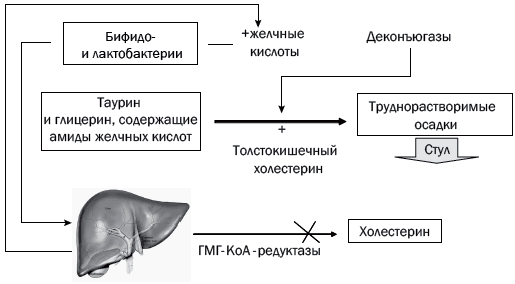
Рис. 1. Схема выведения холестерина
Взаимодействие желчных кислот и энтеробактерий
В процессах деконъюгации комплексов желчных кислот с таурином и глицином активно участвуют ферменты различных бактерий. В норме дезоксихолевая и хенодезоксихолевая кислоты при участии секреторного IgA, влияющего на антимикробную активность этих кислот, подавляют рост патогенных и условно-патогенных микроорганизмов даже в физиологических концентрациях [18]. При нарушении энтерогепатической циркуляции желчных кислот создается их значительный дефицит в кишечнике. В тонкой кишке недостаток желчных кислот изменяет работу всего пищеварительно-транспортного конвейера, способствует развитию нарушений всасывания и переваривания пищи – синдрома нарушенного пищеварения. В толстой кишке нехватка желчных кислот (помимо многочисленных метаболических нарушений) приводит к снижению «стерилизующих» и нутритивных свойств желчи. В результате – прогрессирование дисбиоза в толстой кишке, брожение, дисфункция баугиниевой заслонки и усиление микробной контаминации тонкой (подвздошной) кишки, с одной стороны, с другой – поступление через систему воротной вены с кровью в печень повышенного количества эндотоксина грамотрицательной микрофлоры. Важным и крайне необходимым условием восстановления энтерогепатической циркуляции желчных кислот является нормализация процессов синтеза желчи в печени и адекватного поступления ее в кишечник (табл. 1) [19]. Желчегонные свойства таурина в связи с этим также могут оказывать дополнительный эффект при лечении НАЖБП.
Таблица 1. Показатели обмена веществ у пациентов до начала исследования
| Показатель | Значение нормы | Первая группа, принимавшая таурин | Вторая группа, принимавшая плацебо |
| Белок | 66–87 г/л | 73,69±1,19 | 74,10±1,33 |
| Билирубин | 3,4–21 мкмоль/л | 15,39±1,84 | 18,14±1,98 |
| Глюкоза | 4,1–6,4 ммоль/л | 7,33±0,45 | 7,14±0,36 |
| АЛТ | 5–34 Ед/л | 51,48±8,90 | 37,33±10,84 |
| АСТ | 5–31 Ед/л | 39,13±6,53 | 31,67±5,47 |
| ЩФ (щелочная фосфатаза) | 30–120 Ед/л | 80,70±4,7 | 79,50±5,26 |
| ГГТП | 7–38 Ед/л | 67,86±17,56 | 52,91±6,35 |
| Мочевина | 1,7–8,3 ммоль/л | 5,22±0,39 | 5,23±0,47 |
| Холестерин | 1,4–5,2 мкмоль/л | 7,27±0,33 | 6,18±0,27 |
| ХС-ЛПНП | 2,1–3,3 мкмоль/л | 4,70±0,23 | 3,97±0,26 |
| ХС-ЛПВП | 1,1–2,3 ммоль/л | 1,37±0,12 | 1,27±0,10 |
| ТГ | 0,0–1,7 мкмоль/л | 2,43±0,21 | 2,01±0,09 |
| СРБ | мг/л | 7,23±0,30 | 7,56±0,50 |
Целью исследования было изучение фармакодинамических показателей метаболитов оксида азота (NO) и бактериального эндотоксина в результате трехмесячного курса фармакотерапии таурином у больных НАЖБП и СД2, сопоставление содержания оксида азота и эндотоксина у больных НАЖБП с СД2 с биохимическими показателями крови.
Материал и методы
В двойное слепое плацебо-контролируемое исследование было включено 40 больных, страдающих НАЖБП и СД2 (30 женщин и 10 мужчин), средний возраст которых составил 56,35±8,75 года. Верификацию диагноза проводили по данным клинических, биохимических, инструментальных методов исследования. Индекс массы тела больных был увеличен на 30–35 %, у некоторых – до 40 %. Все больные получали терапию по поводу сахарного диабета метформина гидрохлоридом, по поводу артериальной гипертензии – амлодипином и эналаприлом. Методом случайных чисел пациентов разделили на 2 группы. 1-я группа получала таурин (Дибикор, ООО «ПИК-ФАРМА») в дозе 0,5 г 2 раза в день за 20 мин до еды в течение 3 мес. 2-я, контрольная, группа дополнительно к основному лечению получала плацебо-таурин.
Уровень метаболитов оксида азота в сыворотке крови определяли экспресс-методом для биологических жидкостей с использованием ванадия хлорида (Германия) [20]. Уровень эндотоксина определяли ЛАЛ-тестом (США). Статистическую обработку данных проводили с использованием программы «Биостат».
Результаты
У больных НАЖБП отмечено повышение аминотрансфераз АЛТ и АСТ, а также гамма-глютамилтранспептидазы (ГГТП) у 35 больных. По показателям липидного спектра у обследованных больных также наблюдалось повышенное содержание общего холестерина, холестерина ЛПНП и триглицеридов (см. табл. 1). Как видно из таблицы, по некоторым показателям группы отличались. Повышение АСТ и АЛТ, а также общего холестерина и триглицеридов было более выражено в 1-й группе, билирубина и С-реактивного белка (СРБ) – во 2-й. По данным УЗИ выявлена жировая дистрофия печени у всех больных.
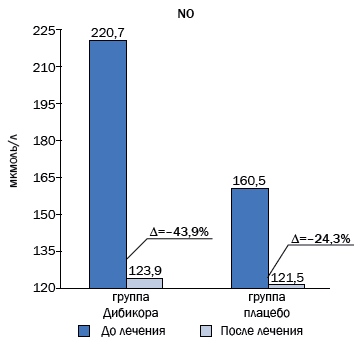
Уровень метаболитов оксида азота в 1-й группе до лечения был увеличен в 6,8 раза и составлял 220,70±14,27 мкмоль/л. Норма – 32,15±0,51 мкмоль/л (p=0,001). Во 2-й группе, получавшей плацебо, уровень метаболитов был несколько ниже, составил 160,50±8,87 мкмоль/л и был увеличен в 5 раз. В результате фармакотерапии таурином содержание метаболитов снизилось на 44 %, или на 97 мкмоль/л. В группе контроля (плацебо) снижение метаболитов оксида азота составило 25 %, или 39 мкмоль/л.
У больных НАЖБП уровень эндотоксина был увеличен в 7 раз (n=34) (норма – 0,29±0,05 Е/Эмл) и составлял 2,20±0,04 Е/Эмл. В результате проведения курса лечения с включением таурина содержание эндотоксина снизилось до 0,90±0,01 Е/Эмл (p=0,001). В группе плацебо (вторая группа) изменения были также статистически значимы, уровень эндотоксина достиг 1,80±0,05 Е/Эмл. Фармакотерапия больных НАЖБП с включением таурина снижает активность маркеров воспаления.
Достоверное увеличение продукции сывороточного эндотоксина сопровождалось ростом синтеза оксида азота и находилось в прямой корреляционной зависимости (коэффициент корреляции равен 0,625.) Лечение таурином сопровождалось улучшением биохимических показателей крови, улучшением общего самочувствия больных. Уровень метаболитов оксида азота снижался параллельно уровню АЛТ, АСТ и ГГТП. Изменения показателей обмена веществ приведены в табл. 2.
Таблица 2. Изменения показателей обмена веществ после курса лечения в группах таурина и плацебо, %
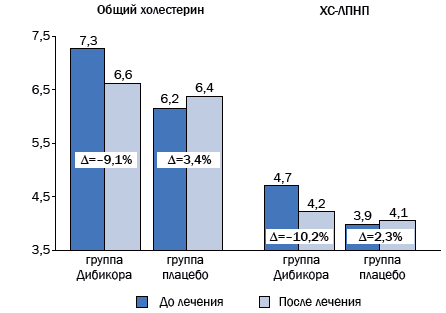
При данной выборке пациентов достоверно статистические изменения (снижение) наблюдали в 1-й группе по показателям АСТ, АЛТ, ГГТП. Остальные изменения были недостоверны. Наблюдалось достоверное снижение веса с 91,32±3,5 до 87,42±3,06; p=0,001. Во 2-й группе наблюдалась тенденция ухудшения – возрастание ЩФ, уровня гликемии, общего холестерина, ХС-ЛПНП. В 1-й группе ХСЛПВП не изменился, во 2-й – вырос на 17,3 %.
Рис. 2. Снижение уровня метаболитов NO на фоне фармакотерапии таурином и плацебо
Рис. 3. Динамика липидного спектра крови после 3-месячного курса терапии таурином
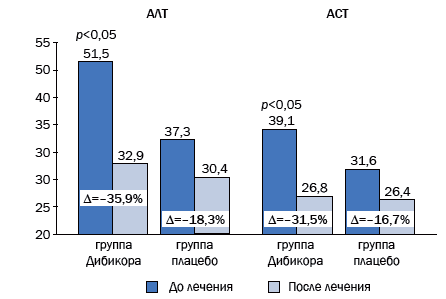
Рис. 4. Динамика показателей биохимического анализа крови у больных, получавших таурин
Обсуждение
Показано, что в 1-й и 2-й группах после лечения наблюдаются положительные изменения со стороны печеночных ферментов. Присоединение к терапии НАЖБП препарата Дибикор (таурин) способствует более выраженному уменьшению активности ферментов печени: АСТ (p
Литература