Что лучше тербинафин или пимафуцин
Кандидозный вульвовагинит
В последние годы отмечается значительный рост и распространение вульвовагинального кандидоза. Распространение эндокринной патологии, растущая частота антибиотикотерапии, назначения цитостатиков в повседневной врачебной практике, широкое применение гормо
В последние годы отмечается значительный рост и распространение вульвовагинального кандидоза. Распространение эндокринной патологии, растущая частота антибиотикотерапии, назначения цитостатиков в повседневной врачебной практике, широкое применение гормональных методов контрацепции, использование вагинальных тампонов, гигиенических прокладок — все это предрасполагает к заболеваниям нижних отделов половой системы, обусловленных дрожжеподобными грибами рода Candida. 75–80% женщин переносят в течение жизни хотя бы один эпизод вульвовагинального кандидоза, а у 40–45% развивается по крайней мере один рецидив. 5% женщин во всем мире страдают рецидивирующим вульвовагинальным кандидозом, для которого характерно три или более эпизодов обострения инфекции в течение года. В связи с широкой рекламой в средствах массовой информации разнообразных антимикотических средств, их доступностью в аптечной сети в настоящее время весьма распространено самолечение, которое приводит к длительно текущим рецидивирующим формам вульвовагинального кандидоза из-за применения однократных коротких курсов терапии [1–8].
В 54–76% случаев возбудителем вульвовагинального кандидоза является Candida albicans, в других случаях обнаруживают C. glabrata, C. tropicalis, C. guillermondii, C. parapsilosis, C. kefir [1–8].
Выделим три основных фактора защиты макроорганизма, препятствующих развитию вульвовагинального кандидоза.
– фагоцитозом, осуществляемым макрофагами и нейтрофилами;
– Т-лимфоцитами разных популяций;
– антителами — иммуноглобулинами всех классов.
Основная роль антител в защите от инфекции заключается в блокировании Candida рецепторов и литических ферментов возбудителя.
К развитию вульвовагинального кандидоза может приводить изменение гормонального фона за счет: повышения содержания гликогена в эпителиоцитах; сдвигов рН; прямого стимулирующего действия эстрогенов на рост грибов, повышения авидности вагинального эпителия к грибам, что способствует их лучшей адгезии; угнетения механизмов иммунной защиты.
Так, во время беременности вульвовагинальный кандидоз развивается в 30–40% случаев, что обусловлено изменениями гормонального баланса во время беременности, накоплением гликогена в эпителиальных клетках в связи с увеличением количества эстрогенов, иммуносупрессивным действием высокого уровня прогестерона в сыворотке крови.
Другим примером может являться использование контрацептивов с большим количеством эстрогенов, которые повышают эффективность связывания дрожжеподобных грибов с эпителиальными клетками влагалища.
Одним из основных факторов риска является антибиотикотерапия, причем не только пероральное и парентеральное применение препаратов, но и местное их использование.
Различные состояния, приводящие к угнетению иммунной системы макроорганизма, например гиповитаминозы, хронические заболевания, травмы, операции, прием антибиотиков, цитостатиков, лучевая терапия, также могут способствовать развитию вульвовагинального кандидоза.
Некоторые работы предрасполагают к экзогенному заражению грибами: на заводах по переработке овощей, фруктов, производству антибиотиков, белково-витаминных препаратов и других биологически активных веществ [5].
В развитии кандидозной инфекции выделяются следующие этапы:
При вульвовагинальном кандидозе псевдомицелий проникает в глубь эпителия. На этом уровне инфекция может персистировать длительное время, так как устанавливается динамическое равновесие между грибами, которые не могут проникнуть в более глубокие слои слизистой оболочки, и макроорганизмом, который сдерживает такую возможность, но не способен полностью элиминировать возбудитель. Нарушение этого равновесия приводит либо к обострению заболевания, либо к выздоровлению, либо к ремиссии.
Выделяют три формы вульвовагинального кандидоза.
Кандиданосительство. Жалоб и выраженной клинической картины заболевания нет. При микробиологическом исследовании в отделяемом влагалища обнаруживают в небольшом количестве почкующиеся формы дрожжеподобных грибов при отсутствии в большинстве случаев псевдомицелия. Кандиданосительство может переходить в клинически выраженную форму.
Острая форма вульвовагинального кандидоза. Длительность заболевания не превышает 2 мес. В клинической картине преобладают выраженные признаки местного воспаления вульвы: гиперемия, отек, выделения, зуд и жжение.
Хроническая форма вульвовагинального кандидоза. Длительность заболевания составляет более 2 мес, при этом на слизистых оболочках вульвы и влагалища выражены инфильтрация, лихенизация, атрофия.
В зависимости от состояния вагинального микроценоза классифицируют три формы Candida-инфекции влагалища.
В клинике патогномоничным симптомом вульвовагинального кандидоза являются творожистые налеты серо-белого цвета, с кислым запахом, точечные или 5–7 мм в диаметре, иногда сливающиеся между собой. Очаги резко отграничены, округлых или овальных очертаний, как бы вкраплены в слизистую оболочку вульвы и влагалища, налеты содержат массы размножающихся грибов Candida.
В острой стадии заболевания творожистые пленки «сидят» плотно, снимаются с трудом, обнажая эрозированную поверхность, в дальнейшем — легко. За счет их отторжения появляются густые беловатые творожистые выделения. Слизистая оболочка в области поражения имеет выраженную склонность к кровоточивости, а по периферии очага интенсивно гиперемирована.
Зуд чаще беспокоит больных во время менструации, после физических нагрузок. В некоторых случаях могут отмечаться чувство жжения, некоторая болезненность при мочеиспускании.
Резкая боль, жжение, как правило, беспокоят пациенток при половых контактах, что может приводить к формированию невротического синдрома.
Микроскопическое исследование позволяет определить наличие гриба, его спор, мицелия, количество лейкоцитов [1–8].
Для видовой идентификации гриба обязательно культуральное исследование. В настоящее время продолжаются разработки методов полимеразной цепной реакции, которые также позволят устанавливать видовую принадлежность.
Лечение показано только при наличии клинической картины заболевания, подтвержденной микроскопически и культурально.
Существующие лекарственные формы современных антимикотиков предполагают два пути проникновения препаратов в кровь: пероральный, со всасыванием в кишечнике, и внутривенный. При вульвовагинальном кандидозе преимущественно используется первый путь.
На всасывание препарата и на распределение его в организме во многом оказывает влияние растворимость. Так, флуконазол является водорастворимым и поэтому быстро и почти полностью всасывается, а в крови существует преимущественно в свободной форме. Последнее обусловливает хорошее распределение в жидких средах организма: содержание препарата в ликворе приближается к плазменной концентрации. Флуконазол слабо метаболизируется печенью и выводится почками, в основном в неизмененном виде, поэтому при снижении клубочковой фильтрации его выведение замедляется, и доза препарата при этом должна быть снижена.
Другие системные антимикотики, используемые в терапии вульвовагинального кандидоза, являются липофильными, они не растворимы в воде. Лучше всех в кишечнике всасывается тербинафин. Итраконазол и кетоконазол хорошо всасываются в кислой среде, поэтому у больных с ахлоргидрией абсорбция может оказаться сниженной.
Липофильные препараты в крови находятся преимущественно в несвободной, связанной с белками плазмы форме. Поэтому их содержание в разных жидких средах незначительно.
Липофильные препараты хорошо накапливаются в тканях, особенно богатых липидами, в частности в печени, селезенке, жировой ткани, в кожном сале. Это свойство, а также кератофильность (способность связываться с кератином эпидермиса) используются в лечении. Жировая ткань служит депо для липофильных ферментов: в ней они концентрируются и из нее медленно высвобождаются в кровь.
Интенсивной биотрансформации подвергаются все липофильные препараты. Быстрый метаболизм кетоконазола, итраконазола и тербинафина с эффектом первого прохождения через печень может существенно снижать их концентрации. Как правило, образующиеся метаболиты неактивны. Биотрансформация, происходящая при участии микросомальных ферментов печени, ускоряется препаратами — индукторами этих ферментов (например, рифампицином, дифенином). Выведение липофильных препаратов происходит с калом (азолы) и мочой (тербинафин), в виде метаболитов и реже в неизмененной форме.
В последние годы наиболее часто предлагаются схемы лечения с использованием флуконазола. Это препарат азольного ряда, с широким спектром противогрибкового действия, являющийся синтетическим производным бис-триазола. Как и другие препараты группы азолов, флуконазол угнетает образование эргостерола, основного компонента мембраны грибов, действуя на фермент 14-α-деметилазу, входящий в систему цитохрома P450. Нарушение биосинтеза мембраны обусловливает фунгистатический эффект препарата, а в ходе перекисного окисления и других процессов приводят к гибели клетки гриба. В отличие от других азольных препаратов флуконазол обладает высокой специфичностью по отношению к зависимым от цитохрома Р450 ферментам грибов. Поэтому при использовании флуконазола не наблюдается побочное действие на синтез стероидов и другие метаболические процессы, связанные с Р450. Среди грибов рода Candida наиболее чувствительными к флуконазолу являются C. albicans, а также C. tropicalis, C. parapsilosis, чувствительными считают штаммы C. krusei, в меньшей степени C. glabrata.
При лечении кандидоза следует учитывать вид возбудителя. Как правило, определять чувствительность к препарату до начала лечения кандидоза не требуется, если заболевание вызвано C. albicans. Устойчивость штаммов C. albicans может развиваться при хронических формах заболевании, у ВИЧ-инфицированных. При кандидозе, вызванном другими видами Candida, следует определить чувствительность до лечения.
Флуконазол растворим в воде, быстро и полностью всасывается в желудочно-кишечном тракте. В кровь попадает более 90% от принятой внутрь дозы. Одновременный прием пищи, а также желудочная кислотность не влияют на абсорбцию препарата. Концентрации в плазме напрямую зависят от дозы. Пиковые концентрации достигаются в течение 1–2 ч. Механизм действия флуконазола связан с нарушением образования эргостерина из ланостерина. Флуконазол ингибирует цитохром Р450-зависимые ферменты грибковой клетки. В настоящее время выпускается флуконазол в таблетках (Микофлюкан), капсулах и в виде раствора для внутривенных инфузий (Флюкостат).
При вульвовагинальном кандидозе показано применение флуконазола по 150 мг перорально однократно. При рецидивирующей форме заболевания флуконазол назначают перорально 150 мг с повторным назначением через 3 дня, затем флуконазол назначают по 150 мг в неделю перорально в течение 6 мес.
У беременных оправдано применение натамицина (Пимафуцин). Натамицин — противогрибковый антибиотик из ряда полиенов-макролидов, продуцируемый актиномицетом Streptomyces natalensis. Механизм действия препарата сходен с таковыми у других полиеновых антибиотиков: натамицин связывается с эргостеролом, нарушая проницаемость мембраны. Вагинальные свечи Пимафуцин назначаются на ночь, в течение 3–6 сут. Исследования подтвердили высокую эффективность и надежность Пимафуцина при лечении беременных
При остром вульвовагинальном кандидозе могут быть использованы местные формы азоловых препаратов: клотримазол в виде вагинальных таблеток по 100 мг на ночь интравагинально глубоко в течение 6 дней; эконазол в виде суппозиториев интравагинально глубоко в течение 14 дней на ночь [4]; итраконазол — вагинальные таблетки 200 мг — интравагинально глубоко в течение 10 дней [3].
Ко многим из существующих местных препаратов для лечения вульвовагинального кандидоза в настоящее время нередко развивается резистентность [6–8].
Основные механизмы устойчивости грибов связаны с тем, что:
В исследованиях in vitro было показано, что существует синергизм между некоторыми антимикотическими препаратами, позволяющий преодолеть проблему перекрестной резистентности. В результате исследования этих взаимодействий стало возможным создание принципиально нового антимикотического препарата — сертаконазола. Сертаконазол — противогрибковый препарат нового поколения «двойных классов». Препарат содержит два синергичных класса в одной молекуле: азоловую и бензотиафеновую группу. Сертаконазол обладает фунгицидным, фунгистатическим действием, блокирует диморфную трансформацию грибов, обладает широким спектром действия, характеризуется высокой комплаентностью. При этом имидазоловая часть молекулы обеспечивает нарушение биосинтеза эргостерола, вмешательство на уровне цитохром Р450-зависимого фермента 14а, ингибирует рост грибов, обеспечивает фунгистатический механизм. Бензотиафеновая структура замещает триптофан в мембране гриба, что приводит к разрушению и гибели гриба, т. е. осуществляется фунгицидное действие. Местное использование сертаконазола (суппозитории Залаин) позволяет повысить эффективность терапии вульвовагинального кандидоза. Схема лечения предусматривает однократное назначение препарата.
При необходимости (выраженности субъективных ощущений, снижения дозы препарата из-за беременности или сопутствующего заболевания и т. п.) антимикотическая терапия кандидозного вульвовагинита может быть дополнена неспецифическими средствами. К ним относятся: 10–20% раствор буры в глицерине, растворы марганцовокислого калия 1 : 5000, нитрата серебра 1 : 2000. Эти препараты не обладают ни фунгицидным, ни фунгистатическим свойством, а лишь способствуют максимальному удалению мицелиальных форм гриба из крипт влагалища, а также нарушению прикрепления гриба к стенке влагалища и торможению его размножения.
Поскольку нередко наблюдается сочетанная инфекция, обусловленная дрожжеподобными грибами и различными бактериями, в последние годы применяют комплексные препараты, к которым относится, в частности, Макмирор комплех (1 вагинальный суппозиторий содержит 10 г нифуратела и 200 000 ЕД нистатина).
При вульвовагинальном кандидозе Макмирор назначают по 1 свече перед сном в течение 10 дней. При применении препарата возможны местные аллергические реакции. Макмирор противопоказан при беременности и лактации.
Обоснована комбинация антимикотических средств с метронидазолом. Метронидазол обладает антибактериальным, противопротозойным, трихомонацидным действием, воздействует на простейшие грамотрицательные анаэробные бактерии, грамположительные анаэробные палочки и кокки, подавляя в них синтез ДНК и РНК, вызывая их деградацию. Вагинальные суппозитории Нео-пенотран содержат (1 доза) 100 мг миконазола и 500 мг метронидазола. Вагинальные таблетки Клион Д 100 (1 доза) содержат 100 мг миконазола и 100 мг метронидазола.
Литература
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
Современные методы лечения онихомикоза
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую з
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую заболеваемость онихомикозом, которая составила в общей популяции населения от 2 до 13 % [1, 2, 3]. Риск развития онихомикоза наиболее высок у больных старшего возраста. Например, у людей старше 70 лет распространенность онихомикоза стоп может составлять 50 % и выше [2, 4, 5]. Считается, что этому способствуют медленный рост ногтевых пластинок, нарушения периферического и магистрального кровообращения у лиц пожилого возраста [6]. Высокую частоту онихомикоза выявляют также у больных с иммунодефицитными состояниями (в том числе у больных СПИДом) и у больных сахарным диабетом [6, 7, 8].
Часто больные и некоторые врачи воспринимают онихомикоз как исключительно эстетическую проблему. Однако это серьезное заболевание, которое протекает хронически и в случаях возникновения иммунодефицитного состояния, декомпенсации эндокринных заболеваний может стать причиной развития распространенного микоза кожи и ее придатков. Нередко онихомикоз сопровождается развитием тяжелых осложнений, например диабетической стопы, хронического рожистого воспаления конечностей, лимфостаза, элефантиаза [9, 10]. У больных, получающих цитостатическую или иммуносупрессивную терапию, болезнь может стать причиной развития инвазивных микозов. Вот почему лечение онихомикоза является необходимым и должно проводиться своевременно [11].
Всего несколько десятилетий назад лечение онихомикоза было трудоемким, длительным и малоперспективным. Лекарственные препараты, применявшиеся для лечения грибковых заболеваний кожи и ее придатков, отличались низкой эффективностью и высокой токсичностью. Для достижения положительного результата требовалось длительное лечение или увеличение дозы препаратов, что нередко сопровождалось тяжелыми осложнениями. Некоторые методы лечения были потенциально опасны для жизни пациентов. Например, рентгенотерапия, применение таллия и ртути приводили к развитию у пациентов онкологических заболеваний кожи, заболеваниям головного мозга и внутренних органов.
Появление высокоэффективных и малотоксичных антимикотических препаратов значительно облегчило лечение грибковых заболеваний кожи и ее придатков. Однако результаты применения новых антимикотиков оказались недостаточно удовлетворительными. Контролируемые клинические испытания показали, что эффективность применения системных антимикотиков после окончания лечения составляет от 40 до 80 %, а через 5 лет — от 14 до 50 % [12]. В то же время эффективность терапии онихомикоза повышается при применении комплексных методов лечения, которые предусматривают использование этиотропных препаратов и средств, влияющих на звенья патогенеза [13]. Также в результате клинических испытаний, проведенных в странах Европы, было установлено, что эффективность лечения онихомикоза можно повысить в среднем на 15 % при сочетанном применении антимикотиков системного действия и антифунгального лака, содержащего аморолфин [14].
Лечение
Аллиламины являются синтетическими антимикотиками. Аллиламины преимущественно действуют на дерматомицеты, при этом они оказывают фунгицидное действие. Механизм их действия заключается в ингибировании фермента скваленэпоксидазы, которая принимает участие в синтезе эргостерола — основного структурного компонента клеточной мембраны дерматомицетов. К аллиламинам относятся тербинафин и нафтифин.
Аллиламины активны в отношении большинства дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp., Malassezia spp.), возбудителя хромомикоза и некоторых других грибов.
Показаниями для назначения тербинафина внутрь являются онихомикоз, распространенные формы дерматомикозов кожи, микоз волосистой части головы, хромомикоз. Показаниями для наружного применения тербинафина и нафтифина служат ограниченное поражение кожи при микозах, отрубевидный лишай, кандидоз кожи. Тербинафин обладает высокой биодоступностью, хорошо всасывается в ЖКТ независимо от приема пищи. В высоких концентрациях препарат накапливается в роговом слое кожи, ногтевых пластинках, волосах, выделяется с секретами потовых и сальных желез. Абсорбция тербинафина при местном применении составляет менее 5 %, нафтифина — 4–6 %. Концентрация тербинафина и нафтифина в коже и ее придатках значительно превышает МПК для основных возбудителей дерматомикозов. Коррекция режима дозирования тербинафина может потребоваться при сочетанном назначении его с индукторами (рифампицин) или ингибиторами микросомальных ферментов печени (циметидин), так как первые повышают его клиренс, а вторые его понижают.
В результате многочисленных контролируемых многоцентровых сравнительных клинических испытаний было установлено, что тербинафин является наиболее эффективным антимикотиком в терапии онихомикоза [12] (табл. 1).
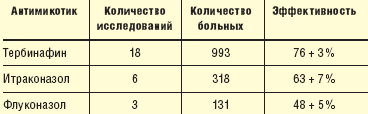 |
| Таблица 1. Сравнительная эффективность антимикотиков в терапии онихомикоза (по результатам метаанализа 27 рандомизированных исследований) |
Тербинафин применяют при распространенном поражении кожи, онихомикозе, хромомикозе, в таких случаях тербинафин назначают перорально. Тербинафин является препаратом выбора в терапии онихомикоза, так как наиболее эффективен по отношению к основных возбудителям онихомикоза — дерматомицетам. Противопоказаниями для назначения аллиламинов являются аллергические реакции на препараты группы аллиламинов, беременность, кормление грудью, возраст до 2 лет, заболевания печени, сопровождающиеся нарушением ее функции (повышением трансаминаз).
Азолы — самая многочисленная группа синтетических антимикотиков. В 1984 г. был внедрен в практику первый системный противогрибковый препарат из группы азолов — кетоконазол, в 1990 г. — флуконазол, в 1992 г. — итраконазол.
Азолы, применяемые в качестве системных препаратов, обладают преимущественно фунгистатической активностью. Важным преимуществом азолов перед другими препаратами является их широкий спектр противогрибковой активности. Итраконазол активен in vitro в отношении большинства возбудителей онихомикоза — дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.), Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), Aspergillus spp., Fusarium spp., S. Shenckii и др. Флуконазол активен против дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.) и Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), но не действует на Aspergillus spp., Scopulariopsis spp., Scedosporium spp.
Фармакокинетика у разных азолов различна. Флуконазол (90 %) хорошо всасывается в ЖКТ. Для хорошего всасывания итраконазола необходим нормальный уровень кислотности. Если у пациента, принимающего эти препараты, кислотность понижена, то всасываемость их уменьшается и, следовательно, снижается биодоступность. Всасываемость раствора итраконазола выше, чем у капсул с итраконазолом. Итраконазол в капсулах следует принимать с пищей, а в растворе — натощак.
Итраконазол метаболизируется в печени и выводится из организма через ЖКТ. В небольших количествах он также выделяется сальными и потовыми железами. Флуконазол метаболизируется частично и в основном выводится в неизмененном виде почками (80 %).
Итраконазол взаимодействует со многими лекарственными препаратами. Биодоступность кетоконазола и итраконазола уменьшается при приеме антацидов, холиноблокаторов, Н2-блокаторов, ингибиторов протонной помпы, диданозина. Итраконазол является активным ингибитором изоферментов цитохрома Р450 и может изменять метаболизм многих лекарственных препаратов. Флуконазол влияет на метаболизм лекарственных средств в меньшей степени. Недопустим прием азолов с терфенадином, астемизолом, цизапридом, хинидином, так как могут развиться смертельно опасные желудочковые аритмии. Совместный прием азолов и пероральных антидиабетических препаратов требует постоянного контроля за содержанием глюкозы в крови, так как может развиться гипогликемия. Прием непрямых антикоагулянтов группы кумарина и азолов может сопровождаться гипокоагуляцией и кровотечениями — следовательно, необходим контроль гемостаза. Итраконазол может повышать концентрацию в крови циклоспорина и дигоксина, а флуконазол — теофиллина и вызывать развитие токсического эффекта. Требуется корректировка доз и постоянный мониторинг за концентрацией препаратов в крови. Противопоказано совместное применение итраконазола с ловастатином, симвастатином, рифампицином, изониазидом, карбамазепином, циметидином, кларитромицином, эритромицином. Флуконазол не следует применять с изониазидом и терфенадином.
Итраконазол применяют при дерматомикозах (эпидермофитии, трихофитии, микроспории), отрубевидном лишае, кандидозе кожи, ногтей и слизистых оболочек, пищевода, кандидозном вульвовагините, криптококкозе, аспергиллезе, феогифомикозе, споротрихозе, хромомикозе, эндемичных микозах, для профилактики микозов при СПИДе.
Флуконазол применяется для лечения генерализованного кандидоза, всех форм инвазивного кандидоза, в том числе и у иммуноскомпрометированных больных, генитального кандидоза, кандидоза кожи, ее придатков и слизистых. Последнее время благодаря своей безопасности и хорошей переносимости все чаще флуконазол применяется для терапии больных дерматомикозами с поражением как кожи, так и ее придатков (ногтей и волос).
Аморолфин входит в состав лака, применяемого для лечения онихомикоза. Механизм действия аморолфина заключается в нарушении синтеза эргостерола — основного компонента клеточной мембраны гриба. Он оказывает фунгистатическое и фунгицидное действие. Обладает широким спектром действия. Концентрация аморолфина в ногтевой пластинке значительно превышает МПК для основных возбудителей дерматомикозов в течение 7 дней. Поэтому аппликация препарата может осуществляться не чаще 1–2 раз в неделю, что делает его применение экономически выгодным. Противопоказания: аллергические реакции на аморолфин, грудной и детский младший возраст. Лак в качестве монотерапии назначают при поражении не более 1–3 ногтевых пластинок и не более чем на 1/2 по площади с дистального конца. Также аморолфин можно использоваться в сочетании с системными антимикотиками при более распространенном поражении ногтей (табл. 2).
Циклопирокс обладает фунгистатическим действием. Активен в отношении дерматомицетов, дрожжеподобных и мицелиальных грибов, плесеней, а также некоторых грамотрицательных и грамположительных бактерий. Циклопирокс (лак) применяется в качестве монотерапии при поражении не более 1–3 ногтевых пластинок не более чем на 1/2 по площади с дистального конца. Также циклопирокс можно использовать в сочетании с системными антимикотиками при более распространенном поражении ногтей. Противопоказания: аллергические реакции на циклопирокс, грудной и младший детский возраст, беременность и лактация.
Перечень рекомендуемых лабораторных исследований при назначении системных антифунгальных препаратов.
Лечение фоновых заболеваний. Эффективность применения антимикотиков повышается при коррекции патологических состояний, способствовавших развитию онихомикоза. Перед началом антимикотической терапии у больных с соматическими, эндокринными, неврологическими заболеваниями, с нарушениями кровообращения в конечностях необходимо провести обследование для выявления основного симптомокомплекса, способствовавшего развитию дерматомикозов. Так, основными задачами патогенетической терапии являются улучшение микроциркуляции в дистальных отделах конечностей, венозного оттока конечностей, нормализация уровня тиреотропных гормонов у больных с заболеваниями щитовидной железы, углеводного обмена у больных сахарным диабетом и т. д. В результате многолетних исследований, проведенных в Военно-медицинской академии и Санкт-Петербургской медицинской академии последипломного образования, установлено, что одной из основных причин развития дерматомикозов являются нарушения со стороны системы гипофиз–гипоталамус–гонады. Это приводит к расстройству кровообращения в дистальных отделах конечностей, нарушениям микроциркуляции, периферической иннервации. Комплекс мероприятий, направленный на коррекцию этих нарушений, включает иглорефлексотерапию, транскраниальную электростимуляцию подкорковых центров головного мозга, назначение препаратов, корригирующих работу симпатической и парасимпатической вегетативной нервной системы. Все это позволяет добиться более быстрого клинического эффекта при терапии дерматомикозов. Проведение патогенетической терапии у больных дерматомикозами с фоновыми заболеваниями целесообразно назначать до начала этиотропного лечения и продолжать ее во время всего курса приема антифунгальных препаратов.
Симптоматическая терапия дерматомикозов, направленная на уменьшение субъективных жалоб больных и объективных проявлений заболевания, не может заменить этиотропную терапию. Однако ее применение в сочетание с антифунгальными препаратами позволяет быстрее добиться улучшения состояния больных, уменьшить чувство дискомфорта и устранить косметический дефект. При онихомикозах наибольшее беспокойство больным доставляют деформированные, значительно утолщенные (гипертрофированные) ногтевые пластинки — онихогрифоз. Для коррекции этого состояния применяют аппаратный педикюр. С помощью аппарата, напоминающего стоматологическую турбину, за короткий промежуток времени механическим путем удаляются измененные участки ногтей, гиперкератотические, роговые массы с кожи, омозолелости. При этом не происходит травматизации матрикса ногтя, и пациент после процедуры остается работоспособен.
При ограниченном поражение ногтей (не более 3 ногтевых пластинок и не более чем на 1/2 по площади с дистального края) применяются препараты для местного применения. Лечение рекомендуется начинать с подчистки пораженного участка ногтевой пластинки при помощи набора «Микоспор», аппаратного педикюра или кератолитических средств. Далее на пораженную ногтевую пластинку наносятся антифунгальные препараты. Раствор аморолфина, содержащий циклопирокс, наносится на ногтевую пластинку 1–2 раза в неделю. Перед нанесением лака не нужно предварительно очищать ногтевую пластинку от предыдущих слоев препарата. Лак наносится ежедневно до полного отрастания здоровой ногтевой пластинки. На 7-й день ногтевая пластинка очищается с помощью любого косметического средства для снятия лака. В литературе встречаются противоречивые сообщения об эффективности этого метода лечения. Указывается процент излеченности больных от 5–9 до 50 %.
При распространенном поражении ногтевых пластинок на пальцах кистей комплекс лечебных мероприятий должен включать назначение системного антимикотика, подчистку ногтей и наружную терапию антифунгальными препаратами. С целью профилактики повторного заражения необходимо обработать перчатки больного, подвергнуть дезинфекции предметы личной гигиены (мочалки, полотенца, пилочки для ногтей, терки и скребки для обработки кожи и ногтей).
Препаратом выбора при лечении онихомикоза любой локализации является тербинафин. Его назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 6 нед. Детям от 2 лет весом менее 20 кг тербинафин назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 6 нед. Препаратами резерва являются средства, содержащие итраконазол и флуконазол. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой и пятой неделях с начала терапии. Для лечения онихомикозов у детей итраконазол не назначается. Флуконазол рекомендуется принимать по 150 мг 1 раз в неделю в течение 3–6 мес.
Проведение комплексной терапии, состоящей из приема системного антимикотика, подчистки ногтей, местного применения антифунгальных препаратов, а также противоэпидемиологические мероприятия, обеспечивают высокую эффективность излечения онихомикоза стоп. Тербинафин назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 12 и более недель. Детям от 2 лет весом менее 20 кг препарат назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 12 нед. Флуконазол рекомендуется применять по 150–300 мг 1 раз в неделю в течение 6–12 мес. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой, пятой и девятой неделях. При поражении больших пальцев стоп рекомендуется проводить 4-й курс пульс-терапии на тринадцатой неделе от начала терапии. Для лечения онихомикозов у детей итраконазол не применяется.
Критериями микологической излеченности онихомикоза являются отрицательные результаты микроскопического и культурального исследования ногтевой пластинки. После окончания лечения итраконазолом и тербинафином здоровые ногтевые пластинки отрастают не полностью, поэтому полное клиническое выздоровление можно наблюдать только спустя 2–4 мес после окончания приема антифунгальных препаратов.
Литература
Л. П. Котрехова, кандидат медицинских наук, доцент
К. И. Разнатовский, доктор медицинских наук, профессор
Н. Н. Климко, доктор медицинских наук, профессор
СПбМАПО, Санкт-Петербург