Что лучше ципролет или норфлоксацин
Современные подходы к терапии хронического бактериального простатита
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу урологических проблем среди мужчин в возрасте от 20 до 50 лет. Для получения данных о частоте встречаемости симптомов простатита с оценкой распространенности дизурии, дискомфорта в промежности и в области полового члена было проведено международное (Англия, Франция, Голландия, Корея) эпидемиологическое исследование Urepik. Анализ, проводившийся на основании шкалы симптомов Nickel и Sorensen (1996), дал возможность выявить признаки простатита у 4800 мужчин в возрасте от 40 до 79 лет. У 35% мужчин за последний год наблюдался как минимум один из симптомов простатита, и для 8% мужчин это представляло, по меньшей мере, неудобство [1].
На долю хронического бактериального простатита (ХБП) приходится 5–15% случаев заболевания [6]. Наиболее распространенными, по мнению большинства исследователей, этиологическими агентами ХБП являются такие грамотрицательные бактерии семейства Enterobacteriaceae, как Escherichia coli, которые обнаруживаются в 65–80% случаев инфекций. Различные виды Serratia, Klebsiella, Enterobacter, Acinetobacter выявляются у 10–15% больных. Большинство исследователей полагают, что на долю таких грамположительных бактерий, как Enterococcus faecalis, приходится от 5 до 10% случаев подтвержденных инфекций простаты [5].
В настоящее время обсуждается роль грамположительных бактерий — коагулазо-негативных стафилококков и стрептококков в развитии ХБП [5, 6, 7]. По нашим данным (Е. Б. Мазо и соавт., 2003, 2004) [1], основанным на результатах микробиологического исследования, которое проводилось в виде четырехстаканного теста Meares–Stamey у 70 больных с ХБП с 2002 г., именно коагулазо-негативные стафилококки играют ведущую роль (66%), если говорить об этиологии ХБП. Между тем на долю грамотрицательных патогенов приходится 19% случаев ХБП, а 15% составляют больные с Enterococcus faecalis. Аналогичными данными располагают М. Ф. Трапезникова и соавторы (2004), суммировавшие результаты идентификации 662 штаммов микроорганизмов у 264 больных ХБП, за которыми велось наблюдение в течение последних 13 лет. При этом выявлена ведущая роль грамположительных кокков в этиологии ХБП: за последние 3 года частота распространения коагулазо-негативных стафилококков составила 87,5% [3]. В то же время удельный вес грамотрицательных палочек — «общепризнанных» возбудителей ХБП — за предыдущие 7 лет неуклонно снижался (с 13,3 до 4,2%). С. Н. Калинина, В. П. Александров, О. Л. Тиктинский (2003) при обследовании 174 больных ХБП также выявили преобладание (82%) грамположительной флоры. Инфекция простаты может быть следствием бактериальной колонизации мочеиспускательного канала. Нормальная флора мочеиспускательного канала у мужчин состоит главным образом из дифтероидов и грамположительных кокков. Сексуальная активность может способствовать колонизации мочеиспускательного канала потенциальными уропатогенами. Blacklock (1974) и Stamey (1980) отметили, что секрет простаты у некоторых мужчин с ХБП содержал те же уропатогены, которые присутствовали в вагинальной флоре их сексуальных партнерш. Бактериальная колонизация может также вызвать персистенцию бактерий в простате. Отличительной чертой этого состояния является персистенция бактерий внутри простаты, несмотря на лечение антибиотиками, что связано с хроническим воспалением и склонностью к обострению инфекции мочевыводящего тракта тем же самым патогеном.
К предрасполагающим факторам развития ХБП относятся: уретропростатический рефлюкс; фимоз; анально-генитальные сношения без предохранения; инфекции мочевых путей; острый эпидидимит; постоянные уретральные катетеры и проведение трансуретральных операций у мужчин с инфицированной мочой без предшествующей антимикробной терапии [1]. У пациентов с ХП может быть выявлено нарушение секреторной функции простаты, характеризующееся изменением состава секрета, т. е. снижением уровней фруктозы, лимонной кислоты, кислой фосфатазы, катионов цинка, магния и кальция; цинксодержащего антибактериального фактора простаты. При этом увеличиваются такие показатели, как рН, отношения изоферментов лактатдегидрогеназы-5 к лактатдегидрогеназе-1, белков воспаления — церулоплазмина и компонента комплемента С3. Эти изменения в секреторной функции простаты также обусловливают неблагоприятное воздействие на антибактериальную природу секрета простаты. Уменьшение действия антибактериального фактора простаты способно снижать врожденную противобактериальную активность секрета, тогда как щелочной показатель рН может препятствовать диффузии в ткань и в секрет простаты основных антимикробных препаратов.
Симптомами ХП являются боли в тазовой области, расстройства мочеиспускания и эякуляции (см. табл. 1).
| Таблица 1 Симптомы хронического простатита | ||
| Локализация боли в тазовой области | Расстройство мочеиспускания | Расстройство эякуляции |
| В промежности В половом члене В яичках В паховой области Над лоном В прямой кишке В крестце | Учащенное мочеиспускание Неполное опорожнение мочевого пузыря Слабая или прерывистая струя мочи Боль или ее усиление во время мочеиспускания | Боли во время или после эякуляции Гемоспермия |
Ведущее место в лабораторной диагностике ХБП принадлежит микробиологическому исследованию — четырехстаканному локализационному тесту, предложенному в 1968 г. Meares и Stamey [8]. Он состоит в получении, после тщательного туалета наружных половых органов (во избежание контаминации поверхностными бактериями), первой (10 мл) и второй (средней) порций мочи для бактериологического исследования, массажа предстательной железы (ПЖ) со взятием секрета для микроскопии и посева, а также третьей порции мочи (после взятия секрета) для посева (рис. 1). Количественные посевы первой и второй порций мочи выявляют бактерии в уретре и мочевом пузыре, в то время как при посевах секрета простаты и порции мочи после взятия секрета (третьей порции мочи) выявляют флору простаты. ХБП характеризуется воспалительной реакцией в секрете (при микроскопии определяется более 10 лейкоцитов в поле зрения при большом увеличении). После инкубации посевов подсчитывают количество колониеобразующих единиц (КОЕ).
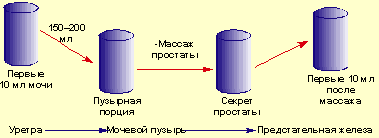 |
| Рисунок 1. Четырехстаканный локализационный тест Meares–Stamey |
Бактериологическое подтверждение ХБП мы проводим на основании, по крайней мере, одного из следующих критериев, предложенных K. G. Naber (2003):
Характерное для ХБП содержание патогенов в образцах примерно следующее:
первая порция мочи 3 КОЕ/мл;
вторая порция мочи 3 КОЕ/мл;
секрет простаты ≥ 10 4 КОЕ/мл;
третья порция мочи ≥ 10 3 КОЕ/мл.
Четкое соблюдение правил микробиологической диагностики и вышеуказанных критериев интерпретации результатов локализационного теста Meares — Stamey на большом количестве наблюдений позволят более точно определить частоту встречаемости истинных патогенов ХБП.
Антимикробная терапия. После идентификации этиологического агента и определения антибиотикорезистентности возникает необходимость назначения больному с ХБП антимикробной терапии. К факторам, оказывающим влияние на выбор антимикробного препарата для лечения ХБП, относятся: чувствительность идентифицированного микроорганизма к антибиотику, его способность в достаточной концентрации проникать через гематопростатический барьер и накапливаться в ткани и секрете простаты, сперме, а также способность препарата преодолевать экстрацеллюлярную полисахаридную оболочку, формируемую микроколониями бактерий, и хорошая переносимость при длительном пероральном приеме. Идеальный антибактериальный препарат для лечения ХБП должен быть жирорастворимым, слабощелочным, с коэффициентом диссоциации, способствующим максимальной концентрации препарата в простате [2]. Антимикробные средства из группы фторхинолонов на сегодняшний день отвечают вышеперечисленным требованиям и являются препаратами выбора для лечения ХБП. Особенностью антибактериального действия фторхинолонов является наличие двух мишеней действия в бактериальной клетке, каковыми являются ферменты (топоизомеразы II типа), ответственные за изменения пространственной конфигурации бактериальной ДНК: ДНК-гираза и топоизомераза IV. ДНК-гираза осуществляет суперспирализацию бактериальной ДНК, а топоизомераза IV — разделение дочерних хромосом в процессе репликации. Ключевым моментом в действии фторхинолонов является образование трехкомпонентного комплекса (бактериальная ДНК–фермент–фторхинолон). Указанный комплекс предотвращает репликацию бактериальной ДНК. Благодаря тому, что топоизомеразы обладают расщепляющей активностью, происходит разрушение молекулы ДНК (С. В. Сидоренко, 2002).
 |
| Рисунок 2. Классификация фторхинолонов (по K.G. Naber,1998) |
В настоящее время в практическое здравоохранение внедрены новые антимикробные препараты из группы фторхинолонов III и IV поколений, которые проявляют активность в отношении как грамотрицательных и грамположительных бактерий, так и атипичных внутриклеточных микроорганизмов, а также обладают способностью воздействовать на бактерии в биологических пленках (см. рис. 2). Антимикробная активность in vitro фторхинолонов III поколения — спарфлоксацина и левофлоксацина, а также фторхинолона IV поколения — моксифлоксацина наглядно представлена в таблице 2.
| Таблица 2 Антимикробная активность in vitro спарфлоксацина, левофлоксацина и моксифлоксацина (МПК90, мкг/мл) [4] | |||
| Микроорганизмы | Спарфлоксацин | Левофлоксацин | Моксифлоксацин |
| Acinetobacter spp. | 0,25 | 16 | 0,5 |
| Citrobacter freundii | 0,25 | 0,5 | 0,5 |
| Enterobacter cloacae | 0,5 | 0,5 | 0,5 |
| Escherichia coli | 0,12 | 0,12 | 0,5 |
| Klebsiella pneumoniae | 0,25 | 0,25 | 0,5 |
| Proteus mirabilis | 0,5 | 0,25 | 0,12 |
| Pseudomonas aeruginosa | 8 | 4 | 16 |
| Staphylococcus epidermidis | 1 | 1 | 2 |
| Staphylococcus saprophyticus | 0,25 | — | 0,5 |
| Enterococcus faecalis | 2 | 16 | 4 |
В 2004 г. мы сравнили чувствительность 25 различных штаммов коагулазо-негативных стафилококков — наиболее распространенных, по нашим данным (Е. Б. Мазо и соавт., 2003, 2004), этиологических агентов ХБП — к левофлоксацину, спарфлоксацину и моксифлоксацину. Бактериологическое исследование проводили классическим методом: выполняли посев мочи и секрета простаты на питательные среды с выделением чистой культуры и идентификацией выделенных штаммов при помощи полуавтоматического микробиологического анализатора Sceptor (Becton Dickinson, USA). Чувствительность выделенных микроорганизмов к левофлоксацину, спарфлоксацину и моксифлоксацину определяли дискодиффузионным методом на среде Мюллера–Хинтона. Результаты оценивали по значениям диаметров зон задержки роста. Всего было изучено 25 штаммов коагулазо-негативных стафилококков (21 — Staphylococcus haemolyticus, 3 — Staphylococcus epidermidis, 1 — Staphylococcus warnerii), выделенных в диагностическом титре из секрета простаты и мочи у больных ХБП при четырехстаканном тесте Meares–Stamey. Проведенный нами анализ чувствительности коагулазо-негативных стафилококков к фторхинолонам III и IV поколений показал наиболее высокую чувствительность этих бактерий к моксифлоксацину — у 24 (96%) штаммов. К левофлоксацину оказались чувствительны 21 (84%), а к спарфлоксацину 20 (80%) штаммов коагулазо-негативных стафилококков. Пять резистентных к спарфлоксацину штаммов были выделены нами у больных после длительной антимикробной терапии этим препаратом. Был выделен также штамм гемолитического стафилококка, резистентный ко всем фторхинолонам III и IV поколений у больного, ранее принимавшего в течение 6 нед моксифлоксацин. Проведенное исследование продемонстрировало высокую чувствительность коагулазо-негативных стафилококков, выделенных от больных ХБП, к фторхинолонам III и IV поколений. Чувствительность исследованных бактерий к моксифлоксацину оказалась наиболее высокой, в то время как к левофлоксацину и спарфлоксацину была практически одинаково ниже. Таким образом, длительная антимикробная терапия моксифлоксацином может привести к селекции устойчивых штаммов и развитию перекрестной резистентности к фторхинолонам III и IV поколений.
На сегодняшний день проведено ограниченное количество клинических исследований применения фторхинолонов в лечении ХБП. Результаты таких исследований, с периодом наблюдения не менее 6 мес, представлены в таблице 3.
Как видно из данных, приведенных в таблице 3, несмотря на существенные различия в количестве больных, принимавших участие в исследованиях, бактериальная эрадикация при различной длительности терапии фторхинолонами, наблюдалась более чем у 60% пациентов. Проведение подобных исследований в будущем, с соблюдением стандартов микробиологической диагностики, позволит выработать единый подход к рациональной антимикробной терапии ХБП.
Согласно актуальным на сегодняшний день рекомендациям Европейской ассоциации урологов по лечению инфекций мочевыводящих путей и инфекций репродуктивной системы у мужчин, принятым в 2001 г., длительность антимикробной терапии ХБП фторхинолонами или триметопримом должна составлять 2 нед (после установления предварительного диагноза). После повторного обследования больного антимикробную терапию рекомендуют продолжать суммарно в течение 4–6 нед только при положительном результате микробиологического исследования секрета простаты, взятого до начала лечения, или в случае, если у больного улучшилось состояние после приема антимикробных препаратов [2].
Антимикробные препараты, используемые для лечения ХБП, а также способы их применения приведены в таблице 4.
| Таблица 4 Способы применения антимикробных препаратов для лечения хронического бактериального простатита | ||
| Группа препаратов | Препараты | Способ применения |
| Фторхинолоны | Ципрофлоксацин (сифлокс, ципролет, цифран) | По 500 мг 2 раза в сутки |
| Офлоксацин (джеофлокс, заноцин, офлоксин 200) | По 400 мг 2 раза в сутки | |
| Ломефлоксацин (ксенаквин, ломфлокс, максаквин) | По 400 мг 1 раз в сутки | |
| Левофлоксацин (таваник) | По 500 мг 1 раз в сутки | |
| Спарфлоксацин (спарфло) | Первый прием 400 мг, затем по 200 мг 1 раз в сутки | |
| Моксифлоксацин (авелокс) | По 400 мг 1 раз в сутки | |
| Триметоприм/ сульфаметоксазол | Ко-тримоксазол (бикотрим, бисептол) | По 960 мг 2 раза в сутки |
Следует отметить, что больные с ХБП должны принимать антибиотик фторхинолонового ряда в течение длительного периода (от 4 до 6 нед) для предотвращения рецидива инфекции нижних мочевых путей. Продолжительная терапия антибиотиками в низких профилактических дозах или супрессивная антимикробная терапия могут применяться в случаях рецидивирующего или невосприимчивого к лечению простатита.
Литература
С. В. Попов
А. К. Чепуров, доктор медицинских наук, профессор
В. И. Карабак, кандидат медицинских наук
РГМУ, Москва
Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Современные аспекты лечения воспалительных заболеваний органов малого таза у женщин
Воспалительные заболевания органов малого таза характеризуются различными проявлениями, в зависимости от уровня поражения и силы воспалительной реакции. Заболевание развивается при проникновении в половые пути возбудителя (энтерококки, бактероиды, хлами
Воспалительные заболевания органов малого таза характеризуются различными проявлениями, в зависимости от уровня поражения и силы воспалительной реакции. Заболевание развивается при проникновении в половые пути возбудителя (энтерококки, бактероиды, хламидии, микоплазмы, уреаплазмы, трихомонады) и при наличии благоприятных условий для его развития и размножения. Эти условия имеют место в послеродовом или послеабортном периодах, во время менструаций, при различных внутриматочных манипуляциях (введении внутриматочных контрацептивов (ВМК), гистероскопии, гистеросальпингографии, диагностических выскабливаниях) [1, 5].
Существующие естественные защитные механизмы, такие как анатомические особенности, местный иммунитет, кислая среда влагалища, отсутствие эндокринных нарушений или серьезных экстрагенитальных заболеваний, способны в подавляющем большинстве случаев предотвратить развитие генитальной инфекции.
В ответ на инвазию того или иного микроорганизма возникает воспалительный ответ, который, исходя из последних концепций развития септического процесса, принято называть «системным воспалительным ответом» [16, 17, 18].
Эндометрит
Острый эндометрит всегда требует антибактериальной терапии. Воспалительным процессом поражается базальный слой эндометрия вследствие инвазии специфических или неспецифических возбудителей. Защитные механизмы эндометрия, врожденные или приобретенные, такие как Т-лимфоциты и другие элементы клеточного иммунитета, напрямую связаны с действием половых гормонов, особенно эстрадиола, действуют совместно с популяцией макрофагов и защищают организм от повреждающих факторов. С началом менструации этот барьер на большой поверхности слизистой оболочки исчезает, что делает возможным ее инфицирование. Другой источник защиты в матке — это инфильтрация подлежащих тканей полиморфно-ядерными лейкоцитами и богатое кровоснабжение матки, способствующее адекватной перфузии органа кровью и содержащимися в ее сыворотке неспецифическими гуморальными элементами защиты: трансферрином, лизоцимом, опсонинами [16].
Воспалительный процесс может распространиться и на мышечный слой, и возникает метроэндометрит и метротромбофлебит с тяжелым клиническим течением. Воспалительная реакция характеризуется расстройством микроциркуляции в пораженных тканях, выраженной экссудацией, при присоединении анаэробной флоры может возникнуть некротическая деструкция миометрия [12].
Клинические проявления острого эндометрита характеризуются уже на 3–4-й день после занесения инфекции повышением температуры тела, тахикардией, лейкоцитозом с палочкоядерным сдвигом, увеличением скорости оседания эритроцитов (СОЭ). Умеренное увеличение матки сопровождается болезненностью, особенно по ее ребрам (по ходу кровеносных и лимфатических сосудов). Появляются гнойно-кровянистые выделения. Острая стадия эндометрита продолжается 8–10 дней и требует достаточно серьезного лечения. При правильном лечении процесс заканчивается, реже переходит в подострую и хроническую форму, еще реже, при самостоятельной и беспорядочной терапии антибиотиками, эндометрит может принимать более легкое абортивное течение [5, 12].
Лечение острого эндометрита вне зависимости от тяжести его проявлений начинается с антибактериальной инфузионной, десенсибилизирующей и общеукрепляющей терапии.
Антибиотики лучше всего назначать с учетом чувствительности к ним возбудителя, дозы и длительность применения антибиотиков определяются тяжестью заболевания. Из-за угрозы анаэробного инфицирования рекомендуется дополнительное применение метронидазола. Учитывая очень бурное течение эндометрита, из антибиотиков предпочтительны цефалоспорины с аминогликозидами и метронидазолом. Например, цефамандол (или цефуроксим, цефотаксим) по 1,0–2,0 г 3–4 раза в день внутримышечно или внутривенно капельно + гентамицин по 80 мг 3 раза в сутки внутримышечно + метронидазол по 100 мл внутривенно капельно.
Вместо цефалоспоринов можно использовать полусинтетические пенициллины (при абортивном течении), например ампициллин по 1,0 г 6 раз в сутки. Длительность такой комбинированной антибактериальной терапии зависит от клиники и лабораторного ответа, но не менее 7–10 дней.
В качестве профилактики дисбактериоза с первых дней лечения антибиотиками используют нистатин по 250 000 ЕД 4 раза в день или флуконазол по 50 мг в день в течение 1–2 нед внутрь или внутривенно [5].
Дезинтоксикационная инфузионная терапия может включать назначение инфузионных средств, например: раствор Рингера — 500 мл, полиионные растворы — 400 мл, 5% раствор глюкозы — 500 мл, 10% раствор хлорида кальция — 10 мл, унитиол с 5% раствором аскорбиновой кислоты по 5 мл 3 раза в сутки. При наличии гипопротеинемии целесообразно проводить инфузии белковых растворов (альбумин), кровозамещающих растворов, плазмы, эритроцитарной массы, препаратов аминокислот [12].
Физиотерапевтическое лечение занимает одно из ведущих мест в лечении острого эндометрита. Оно не только уменьшает воспалительный процесс в эндометрии, но и стимулирует функцию яичников. При нормализации температурной реакции целесообразно назначать ультразвук малой интенсивности, индуктотермию электромагнитным полем высокой частоты или ультравысокой частоты (УВЧ), магнитотерапию, лазеротерапию.
– парацетамол + ибупрофен по 1–2 таблетки 3 раза в день — 10 дней;
– диклофенак ректально в свечах или перорально по 50 мг 2 раза в день — 10–15 дней;
– индометацин ректально в свечах или перорально по 50 мг 2 раза в день — 10–15 дней;
– напроксен по 500 мг 2 раза в день ректально в свечах или перорально — 10–15 дней.
– метилглукамина акридонацетат по 250 мг внутримышечно через день — 10 дней;
– оксодигидроакридинилацетат натрия по 250 мг внутримышечно через день — 10 дней.
Рекомендуется дополнительное лечение.
– этинилэстрадиол 30 мкг + левоноргестрел 150 мкг (ригевидон);
– этинилэстрадиол 35 мкг + норгестимат 250 мкг (силест);
– этинилэстрадиол 30 мкг + гестоден 75 мкг (фемоден);
– этинилэстрадиол 30 мкг + дезогестрел 150 мкг (марвелон).
Дополнительное лечение в дни менструаций включает следующее.
Тетрациклины (обладают широким спектром действия: грамположительные кокки, спорообразующие бактерии, неспорообразующие бактерии, грамотрицательные кокки и палочки, хламидии, микоплазмы): доксициклин по 100 мг 2 раза в день.
Макролиды (активны в отношении грамположительных кокков, грамотрицательных бактерий, гарднерелл, хламидий, микоплазм, уреаплазм):
– азитромицин по 500 мг 2 раза в день;
– рокситромицин по 150 мг 2 раза в день;
– кларитромицин по 250 мг 2 раза в день.
Фторхинолоны (активны в отношении всех грамположительных и грамотрицательных бактерий): ципрофлоксацин по 500 мг 2 раза в день; офлоксацин — 800 мг однократно в день в течение 10–14 дней.
Производные нитроимидазола (активны в отношении анаэробов, простейших): метронидазол по 500 мг 4 раза в день.
Противогрибковые средства (активны в отношении грибов рода Candida):
– нистатин по 250 000 ЕД 4 раза в день;
– натамицин по 100 мг 4 раза в день;
– флуконазол — 150 мг однократно.
Острый сальпингоофорит
Относится к самым частым заболеваниям воспалительной этиологии у женщин. Каждой пятой женщине, перенесшей сальпингоофорит грозит бесплодие. Аднексит может быть причиной высокого риска внематочной беременности и патологического течения беременности и родов. Первыми поражаются маточные трубы, при этом воспалительным процессом могут быть охвачены все слои слизистой оболочки одной или обеих труб, но чаще возникает катаральное воспаление слизистой оболочки трубы — эндосальпингит. Воспалительный экссудат, скапливаясь в трубе, нередко вытекает через ампулярное отверстие в брюшную полость, вокруг трубы образуются спайки, и брюшное отверстие трубы закрывается. Развивается мешотчатая опухоль в виде гидросальпинкса с прозрачным серозным содержимым или в виде пиосальпинкса с гнойным содержимым. В дальнейшем серозный экссудат гидросальпинкса рассасывается в результате лечения, а гнойный пиосальпинкс может перфорировать в брюшную полость. Гнойный процесс может захватывать более широкие области малого таза, распространяясь на все близлежащие органы [9, 10, 13].
Воспаление яичников (оофорит) как первичное заболевание встречается редко, инфицирование происходит в области лопнувшего фолликула, так как остальная ткань яичника хорошо защищена покрывающим зародышевым эпителием. В острой стадии наблюдается отек и мелкоклеточная инфильтрация. Иногда в полости фолликула желтого тела или мелких фолликулярных кист образуются гнойники, микроабсцессы, которые, сливаясь, формируют абсцесс яичника или пиоварий. Практически диагностировать изолированный воспалительный процесс в яичнике невозможно, да в этом и нет необходимости. В настоящее время лишь у 25–30% больных с острым аднекситом отмечается выраженная картина воспаления, у остальных пациентов наблюдается переход в хроническую форму, когда терапия прекращается после быстрого стихания воспаления.
Острый сальпингоофорит лечится также антибиотиками, (предпочтительнее фторхинолоны III поколения — ципрофлоксацин, офлоксацин, пефлоксацин), так как нередко сопровождается пельвиоперитонитом — воспалением тазовой брюшины.
При нетяжелой форме назначается следующее.
1. Антибактериальная терапия перорально в течение 5–7 дней.
– азитромицин по 500 мг 2 раза в день;
– рокситромицин по 150 мг 2 раза в день;
– кларитромицин по 250 мг 2 раза в день.
– ципрофлоксацин по 500 мг 2 раза в день;
– офлоксацин — 800 мг однократно в день — 10–14 дней.
2. Производные нитроимидазола перорально (активны в отношении анаэробов, простейших):
– метронидазол по 500 мг 3 раза в день;
– орнидазол по 500 мг 3 раза в день.
3. Противогрибковые средства перорально (активны в отношении грибов рода Candida):
– нистатин по 500 000 ЕД 4 раза в день;
– натамицин по 100 мг 4 раза в день;
– флуконазол — 150 мг однократно.
4. Антигистаминные препараты перорально (предупреждают развитие аллергических реакций):
– фексофенадин по 180 мг 1 раз в день;
– хлоропирамин по 25 мг 2 раза в день.
Дополнительное лечение включает следующее.
– парацетамол + ибупрофен по 1–2 таблетки 3 раза в день;
– диклофенак или индометацин ректально в свечах или перорально по 50 мг 2 раза в день — 10–15 дней;
– напроксен по 500 мг 2 раза в день ректально в свечах или перорально — 10–15 дней.
При тяжелом течении назначаются препараты следующих групп.
1. Антибактериальная терапия перорально в течение 7–10 дней. Во время антибактериальной терапии оценка клинической эффективности комбинации препаратов проводится через 3 дня, при необходимости — смена препаратов через 5–7 дней.
– ципрофлоксацин 1000 мг однократно в день;
– пефлоксацин, офлоксацин по 200 мг 2 раза в день внутривенно.
– гентамицин по 240 мг 1 раз в день внутривенно;
– амикацин по 500 мг 2 раза в день внутривенно.
2. Противогрибковые средства (активны в отношении грибов рода Candida): флуконазол 150 мг однократно перорально.
3. Производные нитроимидазола (активны в отношении анаэробов, простейших): метронидазол по 500 мг 2 раза в день внутривенно.
4. Коллоидные, кристаллоидные растворы (внутривенно капельно):
– реополиглюкин 400 мл;
– глюкоза 5% раствор 400 мл.
5. Витамины и витаминоподобные вещества (оказывают антиоксидантное действие). Внутривенно струйно или капельно в 0,9% растворе натрия хлорида:
– аскорбиновая кислота 5% раствор 5 мл;
– кокарбоксилаза 100 мг.
Дополнительное лечение включает следующее.
– метилглукамина акридонацетат по 250 мг внутримышечно через день — 10 дней;
– оксодигидроакридинилацетат натрия по 250 мг внутримышечно через день — 10 дней.
Лечение при хроническом сальпингоофорите включает следующее.
– парацетамол + ибупрофен по 1–2 таблетки 3 раза в день после еды — 10 дней;
— диклофенак или индометацин ректально в свечах или перорально по 50 мг 2 раза в день — 10–15 дней;
– напроксен по 500 мг 2 раза в день ректально в свечах или перорально — 10–15 дней.
Рекомендуется дополнительное лечение.
– этинилэстрадиол 30 мкг + левоноргестрел 150 мкг (ригевидон)
– этинилэстрадиол 35 мкг + норгестимат 250 мкг (силест).
– этинилэстрадиол 30 мкг + гестоден 75 мкг (фемоден)
– этинилэстрадиол 30 мкг + дезогестрел 150 мкг (марвелон).
Низкодозированные пероральные контрацептивные препараты нормализуют функцию гипоталамо-гипофизарно-яичниковой системы. При длительном приеме необходим контроль гемостаза, функций печени.
Пельвиоперитонит
Воспаление тазовой брюшины возникает чаще всего вторично от проникновения инфекции в брюшную полость из инфицированной матки (при эндометрите, инфицированном аборте, восходящей гонорее), из маточных труб, яичников, из кишечника, при аппендиците, особенно при тазовом его расположении. При этом наблюдается воспалительная реакция брюшины с образованием серозного, серозно-гнойного или гнойного выпота. Состояние больных при пельвиоперитоните средней тяжести температура повышается, пульс учащается, однако функция сердечно-сосудистой системы нарушается незначительно. При пельвиоперитоните кишечник остается невздутым, пальпация верхней половины органов брюшной полости безболезненна, а симптомы раздражения брюшины определяются лишь над лоном и в подвздошных областях. Тем не менее больные отмечают сильные боли в нижних отделах живота, может быть задержка стула и газов, иногда рвота. Уровень лейкоцитов повышен, сдвиг лейкоцитарной формулы влево, СОЭ ускорена. Постепенно нарастающая интоксикация ухудшает состояние больных [14, 15].
Лечение сальпингоофорита с пельвиоперитонитом или без него начинается с обязательного обследования больной на флору и чувствительность к антибиотикам. Самое главное — следует определить этиологию воспаления. На сегодняшний день для лечения специфического гонорейного процесса широко используется бензилпенициллин, хотя такие препараты, как цефтриаксон, перазон, цефтазидим, предпочтительнее.
«Золотым стандартом» при лечении сальпингоофорита из антибактериальной терапии является назначение цефотаксима в дозе 1,0–2,0 г 2–4 раза в сутки внутримышечно или 1 дозу — 2,0 г внутривенно в сочетании с гентамицином по 80 мг 3 раза в сутки (можно гентамицин вводить однократно в дозе 160 мг внутримышечно). Обязательно следует сочетать эти препараты с введением метронидазола внутривенно по 100 мл 1–3 раза в сутки. Курс лечения антибиотиками следует проводить не менее 5–7 дней и варьировать можно в основном базисный препарат, назначая цефалоспорины II и III поколения (цефамандол, цефуроксим, цефтриаксон, перазон, цефтазидим и другие в дозе 2–4 г в сутки) [14].
При неэффективности стандартной антибиотикотерапии применяется ципрофлоксацин в дозировке 500 мг 2 раза в день в течение 7–10 дней.
При остром воспалении придатков матки, осложненном пельвиоперитонитом, оральное введение антибиотиков возможно лишь после проведения основного курса, и притом если в этом возникает необходимость. Как правило, такой необходимости нет, а сохранение прежних клинических симптомов может свидетельствовать о прогрессировании воспаления и о возможном нагноительном процессе.
Дезинтоксикационная терапия в основном проводится кристаллоидными и дезинтоксикационными растворами в количестве 2–2,5 л с включением растворов реополиглюкина, Рингера, полиионных растворов — ацессоля и др. Антиоксидантная терапия проводится раствором унитиола 5,0 мл с 5% раствором аскорбиновой кислоты 3 раза в сутки внутривенно [14].
С целью нормализации реологических и коагуляционных свойств крови и улучшения микроциркуляции используют ацетилсалициловую кислоту по 0,25 г/сут в течение 7–10 дней, а также внутривенно введение реополиглюкина по 200 мл (2–3 раза на курс). В дальнейшем применяют целый комплекс рассасывающей терапии и физиотерапевтического лечения (глюконат кальция, аутогемотерапию, тиосульфат натрия, гумизоль, плазмол, алоэ, фиБС) [3, 15]. Из физиотерапевтических процедур при остром процессе уместны ультразвук, который обеспечивает анальгезирующий, десенсибилизирующий, фибролитический эффекты, усиление обменных процессов и трофики тканей, индуктотермия, УВЧ-терапия, магнитотерапия, лазеротерапия, в дальнейшем — санаторно-курортное лечение.
Гнойные тубоовариальные образования
Среди 20–25% стационарных больных с воспалительными заболеваниями придатков матки у 5–9% возникают гнойные осложнения, требующие хирургических вмешательств [9, 13].
Можно выделить следующие особенности, касающиеся формирования гнойных тубоовариальных абсцессов:
Встречаются следующие морфологические формы гнойных тубоовариальных образований:
Все остальные сочетания являются осложнениями этих процессов и могут протекать:
Клинически дифференцировать каждую из подобных локализаций практически невозможно и нецелесообразно, так как лечение принципиально одинаково — антибактериальная терапия занимает ведущее место как по использованию наиболее активных антибиотиков, так и по длительности их применения. При гнойных процессах последствия воспалительной реакции в тканях носят зачастую необратимый характер. Необратимость обусловлена морфологическими изменениями, их глубиной и тяжестью. Часто наблюдается тяжелое нарушение функции почек [3, 9].
Консервативное лечение необратимых изменений придатков матки малоперспективно, так как если таковое проводится, то оно создает предпосылки к возникновению новых рецидивов и усугублению нарушенных обменных процессов у больных, увеличивает риск предстоящей операции в плане повреждения смежных органов и невозможности выполнить нужный объем операции [9].
Гнойные тубоовариальные образования представляют собой тяжелый в диагностическом и клиническом плане процесс. Тем не менее можно выделить характерные синдромы.
Стратегия лечения данной группы больных строится на органосохраняющих операциях, но с радикальным удалением основного очага инфекции. Поэтому у каждой конкретной больной и время операции, и выбор ее объема должны быть оптимальными. Уточнение диагноза иногда занимает несколько суток, особенно при дифференциации с онкологическим процессом. На каждом этапе лечения требуется антибактериальная терапия [1, 2].
Предоперационная терапия и подготовка к операции включают:
Хирургический этап включает также продолжающуюся антибактериальную терапию. Особенно целесообразно введение одной суточной дозы антибиотиков на операционном столе, сразу после окончания операции. Эта концентрация является необходимой и создает барьер для дальнейшего распространения инфекции, так как проникновению в зону воспаления уже не препятствуют плотные гнойные капсулы тубоовариальных абсцессов. Хорошо проходят эти барьеры b-лактамные антибиотики (цефоперазон, цефтриаксон, цефтазидим, цефотаксим, имипинем/циластатин, амоксициллин + клавулановая кислота).
Послеоперационная терапия включает продолжение антибактериальной терапии теми же антибиотиками в сочетании с антипротозойными, антимикотическими препаратами и уросептиками. Курс лечения назначается в соответствии с клинической картиной, лабораторными данными; он не должен быть прекращен ранее чем через 7–10 дней. Инфузионная терапия должна быть направлена на борьбу с гиповолемией, интоксикацией и метаболическими нарушениями. Очень важна нормализация моторики желудочно-кишечного тракта (стимуляция кишечника, гипербарическая оксигенация, гемосорбция или плазмаферез, ферменты, перидуральная блокада, промывание желудка и т. д.). Гепатотропная, общеукрепляющая, антианемическая терапия сочетается с иммуностимулирующей терапией (ультрафиолетовое облучение, лазерное облучение крови, иммунокорректоры) [2, 9, 11].
Все больные, перенесшие оперативное вмешательство по поводу гнойных тубоовариальных абсцессов, нуждаются в постгоспитальной реабилитации с целью восстановления функции органа и профилактики.
Литература
В. Н. Кузьмин, доктор медицинских наук, профессор
МГМСУ, Москва




