что принимать когда пьешь антибиотики чтобы не было дисбактериоза
Современные подходы к профилактике антибиотик-ассоциированной супрессии микрофлоры желудочно-кишечного тракта
Антибиотики применяются врачами самых разных специальностей, причем в ряде случаев специалисты не имеют достаточных знаний по вопросам применения противомикробных препаратов. Существенно шире стал и спектр заболеваний, при которых применяют эту группу лек
Антибиотики применяются врачами самых разных специальностей, причем в ряде случаев специалисты не имеют достаточных знаний по вопросам применения противомикробных препаратов. Существенно шире стал и спектр заболеваний, при которых применяют эту группу лекарственных средств.
Так, в конце XX века по мере совершенствования микробиологических техник и появления новых методов изучения микробиоценозов и роли отдельных микроорганизмов дальнейшее развитие получила «инфекционная гастроэнтерология». К примеру, активно изучается роль инфекционных агентов в развитии атеросклероза (хламидии, вирусы), нарушении обмена веществ (гипохолестеринемическое и гипогликемическое действие) и т. д.
Постепенно антимикробные препараты (АМП) вышли за рамки «классических инфекций».
Огромное количество антибиотиков используется животноводством. Так, по данным H. L. DuPont и J. H. Steele (1987) около 45% антибиотиков в США потребляется именно этой сферой.
В 1999 году по данным, опубликованным Европейской федерацией здоровья животных (FEDESA), ежегодный расход антибиотиков во всем ЕС, включая Швейцарию, составил в целом 13 200 т. При этом медицина потребляет 8 500 т, а ветеринария — 3 900 т, 800 из которых (6% всего потребления антибиотиков) назначались в виде так называемых кормовых антибиотиков (стимуляторов роста животных).
Американская ассоциация общественного здоровья (APHA), принимая во внимание постоянно растущую антибиотикорезистентность основных возбудителей заболеваний у человека, призвала Управление по контролю за пищевыми продуктами и лекарственными средствами США (FDA) запретить применение семи классов антибиотиков в сельском хозяйстве в качестве стимуляторов роста и лечения животных. Такое решение обусловлено нарушением стандартов безопасности, провозглашенных FDA. В соответствии с рекомендациями FDA препараты, имеющие высокую важность при лечении заболеваний людей, не подлежат широкому использованию в сельском хозяйстве. Тем не менее, антибиотики семи классов, в том числе важнейших для человека, таких как пенициллины и тетрациклины, широко применяются при лечении животных. Около 70% антибиотиков используются ежегодно при кормлении крупного рогатого скота и домашней птицы с целью стимуляции роста и для профилактики заболеваний, опасность возникновения которых обусловлена большими скоплениями животных и негигиеничными условиями содержания. Более половины антибиотиков относятся или близки к тем же классам препаратов, которые используются у человека, что сопровождается риском потери этих препаратов для лечения заболеваний людей [1].
В России в 2001–2003 гг. наиболее высокий уровень потребления АМП был характерен для бета-лактамов, тетрациклинов и ко-тримоксазола, в 2004 г. — для бета-лактамов, тетрациклинов и фторхинолонов [2]. При сокращении потребления бензилпенициллина и ампициллина отмечался рост потребления амоксициллина и амоксициллина/клавуланата. В два раза выросло потребление цефалоспоринов, преимущественно за счет цефазолина (I поколение) и цефотаксима (III поколение). Доксициклина потреблялось в 5–7 раз больше, чем тетрациклина. Значительный рост потребления фторхинолонов был связан с широким применением ципрофлоксацина и норфлоксацина. Продолжал широко применяться хлорамфеникол (Левомицетин). На основании полученных данных авторы делают заключение, что «для РФ присущ необычный в сравнении с большинством европейских стран профиль потребления АМП, характеризующийся существенно более высоким удельным весом относительно дешевых, нередко устаревших препаратов с неблагоприятным профилем безопасности…».
Большое число ошибок в назначении антибиотиков характерно при лечении острых респираторных инфекций у детей (Таточенко В. К., 2002), острого тонзиллофарингита (Козлов С. Н. и соавт., 2001, 2002), острых кишечных инфекций (Захаренко С. М. и соавт., 2002, 2006), острого синусита, инфекций мочевыводящих путей (Ершов Г. В. и соавт., 2001), инфекций кожи и мягких тканей (Рафальский Б. В. и соавт., 2004), внебольничной пневмонии и др.
Основной причиной пристального внимания к проблеме необоснованного применения антибиотиков является драматической рост резистентности микроорганизмов к антимикробным препаратам. Именно этот аспект остается приоритетным для Всемирной организации здравоохранения [3, 4] и государственных систем здравоохранения во всех странах.
Вместе с тем существует и еще одна важнейшая сторона проблемы применения АМП — необоснованное негативное воздействие на микробиоценозы человека.
Позиция FDA и ФЦМБЛС (Федеральный центр мониторинга безопасности лекарственных средств), отражающая точку зрения американских, российских и европейских специалистов по антимикробной терапии, однозначна:
«Все классы антибиотиков широкого спектра действия в той или иной степени угнетают нормальную микрофлору толстого кишечника, что может привести к избыточному росту Clostridium difficile, последующему высвобождению токсинов А и В и развитию антибиотик-ассоциированной диареи (ААД).
Клинические проявления нарушения кишечного микробиоценоза могут варьировать по степени тяжести от легкой диареи до тяжелейшего колита со смертельным исходом и проявляться отсроченно: зафиксированы случаи развития псевдомембранозного колита спустя два месяца после завершения курса антибактериальной терапии».
Негативное воздействие АМП на микробиоценозы человека в целом и кишечника в частности связано с несколькими механизмами: прямым подавляющим действием на нормофлору, опосредованными эффектами и влиянием компонентов препарата (не самого антибиотика).
Спектры действия антибиотиков имеют существенные различия, однако в той или иной степени они воздействуют на аэробную и анаэробную микрофлору, относящуюся к индигенной. Цефоперазон и цефиксим, кроме того, при неполном всасывании в кишечнике могут способствовать развитию гиперосмолярной диареи [5], пенициллины могут вызывать сегментарный колит, а тетрациклины — оказывать токсическое действие на слизистую оболочку желудочно-кишечного тракта [6]. Клавулановая кислота, являющаяся важным компонентом ряда «защищенных» антибиотиков, стимулирует двигательную активность кишечника, приводя к развитию гиперкинетической диареи [6]. Гиперкинетический эффект характерен и для некоторых макролидов, например эритромицина.
К опосредованным эффектам относят нарушение рециркуляции желчных кислот, приводящее к появлению секреторного компонента в развитии диареи; нарушение пристеночного пищеварения, особенно углеводов, «добавляющее» осмотический компонент к формирующемуся патологическому состоянию; снижение количества короткоцепочечных жирных кислот, ведущее к нарушению энергообеспечения кишечного эпителия; активность ряда важных бактериальных энзимов и утрату контроля за активностью условно-патогенных микроорганизмов с продукцией последними ряда токсинов и биологически активных веществ, не характерных для нормобиотического состояния. Эти механизмы лежат в основе формирования такого патологического состояния, как ААД, являющаяся одним из наиболее частых осложнений лечения антибиотиками и встречающаяся приблизительно у 5–25% пациентов, получающих эти препараты [7, 8].
Именно ААД составляет до 20–45% всех внутрибольничных диарей [9]. Частота развития этого состояния зависит от применявшегося антибиотика и составляет для амоксициллина/клавуланата 10–25%, цефиксима — 15–20%, ампициллина и клиндамицина — 5–10%, фторхинолонов — 1–2%, ко-тримоксазола — около 1%.
ААД является полиэтиологичным состоянием, которое обусловлено в 15–30% случаев C. difficile, а при развитии колита — 50–75% и псевдомембранозного колита — до 90%. CD-инфекция может протекать в разных клинических формах [10]:
Основное значение в патогенезе этих состояний имеет активация продукции C. difficile ряда токсинов — токсина А (TcdA), больше имеющего свойство энтеротоксина; токсина В (TcB), являющегося цитотоксином; бинарного токсина (ADP-ribosyltransferase toxin), сходного с токсинами C. spiroforme и C. perfringens; токсина TcdB-1470, обладающего цитотоксической активностью и сходного с TcsL-токсином C. sordellii [11].
Штаммы C. difficile продуцируют токсины А и В в лог-фазу роста вегетирующих форм [12–14], активность синтеза токсинов в значительной мере зависит от факторов окружающей среды.
Несмотря на разработанные схемы лечения CD-ассоциированной диареи частота рецидивов при использовании метронидазола и ванкомицина составляет от 5–16% до 50% [15–17]. При этом риск развития рецидива сохраняется в течение 30 суток после назначения антимикробного препарата, явившегося причиной первого эпизода заболевания.
Одним из неблагоприятных факторов, присущих современному урбанизированному обществу, является ежедневный дефицит физиологических пребиотических веществ, которые наша микрофлора «привыкла» получать с пищей.
Хотя и не существует определенной рекомендованной ежедневной лечебной дозы пребиотиков, доза 4–20 г/сут оказалась эффективной у взрослых. По данным M. B. Roberfroid и соавт. [18] минимальная эффективная доза для взрослого человека для инулина или фруктоолигосахаридов составляет 4 г, а при назначении дозы 20 г возможно появление у части лиц побочных эффектов, таких как вздутие живота или флатуленция. Эти эффекты в большей степени присущи короткоцепочечным фруктоолигосахаридам [19]. Вместе с тем, по данным Ткаченко Е. И. и Успенского Ю. П. (2008), при современном стереотипе питания городского жителя реальное фактическое поступление пребиотических веществ с пищей, как правило, не превышает 1/3–1/2 от условно-необходимого их количества. Т. е. можно говорить о сформировавшейся «пребиотической недостаточности» питания. Одним из способов восполнения дефицита пребиотиков является использование лекарственных препаратов или биологически активных добавок к пище, содержащих чаще всего инулин и/или олигофруктосахариды или лактулозу. Ряд исследователей, чрезмерно идеализируя возможности пребиотической терапии, предлагает отказаться от применения пробиотиков и использовать только пребиотики [20].
Таким образом, в современном урбанизированном обществе большинство населения находится в условиях, способствующих формированию дисбиотических реакций в различных микробиоценозах. Одним из подтверждений важности проблемы может служить утвержденный приказом Минздрава России от 09.06.2003 г. № 231 Отраслевой стандарт «Протокол ведения больных. Дисбактериоз кишечника» (ОСТ 91500.11.0004–2003).
Существует ли возможность каким-то образом повлиять на вероятность возникновения или выраженность развивающихся негативных эффектов антибиотикотерапии. Концепция «снижения вреда» от применения антибиотиков может реализовываться по нескольким направлениям:
Обсуждая проблему оптимизации этиотропной терапии, следует помнить не только о необходимости назначения АМП строго по показаниям, выборе оптимальных разовых, суточных и курсовых доз, определении адекватной длительности терапии, но и использовании врачами современных знаний о фармакокинетике антибиотиков (всасывание, экскреция/выведение, распределение и метаболизм).
При парентеральном назначении большинство АМП не создает высокие концентрации в просвете кишечника, а следовательно, в наименьшей степени негативно действует на нормофлору этого эпитопа. Но основная масса антимикробных препаратов потребляется в амбулаторных условиях, и основным способом назначения этих препаратов служит энтеральный прием. Т. е. создаются предпосылки для более выраженного воздействия на кишечную микрофлору, особенно верхних отделов желудочно-кишечного тракта. Вместе с тем между препаратами существуют значимые различия в скорости и месте всасывания из просвета кишечника. Некоторые из них относятся к невсасывающимся, создающим достаточно высокие концентрации на всем протяжении желудочно-кишечного тракта (ванкомицин, неомицин, полимиксин М, рифаксимин). Часть препаратов характеризуется замедленным (тетрациклин, хлорамфеникол) или ограниченным всасыванием (ампициллин). Другие АМП создают повышенные концентрации в кишечнике за счет секреции с желчью или желудочным соком (фторхинолоны, нитрофураны, метронидазол, доксициклин). Знание врачом этих особенностей позволяет выбирать не только наиболее эффективный в конкретной клинической ситуации препарат, но и определять наиболее безопасный путь его введения.
Существуют ли основания для совместного применения антимикробных препаратов и пробиотиков.
Залогом успешного одновременного применения антибиотика и пробиотика является субпороговая (субэффективная) концентрация АМП в желудочно-кишечном тракте и/или определенная устойчивость пробиотика к АМП. Помимо того, что не все антибиотики, особенно назначаемые парентерально, создают эффективные концентрации в кишечнике, прежде всего в просвете и в пристеночном слое слизи, при пероральном приеме АМП возможно разделять по времени введение антибиотика и пробиотика (после того как концентрация антибиотика в просвете кишечника снизится до минимальной).
Кроме того, можно использовать сведения об устойчивости пробиотических штаммов к АМП.
Наибольшей устойчивостью к антибиотикам обладают сахаромицеты. Чаще всего применяются Saccharomyces boulardii, однако следует учитывать, что они чувствительны к противогрибковым препаратам. Определенным уровнем устойчивости к действию антимикробных препаратов обладают пробиотические штаммы бацилл (Bacillus), энтерококков (Enterococcus), лактобацилл (Lactobacillus) и в меньшей степени — бифидобактерий (Bifidobacterium) и кишечных палочек (Escherichia coli). Наибольший практический интерес в последних вызывают пробиотические штаммы энтерококков, число которых в Европе достигает нескольких десятков.
Безопасность применения энтерококковых пробиотиков обусловлена отсутствием факторов вирулентности у энтерококков, входящих в состав таких препаратов, как, например, Линекс и Ламинолакт [21]. Молочнокислые энтерококки, входящие в состав пробиотиков (Линекс и Ламинолакт), не адаптированы к длительной персистенции в организме человека. Учитывая естественную концентрацию энтерококков в кишечнике человека — 107–108 на грамм кишечного содержимого, для введения сколько-нибудь значимого количества пробиотиков, сравнимого с количеством собственных энтерококков, нужно в сотни раз увеличивать дозы приема. Пробиотические энтерококки не замещают естественную популяцию энтерококков и других представителей нормофлоры пациента, не передают ей и не принимают от нее никакие факторы патогенности. Исследования штаммов энтерококков, используемых в качестве пробиотиков (Линекс и Ламинолакт), выявили их низкий уровень генетической компетентности по сравнению с индигенными штаммами, что также снижает риск приобретения новых генетических маркеров.
Безопасность применения энтерококковых пробиотиков изучается в течение нескольких десятилетий. В результате сравнительного анализа штаммов установлено, что вирулентность энтерококков обусловлена наличием в их геноме ряда генов, расположенных на островах патогенности большого размера, состоящих в среднем из 154 000 нуклеотидных пар. На островах патогенности могут располагаться многие из известных генов, кодирующих факторы вирулентности: цитолизин (сylA, cylM), фактор аггрегации (agg), поверхностные белки (esp, asa1, efaA), сериновой протеиназы (sprE), феромона (fsrB), комплекс генов репарации ДНК, AraC-подобный регулятор транскрипции, компоненты системы PTS, гидролаза желчной кислоты и др. Набор генов в островке может различаться, но у авирулентных штаммов острова с таким составом генов отсутствуют. Если штамм не имеет такого острова в геноме, то он практически не представляет опасности (Shankar N., 2002). Недавние исследования штаммов энтерококков клинического происхождения в сравнении с аутоштаммами и штаммами пробиотиков (Ламинолакт, Линекс) показали, что штаммы энтерококков можно достаточно четко разделить на две большие генетические линии, разительно отличающиеся между собой. Исследования показали, что клинические штаммы отличаются от штаммов пробиотиков по характеру организации их генома, что можно установить с применением рутинных методов генетического анализа, таких как электрофорез в пульсирующем электрическом поле [21, 22].
Бифидобактерии и лактобациллы обладают менее широким спектром устойчивости к антимикробным препаратам, но и эти микроорганизмы могут применяться в составе схем комплексной терапии. Так, L. acidophillus, входящая в состав Линекса, характеризуется видовой устойчивостью к гентамицину, канамицину, стрептомицину; низкой чувствительностью к бацитрацину, клиндамицину, амоксициллину/клавуланату [23]. Как правило, пробиотические штаммы лактобацилл устойчивы к двум и более АМП [24, 25].
Не вызывает сомнений тот факт, что пробиотики обладают самостоятельной активностью, позволяющей применять их для лечения инфекционных диарей различного генеза. Анализ 63 исследований с общим количеством 8014 пациентов показал, что назначение пробиотиков при диарейных заболеваниях не сопровождается развитием нежелательных реакций. Пробиотики оказывали статистически достоверное влияние на длительность диареи, сохранение диареи в течение четырех и более дней и частоту стула на вторые сутки. Показано, что использование наряду со стандартной регидратационной терапией пробиотиков безопасно и обладает явным полезным эффектом, влияя на сокращение длительности острой инфекционной диареи и снижение частоты стула [26]. В сочетании с имеющимися сведениями об устойчивости пробиотиков к антимикробным препаратам давний спор о целесообразности совместного применения антибиотиков и пробиотиков для абсолютного большинства клинических ситуаций закончился в пользу назначения пробиотиков, особенно содержащих штаммы с предсказуемым спектром устойчивости к АМП, одновременно с началом этиотропной терапии, т. е. с первых суток лечения.
При назначении пробиотиков врач должен четко понимать, что эта группа препаратов не может давать значимый клинический эффект через 1–2 приема. Для достижения того или иного положительного результата требуется от нескольких суток до нескольких недель лечения в зависимости от поставленной цели. Кроме того, целью назначения пробиотика все чаще становится не исчезновение каких-то конкретных симптомов заболевания, а именно предупреждение негативных последствий лечения антибиотиками.
Например, если при «обычной» инфекционной диарее эффект заметен к исходу двух суток [26], то при проведении лечебно-профилактических мероприятий при ААД показана большая профилактическая эффективность S. boulardii [27], что позже было подтверждено в ходе проведенного метаанализа. Метаанализ эффективности и безопасности применения S. boulardii за период с 1976 по 2009 г. позволил идентифицировать 31 рандомизированное плацебо-контролируемое исследование с общим числом включенных пациентов 5029. Показано, что препараты на основе S. boulardii продемонстрировали статистически достоверно превышающую плацебо эффективность и безопасность в 84% оцениваемых случаев. По данным метаанализа был показан достоверный эффект от использования S. boulardii в профилактике антибиотик-ассоциированной диареи (относительный риск 0,47, 95% ДИ 0,35–0,63, р Купить номер с этой статьей в pdf
Пробиотики для кишечника: список препаратов
Ребенок появляется на свет со стерильным кишечником, но уже к году состав микрофлоры совпадает со взрослым человеком. На протяжении жизни под влиянием питания, болезней и других факторов баланс микроорганизмов в пищеварительном тракте изменяется, но постепенно восстанавливается до нормальных концентраций. Иногда этот процесс затягивается. Тогда врач может рекомендовать пребиотики и пробиотики для кишечника.
Виды пробиотиков
Для восстановления кишечника применяют два типа лечебных средств. Пробиотики – это препараты, которые содержат полезные бактерии в высушенном или растворенном виде. Чаще всего это микроорганизмы из рода Lactobacillus и Bifidobacterium, которые в норме доминируют в пищеварительном тракте человека.
Пребиотиками называются вещества, необходимые для роста хорошей микрофлоры. В некоторых случаях без них можно обойтись, но после тяжелых болезней, лечения антибиотиками или отравления они ускорят восстановление за счет создания благоприятной среды для бактерий.
В пищеварительном тракте здорового взрослого человека обитает несколько десятков видов бактерий, но преобладают два типа микробов: бифидобактерии и лактобактерии. Другие находятся в меньшинстве. Поэтому выделяют следующие виды пробиотиков в зависимости от состава:
Восстанавливать нормальную микрофлору можно разными формами препаратов. Пробиотики выпускают в сухой форме, из которой перед применением самостоятельно готовят суспензию. Существуют готовые жидкие формы лекарства, которые удобно давать маленькому ребенку. Некоторые средства производят в капсулах в желатиновой оболочке. Она не повреждается в желудке и растворяется только в кишечнике. Это защищает бактерии от действия соляной кислоты.
Создание препаратов для решения проблем с пищеварением проходило в несколько этапов. Поэтому фармацевты выделяют несколько поколений пробиотиков:
Какой препарат подойдет в конкретном случае, должен решать врач с учетом состояния пациента, его возраста. Для взрослых требуется большая дозировка и кратность приема пробиотиков.
ТОП-10 лучших пробиотиков
В аптеках продается большое количество пробиотиков, из которых тяжело выбрать нужный препарат. Правильное решение – обратиться к врачу-гастроэнтерологу или терапевту, чтобы назначили лекарственное средство с хорошим эффектом.
Чтобы решить, какой из них лучше, можно ориентироваться на список ТОП-10:
Советы по выбору
Какой из перечисленных пробиотиков поможет справиться с проблемами пищеварения, зависит от заболевания. Если организму необходима помощь после курса лечения антибиотиками, лучше использовать комплексные препараты, где добавлен пребиотик. Он ускорит заселение бактериями слизистой кишечника.
Вне зависимости от названия, для взрослых походят препараты в виде порошка, капсул или раствора. Капли разработаны специально для маленьких детей, которым необходима небольшая доза препарата. Их хорошо смешивать с напитками или молоком матери.
При использовании средств с пробиотическими эффектами, симптомы вздутия живота, урчания, метеоризм могут усилиться из-за процесса брожения. Но это проходит самостоятельно и не требует отмены терапии. Если на фоне приема пробиотиков появилась аллергическая сыпь, лечение прекращают.
КИШЕЧНЫЙ ДИСБАКТЕРИОЗ
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Нормальная микробная флора кишечника
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
Клинические особенности дисбактериоза
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Основным симптомом псевдомембранозного колита является обильная водянистая диарея, началу которой предшествовало назначение антибиотиков. Затем появляются схваткообразные боли в животе, повышается температура тела, в крови нарастает лейкоцитоз. Эндоскопическая картина псевдомембранозного колита характеризуется наличием бляшковидных, лентовидных и сплошных «мембран», мягких, но плотно спаянных со слизистой оболочкой. Изменения наиболее выражены в дистальных отделах ободочной и прямой кишок. Слизистая оболочка отечная, но не изъязвлена. При гистологическом исследовании обнаруживают субэпителиальный отек с круглоклеточной инфильтрацией собственной пластинки, капиллярные стазы с выходом эритроцитов за пределы сосудов. На стадии образования псевдомембран под поверхностным эпителием слизистой оболочки возникают экссудативные инфильтраты. Эпителиальный слой приподнимается и местами отсутствует; оголенные места слизистой оболочки прикрыты лишь слущенным эпителием. На поздних стадиях болезни эти участки могут занимать большие сегменты кишки.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
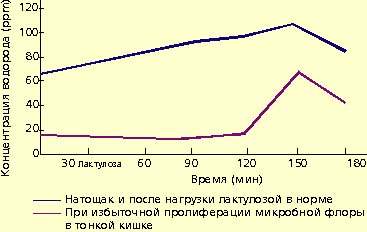 |
| Рисунок 1. Концентрация водорода в выдыхаемом воздухе |
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
 |
Лечение
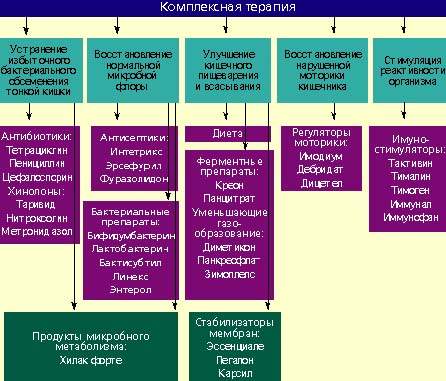
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Совсем недавно появились сообщения о возможности лечения острой диареи, ассоциированной с антибактериальной терапией и Cl. difficile, большими дозами пре- и пробиотиков.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.

