эндоваскулярное лечение аневризм головного мозга
Эндоваскулярное лечение аневризм головного мозга
а) Методы эндоваскулярного лечения аневризмы сосуда головного мозга. Попытки окклюзии аневризмы при помощи отделяемого баллона в 1980-х годах сопровождались высокими рисками и не предотвращали повторное кровоизлияние. Введение Guglielmi отделяемых спиралей (GDC) в 1990 г. оказалось намного более безопасной и более эффективной альтернативой. Платиновые спирали вводятся через катетер в дно аневризмы и отделяются электролитически. «Плотная упаковка» аневризмы несколькими спиралями занимает менее одной трети фактического объема, но этого достаточно, чтобы предотвратить повторное кровотечение у большинства пациентов.
Примерно в одной трети случаев радиологи специально оставляют заполнение шейки аневризмы в связи с риском окклюзии спиралью проксимального сосуда, в этом случае риск повторного кровоизлияния выше.
Приблизительно в 5% случаев эмболизация аневризмы не удается. Аневризмы подходят для эмболизации если соотношение дно/ширина шейки больше чем 2:1. Радиологи могут выбирать спирали разного диаметра и ЗЭ-формы. Как правило, требуется от четырех до пяти спиралей, но возможное количество варьируется от одной спирали для 3 мм аневризмы до 20 спиралей для гигантских аневризм.
1. Коррекция с помощью баллона. Этот метод, разработанный Moret, позволяет эмболизировать аневризмы с широкой шейкой. Периодическое раздувание баллона на отдельном катетере в несущем сосуде предотвратцает выпадение спиралей в просвет сосуда. По окончании процедуры спирали сохраняют форму, приданную им баллоном. Некоторые центры используют эту технику в 30-40% случаев эндоваскулярной хирургии.
2. Биоабсорбирующие полимеры. Новые разработки включают в себя использование биоабсорбирующего полимерного покрытия вокруг спирали (Matrix) или в спирали (Cerecyte). Экспериментальные работы на животных показали, что эти полимеры стимулируют регенерацию клеток, способствуют организации тромба в аневризме и стимулируют образование новой интимы. Будут ли эти спирали улучшать общие результаты, остается неопределенным, эта информация будет получена в ходе исследований.
3. Гидрогелевые и волокнистые спирали. Гидрогелевые спирали покрыты гидрофильным полимером, расширяющимся при контакте с кровью, что помогает заполнить просвет аневризмы. Кроме того, спирали с волокнами дакрона или нейлона вызывают более тромбогенную реакцию, чем платина, однако все эти новые технологии ждут дальнейших исследований.
4. Интракраниальные стенты. Введение в практику стентов подходящего размера и достаточной гибкости для прохождения через внутричерепные сосуды предоставило другую альтернативу для аневризм, имеющих широкую шейку, гигантских или веретенообразных аневризм, особенно развивающихся из внутренней сонной артерии или развилки основной артерии. После установки стента микрокатетером можно пройти через стент в полость аневризмы, чтобы разместить в ней спираль без риска окклюзии просвета сосуда. Для предотвращения тромбоза стента назначается пожизненная антитромбоцитарная терапия.
5. Оникс. Оникс — жидкий полимер, который затвердевает при контакте с кровью, может быть введен в аневризму, если ее шейка защищена баллоном или стентом. Теоретически метод весьма привлекателен, но первые исследования показали высокий уровень сложности выполнения, что ограничивает его более широкое применение.
6. Отдаленные результаты эндоваскулярной хирургии. При любых вмешательствах необходимо проведение контрольной ангиографии, как правило, через шесть месяцев после лечения. Реканализация аневризмы за счет уплотнения или миграции спиралей требует повторного вмешательства примерно у 10% пациентов.
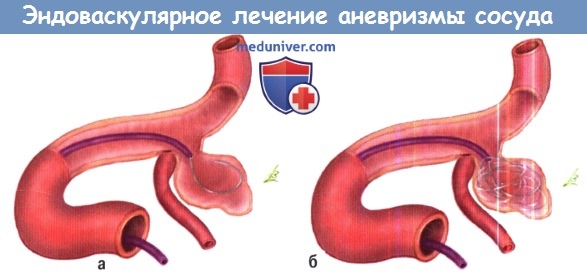
Б. Введение последующих спиралей.
б) Выбор эндоваскулярного метода лечения аневризмы сосуда головного мозга. Изначально, в 1990-х годах эндоваскулярное лечение предназначалось для неоперабельных аневризм. Данная методика лечения чаще используется для тех аневризм, которые трудно лечить открытым путем, в частности, аневризм заднего обращения, несмотря на все убедительные доказательства большей радикальности. Международное исследование аневризматического САК (ISAT)—клипирование против койлинга, началось в 1994 г. Комитет по мониторингу данных остановил сбор информации в 2001 г. после того, как центры изучили данные 2143 пациентов.
Исследование показало, что через один год после эндоваскулярной эмболизации абсолютный риск смерти снизился на 7% (относительный риск снижался на 23%) по сравнению с пациентами, перенесшими клипирование. Значительно больше повторных кровоизлияний и более высокая смертность от повторного кровоизлияния имели место в течение первого года в группе койлинга, однако исследователи по-прежнему выступают за данную методику. Несмотря на отсутствие долгосрочных результатов и то, что пациенты выбранной группы почти всегда имели хороший соматический и неврологический статус, а также небольшую аневризму переднего отдела вилизиева круга, в Великобритании резко сменилась тактика лечения в пользу эмболизации; доля операций внутрисосудистым методом увеличилась с 37 до 54%. Во многих центрах этот показатель в настоящее время превышает 80%.
Последующее семимилетнее наблюдение за пациентами ISAT показало, что выживаемость за это время выше, несмотря на повышенный риск позднего повторного кровоизлияния в эндоваскулярной группе.
Лечение аневризм проводится бригадой специалистов, состоящей из интервенционных радиологов и нейрохирургов. Даже если бы не было разницы в результатах между этими двумя методами лечения, большинство пациентов выбрали бы наименее инвазивный подход. Результаты ISAT подтверждают использование эмболизации в качестве метода первой линии. Тем не менее, не все аневризмы подходят для эндоваскулярного лечения. Следующие факторы делают эмболизацию более трудной или невозможной:
— Аневризма средней мозговой артерии
— Аневризмы с широкой шейкой и соотношением тело/ширина шейки менее чем 2:1
— Аневризмы 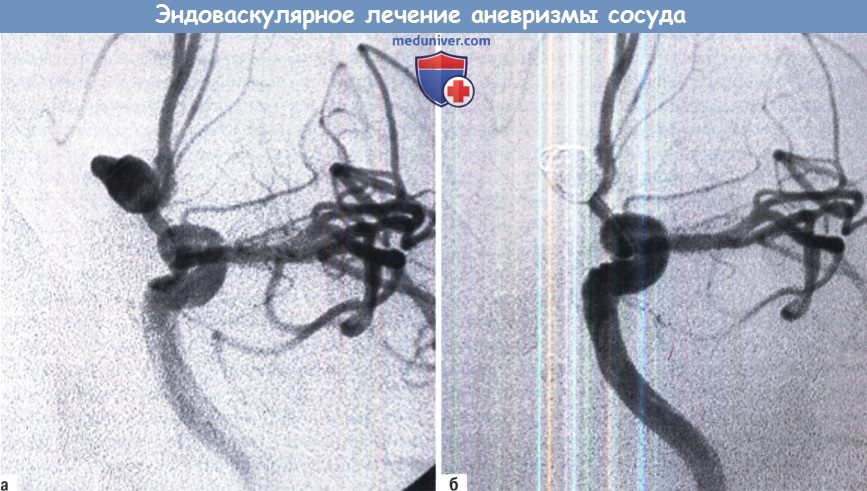
Б. Завершающая стадия эмболизации спиралями, показывающая дно, заполненное спиралями.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гид по эндоваскулярному лечению сосудистых заболеваний головного мозга
Эндоваскулярное лечение сосудистых заболеваний головного мозга
Малоинвазивные вмешательства: эмболизация и стентирование
В большинстве случаев, эндоваскулярная эмболизация – наименее инвазивный на сегодня метод лечения аневризм сосудов головного мозга.
Рис. Эмболизация при аневризме
Проведение внутрисосудистой спиральной эмболизации возможно при мешковидной аневризме и небольшом просвете соустья. При широком просвете возможно одновременное наложение стента (закрытие просвета) с последующей спиральной эмболизацией аневризмы.

В любом случае, тактику выбирает нейрорадиохирург после проведения ангиографии.
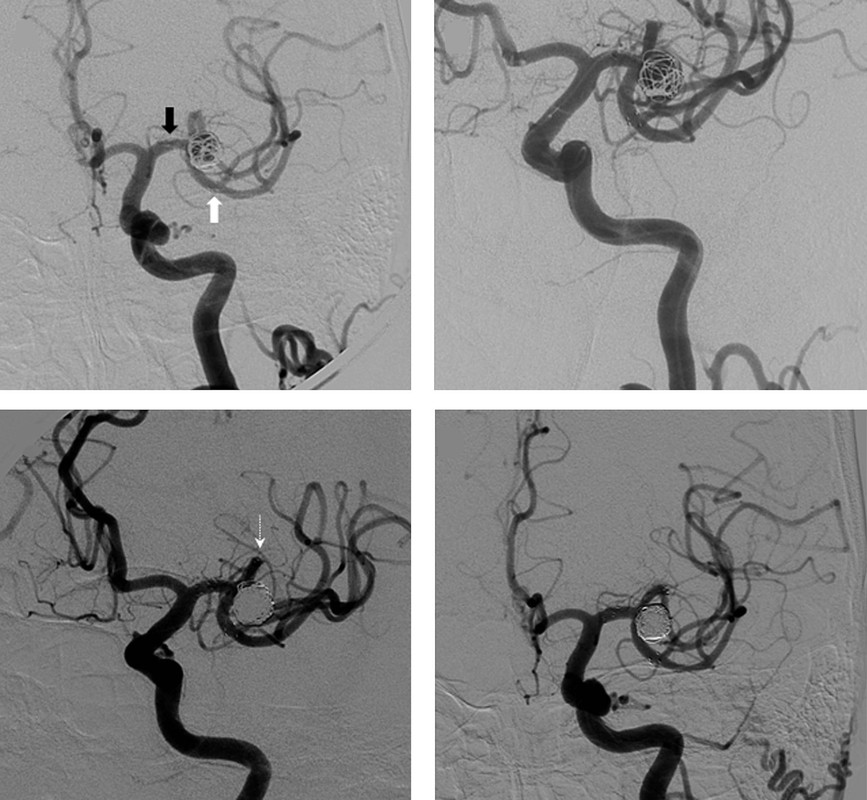
В процессе эмболизации через удобный сосудистый доступ (чаще паховый) под радиологическим контролем вводится катетер и проводится до аневризмы. Затем в катетер вводится более тонкий микро-катетер с уложенной внутри него проволочной микроспиралью, и заводится в полость аневризмы.
Как только кончик микрокатетера окажется в полости аневризмы, из микрокатетера высвобождается микроспираль, которая изменяет свою форму, и в виде беспорядочного мотка проволоки занимает собой полость аневризмы. При больших размерах аневризмы может понадобиться несколько спиралей. Заполненная проволочной спиралью аневризма выключается из кровотока и постепенно зарастает соединительной тканью, то есть, исключается возможность ее разрыва.
Через прокол бедренной артерии по сосудам осуществляется доступ к объемному образованию. Процедура безболезненна и проводится без использования наркоза, под местной анастезией. С помощью специальных веществ (эмболизирующих материалов) сосуды, питающие опухоль, «заклеиваются», после чего образование перестает расти.
Процедура применяется как самостоятельный метод лечения, а также как первый этап перед удалением опухоли.
При каких заболеваниях головного мозга применяется процедура эмболизации?
Современные достижения эндоваскулярной хирургии позволяют рассматривать этот метод как первый шаг в лечении таких заболеваний, как артериовенозная мальформация (АВМ) сосудов головного мозга, аневризма головного мозга, артериовенозная фистула.

Рис. Дуральная артериовенозная фистула
Специалистами используется малоинвазивное эндоваскулярное вмешательство для облитерации («заклеевания» жидким пластиком или клеевым составом) просвета фистулы. Метод применяется когда открытое оперативное вмешательство невозможно из-за труднодоступности патологии, а также если пациент в тяжелом состоянии.
Аневризмы — одна из самых распространенных болезней сосудов головного мозга. Это истончение и выпячивание стенки артерии головного мозга. Самым опасным его проявлением может стать спонтанный разрыв аневризмы с кровоизлиянием в мозг. В таких случаях прогноз без высокотехнологичного лечения крайне неутешительный.

Рис. Аневризма
К сожалению, около 15% пациентов погибают в первые сутки, еще до поступления в стационар, у остальных в ближайшие полгода происходит повторное кровоизлияние, следом в 80% случаев летальный исход.
Стентирование
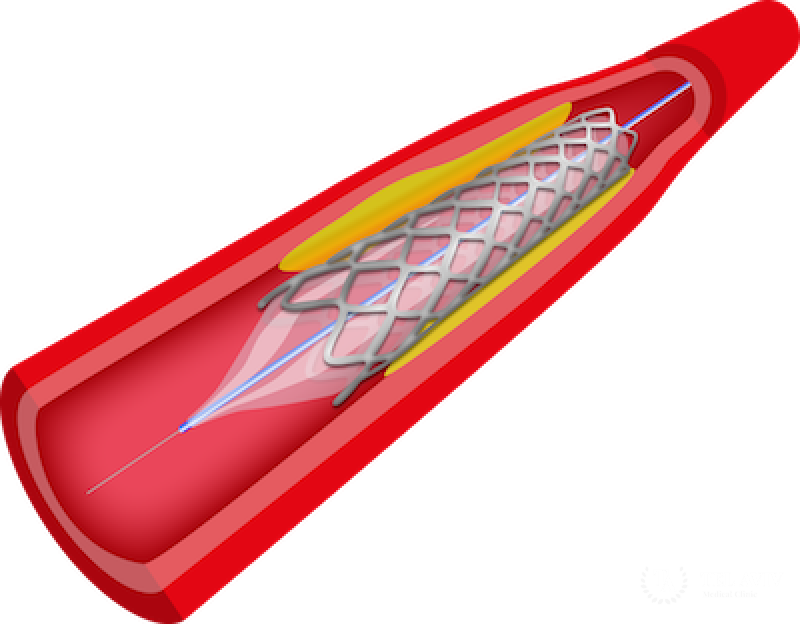
Стентирование сонной артерии – это процедура, заключающаяся в установке в просвет суженного сосуда тонкой проволочной конструкции в виде цилиндра, играющей роль каркаса – стента.

Через катетер хирург вводит проводник со сдутым баллоном и стентом в пораженный участок. После проведения в место сужения баллончик со стентом расширяется до нормального диаметра сосуда. Имплантированный стент прижимается к стенкам сосуда и остается в этом положении, обеспечивая нормальный кровоток.
Процедура выполняется под местной анастезией и контролируется с помощью рентген-мониторов.
При каких заболеваниях головного мозга применяется процедура стентирования?
Процедура стентирования сосудов головного мозга проводится при сужении сонных артерий (атеросклерозе)
Рис. Атеросклероз сосудов головного мозга
Лечение аневризмы головного мозга
Содержание:
Аневризма – патологическое состояние, при котором происходит растяжение стенок артериальных сосудов. При аневризме сосудов головного мозга повреждаются внутричерепные сосуды.
Заболевание протекает по 2 типам:
Течение заболевания по типу опухоли характеризуется симптомом сдавливания. Аневризма увеличивается в размерах и повреждает черепно-мозговые нервы (глазодвигательные, тройничный, лицевой). Течение заболевания с разрывом сосуда характеризуется кровоизлиянием в субарахноидальное пространство или в вещество головного мозга.
Диагноз выставляется на основе жалоб, анамнеза, клинических симптомом, данных компьютерной томографии, МРТ, рентгена. При наличии показаний к операции удаления проводят оперативное лечение: клипирование и эндоваскулярное удаление. С 1999 года в России внедряется классификация международных болезней 10 пересмотра. Аневризма сосудов головного мозга имеет персональный код по МКБ-10 I67.1.
Распространенность
Точную распространенность болезни выявить невозможно. Аневризма часто протекает без каких-нибудь специфических и неспецифических симптомов. Обнаружить такое повреждение возможно только после смерти человека на вскрытии, 50 % случаев находятся именно таким способом.
Распространенность аневризмы в мире составляет 10-15 человек на 100 000 населения.
После разрыва артерии в субарахноидальное пространство моментальная летальность пациентов равняется 15 %. 25 % больных с разрывов скончаются в течение первых 2 дней после происшествия, а 50 % в течение следующих 3 месяцев. Аневризма может появиться у человека или быть у него с рождения. Разрыв происходит в преклонном возрасте к 60 годам.
Причины
Главным звеном в патогенезе болезни является истончение слоев стенки сосудов. Стенка не может сопротивляться и подстраиваться под артериальное давление и начинает растягиваться. Растяжение ускоряется из-за наполнения полости кровью, образуется вихревой кровоток.
Причинами, которые спровоцирует процесс, могут стать различные болезни:
Клинические проявления аневризмы
Главные симптомы связаны с большими размерами аневризмы. Она начинает сдавливать ткани головного мозга. Поэтому если размеры маленькие, то признаков заболевания не будет. Диагностика аневризмы в этом случае носит случайный характер.
При быстром росте образования появляются симптомы:
Аневризма может разорваться. На это влияют несколько причин: быстрое повышение артериального давления, стрессовая ситуация, травма, лихорадка, злоупотребление никотином или алкоголем.
При разрыве человек чаще всего теряет сознание и наступает коматозное состояние. Тяжесть течения заболевания зависит от размеров и месторасположения образования. Если аневризма находилась в субарахноидальном пространстве, то будет субарахноидальная гематома. Клинически это проявится симптомами сдавливания. Если местоположение выпячивания сосудов находилась в веществе головного мозга, наступит геморрагический инсульт. Это более тяжелое состояние.
Симптомы разрыва аневризмы:
При первых симптомах разрыва необходимо доставить человека в больницу или вызвать скорую. Первая доврачебная помощь заключается в том, что нужно уложить больного с возвышенным головным концом, обеспечить приток свежего воздуха, расстегнуть и снять все одежду, которая мешает человеку дышать, проверить проходимость верхних дыхательных путей.
Осложнения заболевания
Аневризма сосудов головного мозга может приводить к серьезным жизнеугрожающим осложнениям:
Диагностика
Заболевание часто носит бессимптомный характер, поэтому обнаружение аневризмы головного мозга — трудная задача. Врач должен подумать о наличии данного образования у пациента, если у него присутствуют сильные головные боли, нарушение функций мозговых структур, судороги.
При подозрении пациента направляют на специальные инструментальные методы исследования: КТ, МРТ, рентгеновское исследование, электроэнцефалография.
Самыми главными и информативными являются методы компьютерной томографии и магнитно-резонансной томографии. На снимках можно увидеть параметры аневризмы сосудов головного мозга:
Высокое диагностическую ценность имеет рентгеновское исследование с введением контрастного вещества в сосуды головного мозга. На рентгеновском снимке можно увидеть толщину сосудистой стенки, наличие тромба в просвете сосуда, растяжение интимы и адвентиции артерий.
Рентген позволяет провести дифференциальный диагноз на ранних сроках развития болезни, отличить злокачественное новообразование от аневризмы головного мозга. Рентгеновское излучение даже в небольших дозах действует на организм с появлением отрицательных эффектов. Беременным женщинам, пациентам детского возраста, пациентам, у которых присутствуют другие заболевания предпочтительнее проводить КТ и МРТ.
Электроэнцефалография регистрирует биологические потенциалы головного мозга, показывает активность белого и серого вещества. При нарушениях функций мозга, выявленных по результатам ЭЭГ, у пациента можно заподозрить аневризму головного мозга и отправить на дополнительные исследования, например, МРТ, где диагноз I67.1 подтвердится. Электроэнцефалография не оказывает отрицательных эффектов на организм человека.
Лечение аневризмы головного мозга
Лечение такого дефекта сосудов заключается в проведении хирургической операции и удалении аневризмы. Операция считается обязательной процедурой, если размеры выпячивания достигают 7 мм. В ходе операции дефект удаляется, целостность сосудов головного мозга восстанавливается.
Существует несколько методов хирургических операций при той болезни: клипирование и эндоваскулярное удаление.
Клипирование
Клипировние – микрохирургическая операция, является самым часто используемым методом лечения неразорвавшихся аневризм.
Суть операции заключается в том, что хирург вскрывает череп, находит местоположение аневризмы и удаляет ее. Операция несет большие риски для жизни пациента. Оперативное вмешательство состоит из нескольких этапов:
Эндоваскулярное удаление
Эндоваскулярные операции проводятся только в высокотехнологических центрах. Для этой манипуляции требуется особое специализированное оборудования, а также квалифицированные специалисты. Клиника МЕДСИ удовлетворяет всем требованиям для проведения операции по эндоваскулярному удалению аневризмы.
Трепанация черепа для этого варианта операции не проводится. До аневризмы хирург добирается через магистральные сосуды. Катетер вводится в сонную или бедренную артерии и продвигается до головного мозга. Операция проводится под контролем ультразвуковой допплерографии или КТ. Игла с катетером доводится до аневризмы, с помощью баллонов она выключается из общего кровотока, и хирург удаляет аневризму.
Отделить аневризму от общего кровотока можно еще одним способом. В артерию пускается особое химическое вещество, которое достигает выпячивания в головном мозгу, образуют эмболы в артерии.
У высокоспециализированной технологии есть ряд преимуществ:
Операция может иметь в себе модификации, авторские методики.
Каждая операция-это риск осложнений. При эндоваскулярном удалении аневризмы сосудов головного мозга также возможны осложнения:
Послеоперационный период
После операции у пациента могут появиться последствия удаления аневризмы головного мозга:
Самой частой проблемой в послеоперационном периоде считается тромбообразование. После наложения клипсы или шва на сосуд, могут оседать атеросклеротические бляшки, которые закроют просвет сосуда и приведут к ишемии мозга.
Также в ранний период после операции могут разойтись швы, что грозит кровоизлиянием в мозговое вещество или субарахноидальное пространство.
Прогноз послеоперационного периода
После операции пациенту необходимо отказаться от приема никотина, алкоголя, избегать стрессовых ситуаций, соблюдать диету с пониженным содержанием жиров.
Если у пациента случился рецидив, и появилась новая аневризма, то больному противопоказаны занятия физической культурой, чтобы избежать повышения артериального давления. Отказ от физической нагрузки нужно соблюдать до проведения следующей операции.
Реабилитационный процесс пациентов
Пациенту после перенесенного разрыва выпячивания сосудов головного мозга требуется проведение реабилитации. Методики, которые используются в реабилитационном курсе:
Если имеются показания к применению физиотерапевтических процедур, то их включают в общий реабилитационный курс.
ЗАДАЙТЕ ВОПРОС запишитесь на приём
Запишитесь на консультацию врача-нейрохирурга по телефону:
Эмболизация аневризмы
Эмболизация — это малоинвазивная процедура, являющаяся альтернативой хирургии. Она показана в случаях, когда выполнение открытого оперативного вмешательства очень травматично или чревато осложнениями. В нейрохирургии эндоваскулярная эмболизация аневризмы головного мозга всё больше вытесняет операции с трепанацией черепа.
Цель эмболизации аневризмы заключается в предотвращении кровотока в аневризматическом мешке путём заполнения его полости специальными спиралями. Это должно предотвратить разрыв и кровотечение. Эндоваскулярная эмболизация аневризмы головного мозга не восстанавливает области уже повреждённого мозга.
Материалами для окклюзии служат спирали, специальные губки или гистоакрил. Для лечения аневризмы обычно используются спирали, либо эмболизирующее вещество.
Спирали бывают разной конфигурации, длины и диаметра. Структурные спирали изготавливают из платины, которая при введении в сосуд сворачивается в трёхмерную фигуру для заполнения полости аневризмы.
Могут потребоваться дополнительные устройства, такие как стент, чтобы помочь удержать спирали внутри аневризмы. Вмешательство с помощью стента подразумевает постоянное размещение его в сосуде, прилегающем к аневризме, для обеспечения поддержки, которая удерживает спирали внутри мешка. Самыми сложными технологиями пользуются для эмболизации аневризм сосудов головного мозга, потому что риски заболевания очень высоки, а доступ к ним, открытым методом очень затруднён.
Подготовка к лечению
 Как проходит лечение
Как проходит лечение
После местной анестезии врач вставляет полую пластиковую трубку (катетер) в в бедренную артерию и продвигает его, используя ангиографию, до места аневризмы.
Используя направляющий катетер,спирали платиновой проволоки или маленькие латексные шарики проводят через катетер и вводят их в аневризму. Они заполняют аневризматический мешок, выключая его из кровообращения, вызывая образование сгустка крови (тромба), который полностью пломбирует полость аневризмы. Мягкость платины позволяет спирали соответствовать причудливой форме мешка. Для полного его заполнения требуется в среднем 5-6 спиралей.
Средняя продолжительность процедуры составляет 1-2 часа.
Когда шейка аневризмы слишком широка иногда требуется установить стент в основной сосуд, чтобы удерживать спирали внутри мешка. Поскольку стент действует как барьер между аневризмой и материнским сосудом, очень маловероятно, что из неё будут выступать катушки.
Возможные осложнения
Прогноз
Эффективны как открытая хирургия, так и эндоваскулярные методы. Выбор лечения зависит от ряда факторов: есть ли риск разрыва аневризмы, её размер, форма и местоположение. Как и все медицинские решения, наилучший вариант лечения следует обсудить с вашим врачом.
Процедуру иногда требуется выполнить несколько раз в течение жизни пациента.
Лечение неразорвавшихся аневризм головного мозга
Общая информация
Краткое описание
Ассоциация нейрохирургов России
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ НЕРАЗОРВАВШИХСЯ АНЕВРИЗМ ГОЛОВНОГО МОЗГА (Москва, 2015)
Клинические рекомендации утверждены на Пленуме Правления Ассоциации нейрохирургов России 14.10.2015 г. Красноярск
Введение
В последние годы число обращений пациентов с неразорвавшимися аневризмами (НА) в нейрохирургические учреждения неуклонно возрастает. Опубликованные в зарубежной литературе серии по анализу этой патологии содержат до нескольких сотен, а кооперативные исследования – до нескольких тысяч больных.
Учитывая, что неразорвавшиеся аневризмы потенциально могут стать источником внутричерепного кровоизлияния, возникла необходимость определения тактики ведения и лечения этих больных. Единой точки зрения по этому вопросу не существует, хотя в последние годы рекомендации различных клиник все более совпадают по различным позициям и становятся более конкретными. Основной проблемой при выявлении неразорвавшейся аневризмы является оценка вероятного риска ее разрыва. Несмотря на опубликованные незначительные показатели первичных кровоизлияний из ранее неразорвавшихся аневризм [28, 75, 90], существуют группы больных с высоким риском разрыва аневризм. К таким факторам риска относят как морфологические особенности выявленной аневризмы (несколько куполов, неровность тела аневризмы, соотношение размера аневризмы к диаметру несущего сосуда, расположение, большой и гигантский размеры, увеличение размеров аневризмы с течением времени и т.д.), так и семейный анамнез кровоизлияния из аневризмы, наличие ряда вредных привычек, таких как курение, присутствие сопутствующих заболеваний (артериальная гипертензия). Существенное увеличение пациентов с диагностированными неразорвавшимися аневризмами в РФ и накопление значительного опыта хирургического лечения этой патологии явилось обоснованием для создания российского рекомендательного протокола по ведению и лечению больных с НА.
Этиология и патогенез
В настоящее время этиология и патогенез НА рассматриваются в рамках этиологии и патогенеза аневризм в целом. Факторы, лежащие в основе заболевания, принято делить на немодифицируемые и модифицируемые. К первым относят: генетические факторы [12, 26, 100]; ряд наследственных заболеваний [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]; возраст и пол [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115]. Во вторую группу входят: артериальная гипертония, курение, алкоголь, лекарства и вещества с симптомиметическим действием, пероральные контрацептивы [31, 32, 36, 45, 52, 53, 114]. Доказательность степени влияния этих факторов на формирование аневризм, в том числе, неразорвавшихся, различна.
Эпидемиология
Факторы и группы риска
Группы повышенного риска выявления НА
Пол и возраст
Частота выявления НА увеличивается с возрастом, достигая максимума в возрастной группе от 50 до 60 лет. Чаще аневризмы выявляются у женщин, в независимости от возрастной категории [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115].
Сопутствующие заболевания
Пациенты с перечисленными ниже заболеваниями входят в группу повышенного риска обнаружения неразорвавшихся аневризм [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]:
— аутосомно-доминантный поликистоз почек (частота обнаружения аневризм в 3-14 раз выше по сравнению с основной популяцией)
— синдром Элерса-Данло IV типа
— синдром Марфана
— коарктация аорты
— двустворчатый аортальный клапан
— эластическая псевдоксантома
— наследственная геморрагическая телеангиэктазия
— нейрофиброматоз 1 типа
— недостаточность α1-антитрипсина
— фиброзномышечная дисплазия
— феохромацитома
— сидром Кляйнфельтера
— туберозный склероз
— Синдром Нунан (наследственное сочетание стеноза клапанов лёгочной артерии, гипертелоризма, оттопыренных ушных раковин и др. нарушений)
— недостаточность α-глюкозидазы
— первичная карликовость с микроцефалией и остеодисплазией
— внутричерепные артериовенозные мальформации
«Семейные аневризмы»
По данным различных исследований [9, 55, 56, 76-78, 83, 86, 94] частота встречаемости «семейных аневризм» составляет от 7 до 20% в зависимости от различных методов оценки семейного анамнеза и анализа полученных данных. Чаще выявляют неразорвавшиеся аневризмы среди родственников первого поколения пациента с разрывом аневризмы – около 4% [74, 94], с некоторой большей встречаемостью среди сибсов пациента, чем среди его детей.
К факторам, повышающим вероятность обнаружения аневризмы среди родственников больного, перенесшего САК, относят следующие: старший возраст, женский пол, курение, наличие в анамнезе гипертонической болезни, гиперхолестеринемия, семейный анамнез поликистозной болезни почек, семейный анамнез наличия САК или аневризмы у 2 и более родственников [74]. Частота выявления неразорвавшихся аневризм у родственников первой степени родства при наличии в анамнезе аневризм и/или САК у 2 и более членов их семей составляет от 8,7% [76] до 19,1% (старше 30 лет, наличие таких отягощающих факторов, как курение и гипертоническая болезнь) [9].
Риск разрыва аневризмы
Таблица 1. Риск разрыва НА в зависимости от ее размера и локализации (по данным ISUIA [114]).
| Пятилетний кумулятивный риск разрыва в соответствии с размером и расположением аневризмы | |||||
| 7-12 мм | 13-24 мм | 25 мм | |||
| Группа 1 | Группа 2 | ||||
| Кавернозный отдел ВСА (n=210) | 0 | 0 | 0 | 3.0% | 6.4% |
| ПСА и ПМА/СМА/ВСА | |||||
(n=1037)
средняя мозговая артерия, ВСА – внутренняя сонная артерия, ВББ – вертебробазилярный бассейн, ЗМА – задняя мозговая артерия, ЗСА – задняя соединительная артерия
Группа 1 – пациентов без САК
Группа 2 – пациенты с САК в анамнезе при разрыве другой аневризмы
Предрасполагающие факторы риска разрыва аневризмы
Рост аневризмы
К факторам, ответственным за рост аневризм с течением времени, относят повышенное АД, гемодинамический стресс в зависимости от формы аневризмы и ее расположения, изначальный размер аневризмы, воспаление в стенке аневризмы, женский пол, курение, молодой возраст, избыточное употребление алкоголя. Отмечается повышенный риск роста аневризм у пациентов с наличием инсульта или транзиторной ишемической атакой в анамнезе, и при выявлении множественных аневризм [39, 58, 89].
Проспективное исследование, проведенное в США и включавшее пациентов с аневризмами диаметром менее 7 мм и без наличия САК в анамнезе (всего 319 аневризм) не зафиксировало ни одного разрыва аневризмы за период наблюдения в течение 2,4 лет. Однако за период наблюдения был отмечен рост аневризмы как минимум на 0,75 мм у 5,4% пациентов в течение года [10].
Отмечено, что ежегодный риск разрыва «растущей» аневризмы может превышать данный показатель у аневризмы без роста в 12 раз [58, 71, 104].
Морфологические параметры и локализация
Наибольшая частота кровоизлияний характерна для аневризм в вертебробазилярном бассейне, в области ПСА и перикаллезной артерии [111,121]. Аневризмы в области СМА менее подвержены риску разрыва.
Больший риск разрыва аневризмы отмечают при выявлении следующих морфологических параметров: больший размер, неправильная форма и/или наличие дивертикулов, узкая шейка аневризмы, соотношение максимального размера аневризмы к диаметру несущей артерии более 2,05, соотношение высоты аневризмы к диаметру шейки более 1,6 [47, 80, 111, 121].
Другие факторы
Факторами риска разрыва НА являются молодой возраст, курение, артериальная гипертензия, женский пол, наличие в анамнезе САК из другой аневризмы, семейный анамнез САК [10, 61].
Клиническая картина
Cимптомы, течение
НА наиболее часто определяются в ходе обследования больных после кровоизлияния из другой аневризмы, а также при наличии у больного неврологической симптоматики или возникновения внезапной головной боли или изменения ее характера. В исследовании ISUIA неразорвавшаяся аневризма была выявлена у пациентов в ходе обследования по поводу кровоизлияния из другой аневризмы (30.4%), головной боли (23.7%), ТИА или ОНМК по ишемическому типу (10.5% и 10.6% соответственно), поражения черепных нервов (8.0%), судорожных припадков (2.9%), появления симптомов объемного образования головного мозга (2.7%), субдуральной или внутримозговой гематомы (1.2%), опухоли головного мозга (0.8%), демиелинизирующих заболеваний головного мозга (0.4%) и неопределенных “приступов” (7.1%) [114].
Характер проявления НА влияет на естественное течение заболевания и на выбор тактики лечения. Отмечено, что среди неразорвавшихся симптомных аневризм риск кровоизлияния в 4 раза выше по сравнению с асимптомными, случайно выявленными, аневризмами [111].
Диагностика
Диагностика
Возможности методов нейровизуализации аневризм резко расширились в последнее десятилетие, включая применение дигитальной субтракционной ангиографии в 2D и 3D режимах, МР-ангиографии и КТ-ангиографии.
После выявления неразорвавшейся аневризмы необходимо оценить ее анатомические особенности (и, что возможно будет доступно в широкой практике в будущем, гемодинамические параметры) как при первичном исследовании, так и при обследовании в динамике для определения дальнейшей тактики лечения [22, 63, 122].
Методы обследования
Компьютерная томография в ангиографическом режиме (КТ-ангиография)
Чувствительность, специфичность и точность КТ-ангиографии в диагностике аневризм составляет 96.3%, 100% и 94.6% соответственно. При милиарных аневризмах размером менее 3 мм эти показатели составляют 81.8%, 100% и 93.3% соответственно [108].
При проведенном в 2003 мета-анализе 21 исследования, включавших 1251 пациентов, выявлено, что чувствительность и специфичность КТ-ангиографии составляет 93.3% и 87.8% соответственно в сравнении с цифровой церебральной ангиографией [14]. Выполнение КТ-ангиографии позволяет оценить наличие кальцификатов в стенке аневризмы и тромбов в ее полости [70]. Однако 3D-реконструкция может не совсем точно отражать истинную анатомию и размеры шейки/купола/несущего сосуда, особенно при аневризмах малых размеров (менее 5 мм) [29].
Дигитальная субтракционная ангиография (ДСА)
ДСА остается «золотым стандартом» в диагностике аневризм, особенно с введением в рутинную практику 3D-ротационной ангиографии, для выявления аневризм менее 3 мм и сосудов малого диаметра (в том числе, перфорирующих артерий) [20, 29, 46, 60, 91, 95, 101, 102, 116]. ДСА не может быть использована как скриннинговое исследование в связи с необходимостью госпитализации пациентов и наличием вероятных осложнений при проведении манипуляции, таких как аллергическая реакция на контраст, ОНМК по ишемическому типу, разрыв аневризмы, повреждение артерии, гематома в области пункции артерии и другие [34, 82]. Количество осложнения при проведении ДСА, включая постоянный неврологический дефицит у пациентов с аневризмами, САК и АВМ, не превышает 0.07% [17].
Проведение ДСА нецелесообразно [рекомендация] у пациентов с аутосомно-доминатным поликистозом почек, почечной недостаточностью, синдромом Элерса-Данло.
Анализ изображений [рекомендации]
При выявлении аневризмы, независимо от того, какой метод использовался, необходимо определить ряд параметров для уточнения тактики лечения и проведения динамического наблюдения. Необходимо оценить размеры шейки аневризмы, соотношение диаметра купола к диаметру шейки, угол расположения аневризмы относительно несущего сосуда (для латеральных аневризм), соотношение максимального размера купола к диаметру несущего сосуда, размеры аневризмы в 3 плоскостях [63].
Скриннинг
Определенные группы в популяции, имеющие повышенный риск обнаружения аневризм головного мозга, подлежат проведению скрининга. Пациент перед проведением обследования должен быть информирован о возможных последствиях как проведения самого исследования, так и различных видов лечения или консервативного лечения, включая такие психологические факторы, как стресс и тревогу, если аневризма будет обнаружена. Учитывая данные эпидемиологических исследований, можно рекомендовать проводить неинвазивные методы скрининга каждому человеку в общей популяции после 30 лет в независимости от наличия или отсутствия факторов риска обнаружения аневризмы. Если при первом обследовании данных за аневризму не обнаружено, повторное обследование можно рекомендовать по достижении 50 лет.
Лечение
Хирургическое лечение пациентов с неразорвавшимися аневризмами
Отбор пациентов с неразорвавшимися аневризмами на операцию [рекомендации]
Проведение операции по поводу НА сосудов головного мозга показано при наличии одного и/или нескольких следующих факторов риска разрыва аневризмы:
• размер аневризмы 7 и более мм
• несферическая форма и наличие дивертикулов
• латеральное расположение аневризмы
• коэффициент соотношения высоты купола аневризмы к диаметру шейки аневризмы более 1,6
• коэффициент соотношения максимального размера аневризмы к диаметру несущего сосуда более 2,05
• угол отклонения латеральной аневризмы от несущей артерии более 1120
• рост размера аневризмы на 0,75 мм и более в течение 6 месяцев
• появление новых клинических проявлений (симптомы поражения черепных нервов, появление и/или изменение характера головных болей, ишемические нарушения в бассейне несущей аневризму артерии)
• незамкнутость артериального круга большого мозга
• «перианевризматическое» окружение – контакт аневризмы с ТМО, костями черепа, черепными нервами, артериями и венами
• множественные аневризмы
• наличие в анамнезе кровоизлияния из другой аневризмы
• курение
• артериальная гипертензия
При выявлении у больного НА размерами 3 мм и менее хирургическое лечение не показано, больному необходимо проведение динамического наблюдения с повторными обследованиями через 6, 12 месяцев и затем каждые 2 года [стандарт]. Подобному же наблюдению подлежат пациенты, отказавшиеся от хирургического лечения [стандарт].
При выявлении аневризм размерами от 3 до 7 мм необходимо измерение морфологических параметров аневризмы, вопрос о проведении хирургического лечения принимается индивидуально с учетом факторов риска (возраст, пол, наличие в анамнезе курения, гипертонической болезни, наличие «семейного» анамнеза, наличие генетических заболеваний) [рекомендации].
Больной с НА должен быть информирован о характере болезни, возможных вариантах течения, возможных осложнениях хирургического вмешательства [стандарт].
Обследование в нейрохирургическом стационаре [рекомендации]
После поступления больного в специализированный нейрохирургический стационар, помимо общих клинических исследований, необходимо провести:
— подробный неврологический осмотр;
— КТ-АГ или МР-АГ головного мозга при поступлении в том случае, если: с момента предыдущего исследования прошло более 6 месяцев; отмечено изменение в неврологическом статусе больного за время с момента выявления аневризмы до госпитализации; качество ранее выполненных КТ и/или МРТ низкое.
— проведение ДСА (в 2D и 3D режимах) показано пациентам со «сложными» аневризмами для оценки их морфологических особенностей и выбором тактики хирургического лечения; также больным с аневризмами размерами менее 7 мм для оценки их морфологических параметров и уточнения рисков разрыва.
Хирургические вмешательства у пациентов с неразорвавшимися церебральными аневризмами [рекомендации]
1) Микрохирургическое лечение:
— пациенты в возрасте до 60 лет
— аневризмы доступной локализации
— аневризмы большого и гигантского размера, оказывающие объемное воздействие на окружающие структуры
— частично тромбированные аневризмы
— при необходимости выполнения комбинированных (микрохирургическое выключение аневризмы из кровотока и реваскуляризирующие вмешательства) операций.
2) Эндоваскулярное лечение:
— пациенты в возрасте старше 60 лет
— локализация аневризм в вертебробазилярном бассейне, в области кавернозного отдела или офтальмического сегмента ВСА
— наличие декомпенсированных соматических заболеваний
Интраоперационный контроль эффективности прямого хирургического вмешательства [рекомендации]
Для подтверждения радикальности клипирования аневризмы и состоятельности кровотока по несущей артерии и функционально значимым ветвям выполняют следующее:
— пункция аневризмы и/или вскрытие просвета аневризмы
— визуальная оценка области клипирования (через микроскоп и/или эндоскоп)
— контактная интраоперационной допплерографии/флуометрия
— интраоперационная ангиография с использованием индоцианина зеленого
Оценка результатов операции и исходов лечения больных, динамическое наблюдение за пациентами после выключения аневризмы из кровотока
Окончательную оценку исходов проводят в сроки не ранее 6 месяцев после операции. Более раннюю оценку (при выписке больного) выполняют как промежуточный этап. Оценку исходов лечения проводят по шкале исходов Глазго.
Пациентам с оперированными церебральными аневризмами, вне зависимости от типа хирургического вмешательства, необходимо проведение контрольных обследований для исключения повторного заполнения аневризмы, оценки остаточной заполняющейся части аневризмы, а также для выявления аневризм de novo [63] [стандарт].
Для проведения динамического наблюдения за пациентами после операции возможно выполнение МР-ангиографии, КТ-ангиографии или ДСА.
Несмотря на то, что применение МР-ангиографии и КТ-ангиографии ограничивается наличием возможных артефактов от металлических имплантов, таких как клипсы, стенты и спирали, эти методы остаются достаточно эффективными для послеоперационного контроля [1, 2, 48, 88, 92]. Напряженность поля при выполнении контрольной МР-ангиографии должна быть 1,5 Тесла [опция].
Применение КТ-ангиографии для динамического наблюдения может быть ограничено в связи с нежелательностью рентгеновского облучения у ряда пациентов [70, 79, 98, 107].
Использование ДСА в качестве контрольного обследования у пациентов с оперированными аневризмами ограничено в связи с инвазивностью обследования и наличием радиационной нагрузки [24, 76].
После проведенного хирургического лечения контрольную ДСА в ранние сроки (до 2 недель после операции) выполняют в том случае, если аневризма не была полностью выключена, при сомнении хирурга в радикальности проведенной операции, или при подозрении на миграцию наложенного клипса. Повторное исследование после микрохирургической операции необходимо провести в течение 6-12 месяцев после вмешательства [рекомендация].
После выполнения эндоваскулярного вмешательства необходимо выполнение контрольного обследования (ДСА) в период от 6 до 12 месяцев после операции [1, 2, 3, 48, 72, 87, 92] [рекомендации]. Время последующих контрольных обследований зависит от характера окклюзии аневризмы при вмешательстве и первом контрольном обследовании, а также от состояния пациента. При наличии резидуальной аневризмы после эмболизации или стентирования обязательно проведение обследований в отдаленном периоде, так как возможны кровоизлияния и рост остаточной части аневризмы. Показано проведение серии контрольных обследований при аневризмах с широкой шейкой, больших и гигантских аневризмах, так как у них имеется высокий риск повторного заполнения [10, 93].
Всем пациентам, входящим в популяционные группы риска по формированию аневризм, независимо от вида оперативного вмешательства, после завершения периода наблюдения можно рекомендовать выполнение неинвазивных методов обследования (МР- или КТ-ангиографии) 1 раз в 5 лет для исключения формирования аневризм de novo [рекомендация].
Динамическое наблюдение за пациентами с неразорвавшимися церебральными аневризмами, не получавшими хирургического лечения [рекомендации]
Пациентам с неразорвавшимися аневризмами сосудов головного мозга, которые не получали хирургического лечения, необходимо проведение нейровизуализационного обследования в динамике для исключения роста аневризмы, изменения ее формы и появление других факторов риска ее разрыва [4, 11, 24, 25, 37, 42, 59, 64].
1) При отсутствии противопоказаний основной методикой для проведения динамического наблюдения является TOF MRA (времяпролётная магнитно-резонансная ангиография), а также у пациентов с почечной недостаточностью и тем, у кого имеет значение доза полученного рентгеновского облучения.
2) КТ-ангиография головного мозга является методом выбора у пациентов с противопоказаниями к проведению МРТ или при наличии аневризм, которые не могут быть правильно оценены с помощью МРТ (милиарные аневризмы менее 3 мм, «сложные» аневризмы).
3) Первое динамическое обследование после выявления неразорвавшейся аневризмы необходимо проводить в период от 6 до 12 месяцев [8, 33, 56, 112, 113]. Затем рекомендуется проводить обследование 1 раз в год или каждые 2 года при отсутствии признаков роста аневризмы и/или изменения ее других морфологических параметров (формы, расположение относительно несущего сосуда и т.д.) [113].
Госпитализация
Больного с неразорвавшейся аневризмой сосудов головного мозга, при наличии показаний к хирургическому лечению, необходимо госпитализировать в плановом порядке в стационары, где имеются:
— нейрохирургическое отделение;
— специалисты, владеющие опытом прямых микрохирургических операций по поводу церебральных аневризм;
— специалисты, владеющие опытом эндоваскулярного выключения аневризм;
— отделение лучевой диагностики, оснащенное аппаратурой для проведения КТ или МРТ, спиральной КТ-ангиографии, МР-ангиографии, ангиографическая операционная для проведения ДСА и выполнения эндовазальных операций;
— операционная, оснащенная оборудованием для микрохирургии церебральных аневризм (операционный микроскоп, микрохирургический инструментарий, съемные и постоянные немагнитные клипсы);
— отделение нейрореанимации.
Информация
Источники и литература
Информация
| Крылов Владимир Викторович | академик РАН, профессор, доктор медицинских наук, заведующий научным отделением неотложной нейрохирургии НИИ скорой помощи им. Н.В. Склифосовского, заведующий кафедрой нейрохирургии и нейрореанимации Московского государственного медико-стоматологического университета им. А.И. Евдокимова, главный внештатный специалист нейрохирург Министерства Здравоохранения Российской Федерации |
| Элиава Шалва Шалвович | Доктор медицинских наук, профессор, заведующий отделением сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Яковлев Сергей Борисович | Доктор медицинских наук, заведующий отделением эндоваскулярной нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Хейреддин Али Садек | Доктор медицинских наук, врач отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Белоусова Ольга Бенуановна | Доктор медицинских наук, ведущий научный сотрудник отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Полунина Наталья Алексеевна | Кандидат медицинских наук, научный сотрудник отделения неотложной нейрохирургии НИИ СП им. Н.В. Склифосовского |
Определение понятий
Стандарт
Общепринятые принципы диагностики и лечения, которые могут рассматриваться в качестве обязательной лечебной тактики (эффективность подтверждена несколькими рандомизированными исследованиями, мета-анализами или когортными клиническими исследованиями).
Рекомендация
Лечебные и диагностические мероприятия, рекомендованные к использованию большинством экспертов по данным вопросам. Могут рассматриваться как варианты выбора лечения в конкретных клинических ситуациях (эффективность подтверждена отдельными рандомизированными исследованиями или когортными клиническими исследованиями).
Опция
Лечебные и диагностические мероприятия, которые могут быть полезны (эффективность подтверждена мнением отдельных экспертов, в отдельных клинических случаях).
Не рекомендуется
Лечебные и диагностические мероприятия, не имеющие положительного эффекта или могущие принести вред (любой уровень подтверждения).



 Как проходит лечение
Как проходит лечение