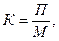Факторы влияющие на процесс авто окисления
Как происходит процесс окисления жиров в косметических продуктах
Окисление жиров является одной из основных причин ухудшения качества косметических продуктов наряду с действием микроорганизмов. Это приводит к изменениям аромата, цвета, потери определенных питательных веществ и образованию потенциально вредных веществ, что приводит к сокращению срока хранения косметики. Этот процесс имеет важные экономические последствия, потому что косметика становится непригодной для потребления.
Окислительный процесс жиров в составе косметического продукта вызывает разрушение жирорастворимых витаминов и деградации полиненасыщенных кислот, также безопасность продукта для человека может быть затронута из-за некоторых летучих веществ: пероксидов и оксикислот, появляющихся в результате этого процесса.
Эта статья посвящена описанию окислительного процесса жиров и, следовательно, важности использования антиоксидантных веществ. Для этого мы сосредоточимся на процессе окисления жиров и основных факторах, которые влияют на их окисление.
Окисление жиров
Исторически считалось, что добавление кислорода к молекуле жирной кислоты образует четырехатомное кольцо в качестве основного продукта реакции. Эта молекула называется «перекисью». Однако фактически образуется гидропероксид из-за добавления кислорода к альфа-углероду двойной связи. Несмотря на это, неточное мнение все еще сохраняется, и пероксиды все еще относятся к продуктам деградации жира.
Автоокисление является необратимым процессом окисления жиров, его невозможно избежать во всей полноте, но его можно отсрочить из-за добавления антиоксидантов.
Механизм окисления состоит из трех фаз:
После полного разрушения жирных кислот образуются вторичные продукты окисления, которые ответственны за возникновение прогорклости.
Чтобы задержать или предотвратить окисление жиров и прогорклость косметических продуктов, необходимо знать, как предотвратить образование первых свободных радикалов или первых гидропероксидов, поскольку это может быть достигнуто только на первой стадии окислительного процесса во время инициирования. Напротив, как только окислительный процесс достигнет фазы распространения, указанный процесс больше не может быть задержан или остановлен.
Факторы, влияющие на окисление
Факторы, которые влияют на окисление, могут быть неотъемлемыми и / или внешними по отношению к косметическому продукту, то есть они могут относиться к продукту и к применяемой технологии. Ниже приводятся некоторые из наиболее актуальных:
Температура. Скорость автоокисления возрастает с температурой. Это может повлиять не только на скорость автоокисления, но и на механизмы реакции.
Кислород. Скорость автоокисления возрастает с увеличением давления кислорода, пока он не достигнет постоянной скорости реакции.
Влажность. Влияние активности воды на скорость окисления липидов очень сложное. Прогорклость развивается быстро при очень высоком и очень низком уровне влажности. Максимальная стабильность наблюдается при промежуточных уровнях влажности, соответствующих значениям монослоя (защитный эффект воды в виде монослоя).
Ионизирующее излучение. Одним из наиболее заметных эффектов облучения высокой энергией на пищу является заметное увеличение восприимчивости окислительной прогорклости.
Катализаторы: Ионы тяжелых металлов являются мощными катализаторами окисления липидов, уменьшают период индукции и увеличивают скорость реакции.
В качестве вывода можно отметить, что для уменьшения или замедления окисления жиров в косметических продукитах необходимо действовать против одного или нескольких факторов, которые способствуют его развитию.
В широком смысле антиоксидантом считается любое вещество или процесс действия, который помогает ограничить скорость и / или расширение окислительных процессов. Согласно этой концепции, три вида антиоксидантов могут быть рассмотрены в зависимости от их механизма действия. Первые два типа связаны с добавлением химических соединений, в то время как третий обязан своим действием модификациям определенных факторов в конечном косметическом продукте и / или на стадия его производства.
Окислительные изменения и гидролиз жиров
В жировой ткани сразу после убоя не обнаруживаются перекиси, так как они не являются нормальным продуктом обмена в организме животного. При производстве и хранении жиров возможны окислительные процессы в жире, скорость и направленность которых зависит от природных свойств жира и условий окисления. Большое влияние на стойкость жиров к окислению оказывает способ их производства. Наличие перекисей обнаружено в свежеизготовленных жирах, так как окисление происходит при подготовке сырья и вытопке жира. Накопление перекисей зависит от способа производства жиров. Глубина изменений, происходящих при производстве жира, определяет в дальнейшем скорость порчи жиров при хранении. Чем выше исходное качество жира, тем больше его стойкость при хранении. Небольшие количества прогоркшего жира, попавшие в свежий, могут привести к быстрой его порче. Высокой стойкостью к окислению обладают жиры, изготовленные с применением вакуума или инертного газа.
Перекисное число жира, вытопленного в открытом котле, 0,013—0,035, а в центробежной машине — 0—0,025% йода. Скорость порчи жира при хранении зависит от химического состава сырья. Многочисленными исследованиями установлены основные факторы, влияющие на подверженность жира окислению: состав жира, в частности содержание ненасыщенных жирных кислот, содержание катализаторов, легко окисляющихся металлов (солей железа, меди, свинца, олова), а также органических веществ, содержащих железо (белков, гемоглобина и др.); парциальное давление кислорода, поверхность, находящаяся в соприкосновении с кислородом; условия хранения жиросодержащих продуктов (температура, освещенность, содержание влаги); равновесие окислительных и аитиокислительных веществ в жире.
Образование в жире перекисей ускоряется при передержке жиросырья перед вытопкой, повышенной температуре, присутствии кислорода, контакте с металлическим оборудованием. Загрязнение медью и железом, происходящее при коррозии оборудования, резко ускоряет окисление. Предполагается, что металлы, особенно медь и двухвалентное железо, катализируют окисление природных антиокислителей и этим сокращают индукционный период. Медь ускоряет окисление жира при концентрации от 0,002 до 0,005 мг% от массы жира. Если расплавленный говяжий жир пропускают через краны, изготовленные из бронзы, скорость окисления жира возрастает в 6 раз.
Свет не только ускоряет окисление при непосредственном воздействии, но и способствует увеличению образования перекисей после прекращения его воздействия. Самоокисление жира ускоряется благодаря ультрафиолетовому свету. Даже сравнительно желтый свет лампы с вольфрамовой нитью накала воздействует на жир; значительно активнее флюоресцентное освещение. Колебания интенсивности света при обработке, хранении и реализации жира могут быть значительны, начиная с солнечного света до искусственного освещения, которое в 1000 раз слабее. Особо следует избегать воздействия на жир дневного света из-за высокой интенсивности и воздействия ультрафиолетового облучения.
Окислительная порча начинается с присоединения активированных молекул кислорода и образования перекисей и развивается по принципу цепных реакций. Окисление жира может происходить в результате его контакта с кислородом воздуха и при воздействии с ранее адсорбированным кислородом.
Современные представления о механизме реакции окисления основаны на перекисной теории Баха—Зиглера и теории вырожденно-разветвленных цепных реакций Н. Н. Семенова. Торможение процессов окисления антиокислителями подтверждает цепной характер реакции окисления. Согласно теории окисления первым продуктом окисления являются перекиси; аналитически обнаруживаются гидроперекиси.
Перекиси стимулируют окисление других молекул, что обусловливает цепной характер окисления:
Окисление жиров происходит через образование свободных радикалов и относится к классу медленно развивающихся цепных разветвленных реакций. В цепной реакции могут быть выделены следующие стадии: зарождение цепи (образование свободного радикала), развитие цепи и обрыв ее, а в разветвленных цепных реакциях — еще и разветвление цепи.
В результате поглощения света молекула жирной кислоты получает энергию hv и переходит в возбужденное состояние:
Возбужденное состояние обусловливает нестабильность молекулы (R*Н) и распад на радикалы:
Получаемые свободные радикалы обладают высокой активностью, и если в системе имеется кислород, то его молекулы вступают в реакцию и образуются реактивные перекисные радикалы:
Образовавшиеся радикалы реагируют с новыми молекулами окисляемого вещества и образуются гидроокиси и новый свободный радикал R:
который вновь вступает в реакцию с кислородом, и, таким образом, возникает цепная реакция.
С молекулой кислорода может также взаимодействовать свободный атом водорода, в результате чего образуется свободный радикал:
Обрыв цепи может произойти в результате рекомбинации свободных радикалов, при развитии которой два свободных радикала образуют одну неактивную молекулу:
Ȯ—OH + Ȯ—OH → H—O—O—O—Ȯ—H → HOOH + O2
В процессы автоокисления жиров легче всего вовлекаются ненасыщенные жирные кислоты, содержащие двойные связи и активно поглощающие кванты света:
При взаимодействии свободного радикала с кислородом образуется перекисный радикал, который реагирует с новой молекулой ненасыщенной жирной кислоты, отрывая от нее атом водорода, превращается в гидроперекись.
При образовании гидроперекиси появляется новый свободный радикал, вступающий в реакцию и продолжающий цепь окислительных изменений. При этом в реакции включаются все новые молекулы жирной кислоты. Гидроперекиси отличаются низкой стойкостью, и в результате разнообразных реакций из них образуются вторичные продукты распада — альдегиды, кетоны, низкомолекулярные кислоты, сообщающие жиру прогорклый вкус и резкий, неприятный запах. В химии жиров карбонильным соединениям уделяется большое внимание и «карбонильный индекс» предлагается как показатель прогорклости пищевого жира взамен перекисного числа.
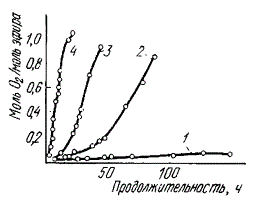
Высокой подверженностью к окислению отличаются ненасыщенные жирные кислоты (особенно арахидоновая) и насыщенные жирные кислоты с короткой цепью (C6—C10). Подверженность окислению различных видов жира обусловлена различным содержанием ненасыщенных жирных кислот. Жир свиней и птицы окисляется быстрее, чем говяжий и бараний. Высокомолекулярные жирные кислоты более устойчивы к таким изменениям. Модельные эксперименты, проведенные с отдельными жирными кислотами, показали, что чем больше в составе молекулы двойных связей, тем более коротким является индукционный период и тем быстрее протекает окисление.
| Жирные кислоты | Число двойных связей | Индукционный период, ч | Относительная скорость окисления |
| Стеариновая | 0 | — | 1 |
| Масляная | 1 | 82 | 100 |
| Линолевая | 2 | 19 | 1200 |
| Линоленовая | 3 | 1,34 | 2500 |
Зависимость скорости окисления эфиров жирных кислот на воздухе при температуре 37° С от количества двойных связей в них: 1 — этилолеат; 2 — этиллинолеат; 3 — этиллиноленат; 4 — метиларахидонат
На рисунке показана зависимость скорости окисления эфиров ненасыщенных жирных кислот от количества двойных связей. В жировой ткани убойных животных важное значение имеет окисление, катализируемое гематином. Некоторые авторы считают, что окислительные процессы в липидах мышечной ткани почти всецело зависят от Mb и Hb и их производных. Гемовые соединения Mb и Hb и цитохромы являются главными катализаторами окисления жиров, особенно в гетерогенных системах, содержащих водную и липидную фазы. При содержании в жире-сырце остатков крови при вытопке Mb и Hb разрушаются с образованием парагематинов, что вызывает потемнение жира.
Катализируемое гематином окисление не имеет столь большого значения для топленых жиров длительного хранения, так как в них не содержится гемовых соединений в количествах, необходимых для развития процессов окисления. Такое окисление может играть определенную роль в шпике, особенно если в результате шпарки при чрезмерно высоких температурах в кожных и подкожных кровеносных сосудах остается значительное количество крови, которая при хранении медленно проникает в жировую ткань, вызывая каталитическое действие гемоглобина.
Особенно подвержены окислению липиды мышечной ткани, которые представляют собой составные части различных клеточных структур: мышечных волокон, митохондрий и микросом. Катализированное гематином окисление обладает более коротким индукционным периодом, чем самоокисление, что объясняется относительно низкой энергией активации катализированного гематином окисления. Коагуляция белков уменьшает каталитическую активность пигментов мяса. После замораживания окисление жира, катализируемое гематином, практически прекращается, но оно ускоряется после размораживания мяса.
Установлено, что фосфаты тормозят катализируемое Mb и Hb окисление жиров в мясе, причем даже 0,01%-ный раствор трифосфата тормозит окисление жиров в вареном мясе. Нитрозомиоглобин также является катализатором окисления. Однако его окислительная активность снижается при нагреве в результате денатурации. Попытки создать ингибиторы гемовых окислителей пока не имели успеха. Наряду с этим аскорбиновая кислота является хорошей защитой от способности НЬ катализировать окисление жира. Посол мяса, увеличивая сопротивляемость к гнилостной порче, одновременно часто увеличивает чувствительность жира к окислению. Это обусловлено окислительным действием соли.
Окислительные изменения жиров ускоряются ферментами микроорганизмов. Развитие микрофлоры на жиросырье значительно снижает стабильность топленого жира к атмосферному окислению. Говяжье жиросырье после трехдневного хранения при повышенной влажности приобретает запах порчи и при вытопке дает жир с индукционным периодом от 3 до 15 ч при 70° С. В то же время при вытопке в парном состоянии индукционный период составил 150 ч при 70° С.
В начальной стадии окисления отсутствуют изменения органолептических и химических показателей жира. Этот период, различный по продолжительности, обусловлен тем, что в начальной стадии в жире содержится значительное количество возбужденных молекул или свободных радикалов. Кроме этого, в нем содержатся естественные антиокислители, препятствующие окислению.
При окислении жиров образуются вещества, обусловливающие прогорклый, металлический или другой посторонний оттенок аромата и вкуса продуктов. Продукты окисления — перекиси, альдегиды, кетоны, оксикислоты и свободные низшие жирные кислоты ухудшают вкус и запах жира. Гептиловый альдегид обнаруживается органолептически при концентрации 1 мг%. В формировании вкуса и запаха жира, подвергнутого окислительной порче, участвуют также жирные кислоты: капроновая, каприловая, масляная, акриловая, уксусная, муравьиная и др.
Снижение пищевой ценности жиров при окислении обусловлено тем, что сопровождается снижением содержания в жире ненасыщенных жирных кислот, распадом витаминов, все это происходит до появления обнаруживаемых органолептически признаков порчи. В окисляющихся жирах снижается содержание витаминов А и Е; разрушается каротин. Окисление каротина и других липохромов проходит быстрее при температуре вытопки выше 60° С. При окислении в результате контакта с пигментами мяса и крови разрушаются витамины комплекса В. Предполагается, что отрицательное влияние на организм окисленных жиров обусловлено их прямым токсическим действием или разрушением ими жизненно важных компонентов продукта. В прогорклых жирах содержатся токсические вещества, вызывающие нарушение обмена, расстройство нормальной жизнедеятельности организма. Установлена токсичность гидроперекисей, выделенных в чистом виде. Имеются данные, что образование глубоких продуктов распада жиров сопровождается накоплением канцерогенных веществ.
Употребление в пищу окисленных жиров может явиться причиной атеросклероза, так как окисленные липиды образуют комплексы с белками, которые откладываются в аорте, а холестерин и его эфиры осаждаются на этих комплексах.
Важным показателем, характеризующим качество жира, показывающим степень его окисленности во всех случаях, когда нет условий для разложения перекисей, является перекисное число. Наиболее широко в промышленности применялась шкала зависимости между перекисным числом и качеством жира, разработанная А. А. Зиновьевым. По этой шкале качество топленых животных жиров определяют по перекисному числу. При перекисном числе выше 0,1 животные жиры по органолептическим показателям непригодны для хранения.
| Качество жиров | Переписное число, % йода |
| Свежий | не >0,03 |
| Свежий, непригодный к длительному хранению | от 0,03 до 0,05 |
| Сомнительной свежести (порча, обнаруживаемая органолептически) | от 0,06 до 0,1 |
| Испорченный | выше 0,1 |
Величина предельного перекисного числа в ГОСТе для топленого жира может быть уменьшена при создании более совершенного оборудования. Снижение интенсивности окислительных процессов достигается охлаждением, ограничением доступа воздуха, хранением в темноте, дезактивацией металлических примесей, способствующих окислению, инактивацией ферментов нагреванием и регулированием содержания влаги. Развитие окисления затормаживается при применении любого вида упаковки, снижающей контакт жира с кислородом воздуха. Наиболее совершенной является вакуумная упаковка с введением в пакет инертного газа. Хранение бекона при —10° С в атмосфере CO2 позволяет удлинить срок хранения на 12 мес.
При хранении жиросырья окисление развивается вначале в поверхностных слоях и медленно проникает внутрь. Установлено, что в поверхностных слоях бекона, сохраняемого в течение 3 мес, количество перекисей в 25 раз больше, чем на глубине 1 см.
Скорость окисления жира возрастает примерно в 2 раза при повышении температуры на 10° С. При варке окисление резко возрастает, хотя оно не всегда сопровождается увеличением перекисного числа из-за чувствительности перекисей к нагреву. Более интенсивное прогоркание жира вареного мяса обусловлено инактивацией при тепловой обработке веществ, обладающих антиокислительным действием.
Наиболее эффективное удлинение сроков хранения жиров и сохранение их качества достигаются применением антиокислителей. Механизм действия антиокислителей основан на взаимодействии со свободными радикалами, которые передают энергию антиокислителю и выводятся из цепи окисления, в результате чего цепь обрывается.
где R — жирная кислота; А — антиокислитель; hv — энергия.
В результате взаимодействия с кислородом активная молекула антиокислителя теряет энергию и переходит в неактивный окисленный продукт:
Некоторые антиокислители разрушают возникшие перекиси. В состав жиров входят природные антиокислители (каротин, токоферол, лецитин), однако в процессе производства и очистки происходят потери природных антиокислителей, что снижает устойчивость жиров к окислению. При изучении антиокислительных свойств некоторых каротиноидов и витамина А установлено, что β-каротин и витамин А являются ингибиторами спонтанного окисления жиров. Токоферолы представляют собой естественные антиокислители жиров; жиры тем устойчивее к прогорканию, чем больше в них содержится токоферолов. Животные жиры очень бедны токоферолом; в растительных жирах их содержание значительно выше. Значительный распад токоферолов происходит при вытопке; недостаток токоферолов в организме животного является эндогенным фактором порчи жира.
Пищевой антиокислитель должен иметь такую величину молекул, чтобы они легко могли проникать через клетки животной ткани, а также обладать растворимостью в жирах, обеспечивающей проникновение в водную и жировую фазы. К антиокислителям предъявляют следующие требования: наличие эффективного антиокислительного действия, они не должны сообщать жиру постороннего привкуса, запаха и цвета при длительном хранении, отсутствие вредного физиологического действия, устойчивость к воздействию высоких температур. Этим требованиям в наибольшей степени отвечают бутилоксианизол и бутилокситолуол. В практике применяют смеси антиокислителей, а также композиции антиокислителей с синергистами, например при совместном применении бутилоксианизола и бутилокситолуола наблюдается заметный синергетический эффект.
Лецитин обладает способностью легко окисляться и является синергистом антиокислителей. Исследовано влияние добавок, усиливающих действие антиокислителей. При наличии водной фазы лучшие результаты дали полифосфаты. Эффективность действия антиокислителей возрастает с увеличением концентрации. Установлено следующее соотношение эффективности: α-токферол
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Большая Энциклопедия Нефти и Газа
Процесс автоокисления углеводородов является самоускоряющимся. В первый период окисления, называемый периодом индукции, происходит накопление пероксидов. При обычных температурах скорость этого процесса невелика. При развитии и разветвлении окислительных цепей скорость окисления возрастает. В продуктах окисления со временем появляются стабильные конечные соединения, и некоторые из них способны обрывать окислительные цепи, и скорость окисления снижается. [1]
Процесс автоокисления углеводородов является самоуско-ряющимс я. В первый период окисления, называемый периодом индукции, происходит накопление пероксидов. При обычных температурах скорость этого процесса невелика. В продуктах окисления со временем появляются стабильные конечные соединения, и некоторые из них способны обрывать окислительные цепи, и скорость окисления снижается. [2]
Согласно современным представлениям, процесс автоокисления углеводородов протекает по цепному механизму. Окислительная цепь развивается благодаря накоплению в объеме окисляемых углеводородов свободных радикалов. Первичная активация углеводородов, приводящая к их диссоциации с образованием свободных радикалов, происходит под действием света, температуры, катализатора и других факторов. Образование радикалов дает начало основной цепи окисления. [3]
Большое значение в развитии процесса автоокисления углеводородов несомненно принадлежит образованию свободных радикалов при распаде перекисей. [4]
После отделения адсорбционных смол, включавших и ингибирующие соединения, процесс автоокисления углеводородов прямогонного топлива и крекинг-керосина начал развиваться значительно интенсивнее, чем в не-обессмоленном топливе. [6]
Приведенные данные о превращениях перекисных соединений, первоначально образующихся в процессе автоокисления углеводородов и их кислородных производных, и вытекающие из них соображения дают возможность сформулировать некоторые общие выводы и построить схему вероятных направлений этих превращений, имеющих место в ходе развития окислительного процесса. [8]
Камневой и сотрудниками [20] выполнена большая работа по изучению химизма образования смол в процессе автоокисления углеводородов в жидкой фазе. Обследованы продукты окисления цикло-гексена, тетралина и декалина, полученные при низких температурах под ультрафиолетовым облучением. Автор пришел к интересным выводам о том, что в процессе окисления гидроперекись претерпевает превращение в двух направлениях-происходит распад с образованием мономолекулярных кислородных соединений и полимеризация с образованием димеров и тримеров гидроперекисей. [11]
Стимулирование процесса автоокисления углеводородов может быть достигнуто не только при помощи катализирующих добавок, но, как установлено в последнее время, и действием проникающих у-излучений. В этой же работе дается и теоретическое обоснование эффективности подобного воздействия на процесс автоокисления. [13]
В прямогонных топливах после длительного хранения содержание адсорбционных смол, их йодные числа и средний молекулярный вес изменялись незначительно. Это значит, что процесс автоокисления углеводородов практически приостановился за гчет накопившихся ингибирующих соединений. [14]
Физические и химические свойства жиров
Жиры нерастворимы в воде (гидрофобны), хорошо растворимы в органических растворителях.
Важным физическим показателем жира является его температура плавления и застывания. Чем больше в жире низкомолекулярных непредельных кислот, тем ниже температура его плавления. Наличие ОН-групп в молекуле жира повышает температуру его плавления. Температура застывания жира на несколько градусов ниже, чем плавления, что имеет очень важное физиологическое значение. Например, температура плавления говяжьего жира 51ºС, бараньего – 55ºС, свиного – 48ºС и попадая в организм с пищей, они остаются там в расплавленном состоянии, так как температура их застывания ниже 36ºС,что способствует лучшему их перевариванию. Важнейшим физическим показателем жира является его вязкость, которая увеличивается в жирах по мере развития процессов окисления и полимеризации.
Химические свойства жиров:
1. Гидролиз жиров протекает с выделением глицерина и жирных кислот.
Реакция гидролиза называется реакцией омыления, используется в промышленности для производства мыла. Гидролитический распад жиров, зерна муки, крупы и др. является одной из причин ухудшения их качества и, в конечном счете, – порчи. Скорость и глубину гидролиза жира характеризует кислотное число – количество миллиграммов едкого калия, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г масла или жира. Кислотное число для ряда жиросодержащих пищевых продуктов нормируется стандартами, характеризует их качество.
2. Гидрогенизация жиров – присоединение водорода. Задача гидрогенизации – целенаправленное изменение жирно-кислотного состава исходного жира в результате частичного или полного присоединения кислорода к ненасыщенным остаткам жирных кислот. Реакция проводится при температуре 180-240ºC в присутствии никелевых или медно-никелевых катализаторов при давлении, близком к атмосферному.
3. Окисление жиров – реакция взаимодействия с кислородом воздуха. Жиры, особенно содержащие радикалы ненасыщенных кислот, окисляются кислородом воздуха. В основе механизма окисления лежит теория Баха-Энглера и Н.Н.Семенова. Согласно которой существенную роль на начальных стадиях цепных реакций играют свободные радикалы, образующиеся в жирах под влиянием света. При этом молекула жира поглощает квант света (hν), и переходит в возбужденное состояние. Образующиеся радикалы очень активны, опять образуют перекисные радикалы, которые, вступая в реакцию, образуют цепные гидроперекиси (первичные продукты окисления) и новые радикалы.
Образовавшиеся гидроперикиси неустойчивы и в результате сложных превращений образуются вторичные продукты окисления – окси-эпоксисоединения, спирты, альдегиды, кетоны, кислоты.
Направление и глубина окисления масел и жиров зависит от их жирнокислотного состава: с увеличением степени непредельности жирных кислот, скорость их окисления возрастает. Триглицериды, в состав которых входят насыщенные жирные кислоты кислородом воздуха при обычных условиях практически не окисляются. На скорость окисления, кроме того, влияет присутствие влаги, металлов переменной валентности. Большое влияние на скорость окисления оказывают антиокислители (ингибиторы) – вещества, добавление которых приводит к обрыву цепей окисления. Среди антиоксидантов большое значение имеют вещества фенольной природы, из природных антиокислителей большое значение принадлежит токоферолам.
К основным физико-химическим показателям жиров относятся:
– йодное число, характеризующее степень ненасыщенности жиров, выражается в гр J2, присоединяющегося к 100 г жира;
– кислотное число – характеризует количество свободных жирных кислот в жире;
– число омыления – характеризует общее содержание жирных кислот в жире, выражается в г КОН, необходимого для нейтрализации всех жирных кислот, выделившихся при гидролизе 1 г жира;
– ацетильное число – характеризует количество свободных гидроксильных групп в жире, выражается в мг КОН, необходимых для нейтрализации уксусной кислоты, выделившейся при омылении 1г предварительного ацетилированного жира;
– перикисное число – характеризует содержание в жире перекисей, выражается в г йода, присоединяющегося к 100 г продукта;
– коэффициент преломлении и вязкость могут также характеризовать степень окисления жира, так как между этими показателями установлена математическая зависимость.
3. Физико-химические изменения жиров при варке продуктов: плавление, эмульгирование, гидролиз
При хранении жиры изменяют свои свойства, особенно при неправильном хранении. Основная роль при этом принадлежит окислению. Особенно легко прогоркают жиры, содержащие ненасыщенные жирные кислоты, при совместном действии света и воздуха. Чтобы увеличить срок хранения жира необходимо соблюдать следующие условия:
– жиры хранят в охлаждаемых помещениях не дольше установленного срока;
– тара должна надежно защищать их доступа света и воздуха;
– нежелательно хранение жиров в жестяной таре, так как из нее переходит в жир железо, ускоряющее окисление;
– нельзя смешивать масла различных партий и наливать масло в немытую тару, где уже хранилось масло.
При свободном доступе воздуха происходит окисление жиров, которое ускоряется с повышением их температуры. При температурах 2-25ºС происходит автоокисление, при температурах жарки (140-200ºС) – термическое окисление. Автоокисление обычно сопровождает, а нередко опережает термическое окисление, поэтому эти два процесса взаимосвязаны. Продукты, полученные при авто- и термическом окислении делятся на три группы:
– продукты окислительной деструкции жирных кислот, в результате которой образуются вещества с укороченной цепью;
– продукты изомеризации, а также окислительные триглицериды, которые содержат в углеводородных частях молекулы новые функциональные группы, содержащие кислород;
– продукты окисления, содержащие полимеризованные или конденсированные жирные кислоты.
Помимо окислительных превращений при любом способе тепловой обработки протекают гидролитические процессы при воздействии на жир воды и высокой температуры. Преобладание того или иного процесса зависит от интенсивности воздействия на него кислорода воздуха и воды, а также продолжительности нагревания и присутствия веществ, ускоряющих или замедляющих эти процессы.
Изменения жиров при варке и припускании
Жир плавится, переходит в бульон. Количество жира, перешедшего в бульон, зависит от его содержания и характера отложения в продукте. Рыба тощая теряет при варке до50% жира, среднежирная – до 14%; из мяса извлекается до 40%, а из костей 25-40%, содержащегося в них жира.
Основная масса извлеченного жира распределяется по поверхности бульона (90-95), а небольшая часть (3,5-10%) эмульгирует, то есть распределяется по всему объему бульона в виде мельчайших шариков, придавая бульону мутность. Интенсивность кипения при варке увеличивает количество эмульгировавшего жира.
В результате эмульгирования поверхность соприкосновения жира с водой увеличивается, что способствует дальнейшему гидролизу жира, о чем свидетельствует возрастание кислотного числа. Гидролиз жира протекает под воздействием высокой температуры и воды в три стадии: 1) от молекулы триглицерида отщепляется одна молекула жирной кислоты с образованием диглицерида; 2) затем от диглецирида отщепляется вторая молекула жирной кислоты с образованием моноглицерида; 3)в результате отделения от моноглицерида последней молекулы жирной кислоты образуется свободный глицерин. Таким образом, при полном расщеплении молекулы триглицерида образуется молекула глицерина и три молекулы свободных жирных кислот.
Поваренная соль и органические кислоты ускоряют гидролиз жира. Однако полного расщепления жиров при варке не происходит. Накапливающиеся жирные кислоты придают бульону салистый привкус. Поскольку эмульгированный жир находится в водной среде и его контакт с воздухом затруднен, то можно заключить, что при варке преимущественно протекают гидролитические процессы, нежели окислительные.
На основании вышеизложенного можно заключить, что в процессе варки бульонов для снижения гидролитических процессов необходимо не допускать бурного кипения, снимать излишки жира с поверхности, солить бульон в конце варки.
Лекция № 6,7
Тема «Физико-химические изменения липидов при жарке:
пиролиз, дымообразование. Физико-химические изменения липидов при фритюрной жарке»
План
1.Физико-химические изменения липидов при жарке: пиролиз, дымообразование.
2. Фритюрная жарка: химические изменения жира, типы реакций.
3. Факторы, влияющие на скорость химических изменений фритюрного жира.
4. Изменения органолептических показателей жира в процессе его фритюрной жарки.
5. Методы увеличения срока службы фритюрного жира.
6. Адсорбция и впитывание жира при жарке. Влияние жарки на пищевую ценность жира.
1. Физико-химические изменения липидов при жарке: пиролиз,
Дымообразование
Наиболее распространенными являются фритюрная жарка (периодическая или непрерывная) и жарка продуктов основным способом.
При основном способе жарки продолжительность нагрева составляет 3-10 мин, что зависит от вида и размеров продукта. При этом глубоких окислительных изменений не происходит, ввиду небольшой продолжительности нагрева и отсутствия повторного использования жира. Однако в случае перегрева жира при жарке может произойти его пиролиз – термическое разложение дыма с выделением дыма. Температура, при которой начинается выделение дыма, называется температурой дымообразования и является показателем термостойкости жира. Температура (или точка) дымообразования различная для разных видов жиров (ºС): у свиного жира – 221, хлопкового масла – 223, пищевого саломаса – 230. На температуру дымообразования жира влияют следующие факторы: содержание свободных жирных кислот (снижает температуру дымообразования), отношение нагреваемой поверхности жира к его объему (так, при нагревании одного и того же количества жира на сковородах диаметром 18 и 20 см температура дымообразования оказалась 185 и 169ºС соответственно), материал посуды.
На крупных пищевых предприятиях, осуществляющих фритюрную жарку чипсов, крекеров, рыбных полуфабрикатов и др., применяют аппараты непрерывной фритюрной жарки (соотношение жира и продукта 20:1), что позволяет ускорить процесс жарки, поддерживать более низкие температуры фритюра, следовательно, снижать скорость его термического окисления. При непрерывной жарки жир постоянной удаляется из жарочной ванны с готовым продуктом, а его количество автоматически пополняется путем долива свежего жира. Поэтому при непрерывной фритюрной жарке жир подвергается незначительным окислительным изменениям.
При периодической фритюрной жарке протекают более глубокие изменения, поскольку жир может длительно нагреваться без продукта и периодически использоваться для жарки различных продуктов при низком коэффициенте его сменяемости.
Коэффициент сменяемости жира определяется по формуле
где П – количество жира, поглощаемого и адсорбируемого обжариваемым продуктом за 24 часа, кг;
М – средняя масса жира в жарочном аппарате, кг.
Кроме того, при периодической фритюрной жарке жир могут охлаждать, затем вновь нагревать и при таком циклическом нагреве вероятность окисления жиров максимальна.
– котлеты по-киевски – 160-170ºС, 3-4 мин;
– рыба в тесте – 60-170ºС, 2-3 мин;
– картофель брусочками – 175-180ºС, 5-6 мин;
– картофель соломкой – 175-180ºС, 3-4 мин;
– пирожки, пончики, чебуреки – 180-190ºС, 4-6 мин;
При этом начальная температура фритюра может составлять 160-190ºС. Фритюр с меньшей температурой используют для жарки продуктов с большим содержанием влаги (тельное, котлеты фаршированные из кур и др.).
2. Фритюрная жарка: химические изменения жира, типы реакций
Химические изменения жира при фритюрной жарке
1. Термическое окисление. В процессе фритюрной жарки происходит термическое окисление жира: быстрое образование и распад перекисей, о чем свидетельствует скачкообразное изменение перикисного числа жира. Циклические перикиси распадаются с образованием двух соединений с укороченной цепью (альдегид и альдогидрокислота), которые при дальнейшем окислении образуют одноосновную и двухосновную кислоты:
Циклические перикиси могут превращаться и в другие долее стабильные продукты вторичного окисления с образованием диоксикислот, дикарбонильных соединений.
2. Гидролиз жира. Вода, попадающая в жир из обжариваемого продукта, способствует его гидролизу, происходит накопление свободных жирных кислот и увеличивается кислотное число жира как за счет гидролиза, так и за счет образования низкомолекулярных кислот при расщеплении перикисей.
3. Снижение температуры дымообразования, усиление выделения дыма по мере увеличения продолжительности нагревания. Кроме того, в результате появления оксикислот, моно- и диглицеридов происходит увеличение ацетильного числа.
4. Реакция полимеризации и поликонденсации. Образующиеся дикарбонильные вещества и соединения с сопряженными двойными связями способны к реакциям полимеризации и поликонденсации, о чем свидетельствует увеличение вязкости фритюрного жира. При этом соединение между мономерами может осуществляться как посредством прямой связи меду атомами углерода, или через кислородный мостик, причем в одной молекуле могут присутствовать оба типа связей.
Типы реакций, протекающих при фритюрной жарке
Реакция автоокисления протекает при хранении жира между циклами, скорость реакции медленная, образуются СО2, СО, Н2О, альдегидокислоты, спирты и альдегиды, кетоны, прочие компоненты. Автоокисление протекает при холостом нагреве жира между циклами жарки и в процессе самой жарки, в этом случае скорость реакции достаточно быстрая.
Реакция пиролиза, изомеризации, полимеризации протекает как при холостом нагреве, так и при непосредственной жарке.
Реакция гидролиза, причем с достаточно большой скоростью протекает при непосредственной жарке продуктов.