гематома в головном мозге у новорожденного
Что такое кефалогематома? Причины возникновения, диагностику и методы лечения разберем в статье доктора Месяцев С. О., остеопата со стажем в 16 лет.
Определение болезни. Причины заболевания
Актуальной темой на сегодняшний день остаются осложнения перинатального (околородового) поражения плода. Одним из осложнений родовой деятельности является родовой травматизм, в частности — кефалогематома.
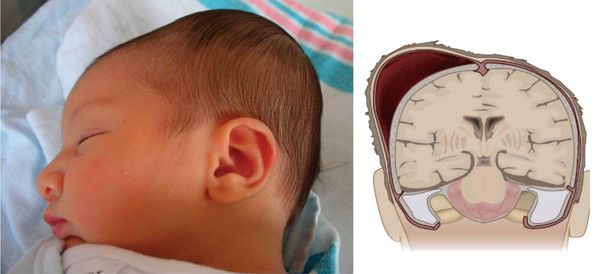
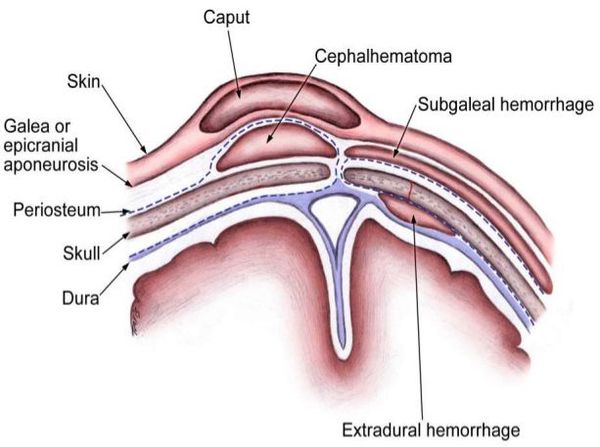
Кефалогематома — это кровоизлияние, локализованное в своде черепа, возникающее под надкостницей в результате сдавления и смещения тканей и костей черепа во время родов. Данное осложнение при родах возникает в 1-3,2% случаях, в зарубежной литературе такой показатель достигает 4%. [1] Вопрос об истинной причине возникновения кефалогематомы остаётся открытым и носит мультифакторный характер.
Немаловажные причины образования кефалогематом (согласно результатам отечественных исследований) — совокупность следующих внутриутробных (пренатальных) факторов:
Существует предположение о влиянии на образование кефалогематом определённых препаратов, которые беременные принимают по профилактическому назначению в женской консультации или по собственному усмотрению. [2]
К другим причинам возникновения данного заболевания относятся сочетания болезней и синдромов, которые возникают при беременности, но не относятся к гинекологическим патологиям:
Также причинами образования кефалогематомы являются совокупности факторов осложнения беременности:
Помимо дородовых причин существуют факторы, увеличивающие риск появления кефалогематомы во время родовой деятельности:
Симптомы кефалогематомы
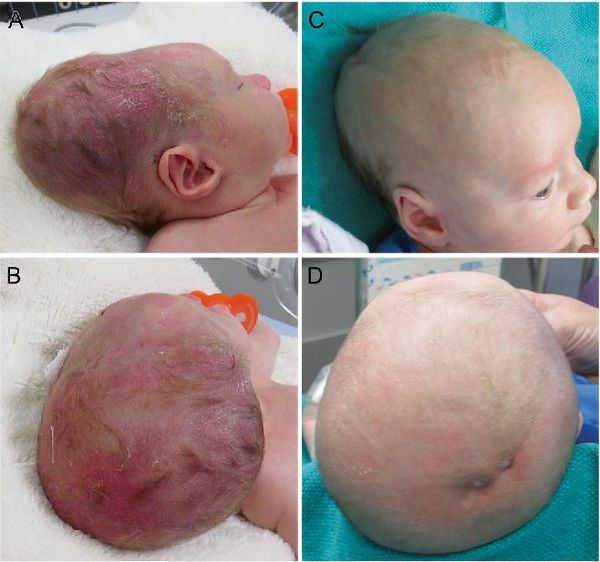
Кефалогематома проявляется как безболезненное образование на костях свода черепа с валикообразным уплотнением по переферии. Возникшей гематоме характерен симптом флюктуации — скопления крови в полости. Данное образование не пульсирующее, однако при нажатии на него ощущается пульсация и перемещение крови. Гематома имеет чёткие границы в пределах одной кости. При пальпации — упругая. Реже возможно появление множественных кефалогематом, которые поражают несколько участков головы.
Появляются данные симптомы в течение 2-3 часов после рождения либо в течение 2-3 суток. Они обнаруживаются неонатологом или педиатром в первые дни патронажа.
Патогенез кефалогематомы
Травма возникает в связи одновременным смещением (отслойкой) кожи и надкостницы, а также разрывом сосудов в момент прохождения головы ребёнка через родовые пути. В результате возникает кровотечение, которое постепенно заполняет образовавшуюся полость. В связи с таким характером кровотечения опухоль может увеличиваться в размерах на протяжении 2-3 дней независимо от того, проявилась она до или после рождения.
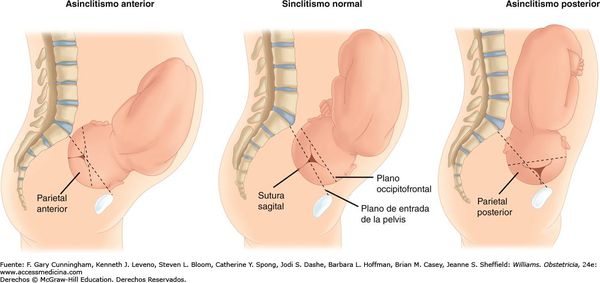
Основной причиной травмирования головки ребёнка является асинклитизм — неправильное положение головки плода относительно входа или полости малого таза. В таком случае головка (по стреловидному шву) отклонена от срединной линии таза к крестцу (передний асинклитизм) или лону (задний асинклитизм). При этом теменные кости расположены одна ниже другой.
Данная аномалия может возникнуть по причине расслабленного состояния брюшной стенки и нижней части матки, а также её появление зависит от размера готовки плода и состояния таза матери (суженный, плоский таз) и его угла наклонения.
Классификация и стадии развития кефалогематомы
По количеству возникших гематом различают:
По размеру кефалогематомы бывают (при множественных образованиях их объём суммируется):
По локализации образования выделяют:
По наиболее частым вариантам повреждения выделяют кефалогематомы:
Осложнения кефалогематомы
Редким осложнением кефалогематомы является инфицирование гематомы, которое происходит при хирургическом вмешательстве — удалении содержимого кефалогематомы (пункционная аспирация). Данное осложнение очень редко возникает в лечебной практике в связи с нечастым проведением данной операции.
Хирургическое лечение кефалогематом диаметром более 6 см показано из‑за опасности в дальнейшем оссификации гематомы, что может привести к деформации черепа.
У детей с такими гематомами в неонатальном периоде возникали такие осложнения как желтуха и анемия. [5]
Крайне редким осложнением кефалогематом является остеолизис костей черепа новорождённого — проявляется разрушением костной ткани [6] и считается показанием к проведению хирургического вмешательства.
Диагностика кефалогематомы
Диагностика кефалогематом не представляет сложности и выявляется, как описывалось выше, в течение 2-3 часов или двух суток после рождения. Подтверждается с помощью УЗИ мягких тканей головы, при котором выявляется наличие крови между надкостницей и костями свода черепа.
Возможные очаги повреждения в мозге и эхонегативную зону определяют с помощью нейросонографии.
К методам первичной диагностики относится рентгенологическое исследование костей черепа без введения контрастного вещества кефалогематома — краниография. С её помощью можно исключить костные повреждения и переломы.
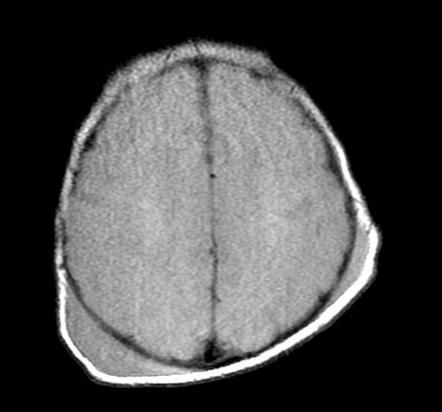
Также проводится мультиспиральная КТ, при которой диагностируются явления оссификации кефалогематомы или остеолизиса с образованием дефекта кости.
Лечение кефалогематомы
Лечение кефалогематомы носит в большинстве случаев охранительный характер и предполагает:
При отсутствии выраженного уменьшения кефалогематомы на протяжении 10-12 дней ребёнок должен быть осмотрен детским хирургом (но не позднее 15 дней с момента рождения). Осмотрев пациента и оценив состояние гематомы, врач принимает решение о дальнейшей тактике лечения. Если же кефалогематома уменьшилась, то хирургическое вмешательство не требуется.
Хотя возникновение кефалогематом — достаточно распространённое явление, всё же на сегодняшний день не существует единой схемы и единого представления при определении показаний к применению хирургического (пункционного) метода лечения. Несмотря на это данная терапия является весьма эффективным способом избавления от кефалогематом, так как препятствует оссификации и дальнейшему осложнению образования. [7]
Перед началом операции проводят общеклиническое обследование, краниографию, нейросонографию. В случае отсутствия противопоказаний согласно результатам обследований проводится пункция кефалогематомы.
После того, как пациента выписали, на следующие сутки участковый педиатр посещает его. Спустя 7-10 дней необходимо пройти контрольный осмотр у детского хирурга в поликлинике. В дальнейшем диспансерном наблюдении дети с кефалогематомой после пункционного лечения не нуждаются. [8]
Однако бывают случаи, когда заболевание обнаруживается только после выписки из род. дома. В таком случае следует обратиться к педиатру и придерживаться выжидательной тактики.
Прогноз. Профилактика
Прогноз для ребенка благоприятный, особенно при малых размерах кефалогематом. Единственный возможный дефект — косметический — может возникнуть в связи с оссификацией содержимого. Однако со временем он будет незаметен, так как его можно будет обнаружить только при прощупывании (незначительные бугры).
Профилактика возникновения кефалогематом у детей заключается прежде всего в профилактике осложнений и заболеваний у женщин в период беременности и их подготовке к родам. Это связано с тем, что процент рождаемости детей с такими травмами как кефалогематома достаточно велик по причине патологии беременности и родов. [9]
Применением антитромботических средств при риске невынашивания беременности, плацентарной недостаточности, позднем гестозе следует проводить курсами, а не беспрерывно, с отменой этих препаратов в 36 недель. [5]
Кефалогематома у детей
Кефалогематома — это родовая травма мягких тканей черепа, в результате которой между надкостницей и костью накапливается кровь. Сосуды плода очень хрупкие, и любое механическое влияние на них сопровождается повреждением сосудистой стенки и кровотечением. Свертываемость крови новорожденного также имеет некоторые особенности. Для формирования тромба организму ребенка требуется больше времени, чем взрослому.
Кефалогематома — довольно распространенная патология. На 1000 новорожденных приходится 2-5 ребенка с данной родовой травмой. Образовавшаяся гематома имеет тенденцию к постепенному увеличению, и на 2-3 день после рождения достигает своего максимального размера. Данное патологическое образование имеет вид опухоли, границы которой совпадают с краями кости (наиболее часто теменной и затылочной кости).
Актуальность проблемы кефалогематомы в педиатрической практике объясняется тесной взаимосвязью родовой травмы с патологией нервной системы. Травматическое поражение головного мозга у новорожденных с кефалогематомой встречается в 30% случаев.
Содержание:
Причины возникновения кефалогематомы
Механизм развития кефалогематомы заключается в повреждении сосудов надкостницы во время родов. Прохождение плода по родовым путям сопровождается неизбежным сдавливанием его головы костями малого таза матери. В норме костный череп плода представлен двумя лобными, двумя теменными, двумя височными и одной затылочной костью. Все они соединены между собою швами. Кости черепа у новорожденного подвижные, что имеет большое практическое значение: во время родов одна кость может частично смещаться на другую, тем самым уменьшая размеры головы. Таким образом, осуществляется более щадящее прохождение плода по родовым путям.
Кефалогематома возникает при выраженном смещении кожи с надкостницей относительно костного черепа, что приводит к травматическому разрыву сосудов. Между надкостницей и плоскими костями накапливается кровь, и образуется гематома. Чаще всего границы кефалогематомы совпадают с краями кости, но бывают случаи, когда после сильного растяжения фиброзной ткани «сухожильного шлема» возникают разлитые гематомы. Причины родовой травмы могут быть связаны с матерью, ребенком или патологией родовой деятельности.
Со стороны матери выделяют следующие факторы риска возникновения кефалогематомы у ребенка:
Со стороны ребенка возможны такие факторы риска:
Патология родовой деятельности повышает риск травмирования головы ребенка:
Виды кефалогематомы
Выделяют изолированную кефалогематому и сочетанную с:
В зависимости от размера патологического очага, выделяют 3 степени кефалогематомы:
По локализации кефалогематома бывает:
Симптомы кефалогематомы
Симптомы кефалогематомы особо выражены на 2-3 день после рождения ребенка. Форма головы становится асимметричной за счет формирования упругого и мягкого образования. Очертания припухлости совпадают с границами плоских костей черепа, поскольку надкостница прочно прикреплена к их краям. Типичной локализацией кефалогематомы является теменная и затылочная области головы. Кожа над образованием не изменена, упругая, при пальпации определяется флюктуация (движение жидкости при надавливании). Отличительная особенность кефологематомы – это постепенное увеличение образования на протяжении первых 2-3 дней жизни младенца. Количество крови под надкостницей может колебаться от 5 до 150 мл. В благоприятных условиях при маленьких размерах кефалогематома регрессирует уже через неделю после её образования самостоятельно.
При изолированной кефалогематоме общее состояние ребенка удовлетворительное. В случае сочетанной патологии появляется неврологическая симптоматика. У большинства детей наблюдается угнетение работы центральной нервной системы: вялая реакция на возбудители, снижение выраженности рефлексов. У некоторых новорожденных отмечается чрезмерное возбуждение центральной нервной системы по типу гипертензивного или гидроцефального симптомокомплекса.
Нарушение самостоятельной регрессии кефалогематомы (при больших размерах образования, нарушении свертываемости крови у младенца) может вызывать разные осложнения: анемия, резорбционная гипербилирубинемия, оссификация и инфицирование гематомы.
При больших кефалогематомах наступает быстрый гемолиз эритроцитов, что сопровождается желтоватым оттенком кожных покровов и видимых слизистых оболочек с первых дней жизни. Такая желтуха сохраняется на протяжении 10 и больше дней, в отличие от физиологической неонатальной желтухи.
Диагностика кефалогематомы
Диагноз кефалогематомы основывается на данных физикального осмотра грудного ребенка и сборе антенатального, интранатального и постнатального анамнеза. Выявление патологического новообразования на 2-3 день после рождения, размеры которого совпадают с краями кости черепа, – основные клинические критерии заболевания. Кефалогематому следует дифференцировать от родовой опухоли, подапоневротических кровоизлияний, мозговой грыжи.
Инструментальная диагностика назначается для уточнения размеров, распространенности и характера патологического новообразования, с целью исключения сочетанной патологии (перелома основания черепа):
Лабораторные исследования проводятся для изучения свертываемости крови ребенка, определения уровня эритроцитов, гемоглобина и билирубина:
Методы лечения кефалогематомы
Существует два метода лечения кефалогематомы: консервативный и хирургический.
Консервативное лечение направлено на восстановление свертываемости крови. Вскармливание ребенка в первую неделю после рождения при изолированной кефалогематоме — грудное, по требованию. В случае неврологической симптоматики может применяться сцеженное грудное молоко.
Хирургическое лечение показано в таких ситуациях:
Операция по удалению кефалогематомы осуществляется на 10-14 день после рождения. Аспирационным методом удаляется содержимое под надкостницей, после чего накладывается тугая повязка. В случае инфицирования гематомы образованную полость дренируют и назначают системные антибактериальные препараты. При оссификации кефалогематомы проводится резекция.
Последствия кефалогематомы
Осложнения кефалогематомы существенно ухудшают прогнозы касательно полного выздоровления ребенка и восстановления функции нервной системы:
Гематома в головном мозге у новорожденного
Данная статья и последующие ближайшие посвящены процессам от начала родов, включая сопутствующие патологические отклонения, до завершения неонатального периода, условно ограниченного первыми 28 днями после рождения. Основная часть неврологических проблем этого периода приходится на первые 10 дней после рождения. В неврологии перинатального периода доминируют внутричерепные кровоизлияния и гипоксически-ишемические поражения ЦНС, однако они не исчерпывают весь спектр возможных неврологических проблем, поэтому не следует упускать из виду возможность присутствия и других важных нарушений, такие как метаболические или нервно-мышечные заболевания.
Пре- и перинатальный периоды в настоящее время все чаще рассматриваются как единое целое, а не два отдельных периода. В определении многих перинатальных нарушений немаловажную роль, безусловно, играют пренатальные факторы: задержка внутриутробного развития, пренатальная гипоксия любого рода, пренатальное воспаление и преждевременные роды. Не менее важна реакция ЦНС на стресс в процессе родов и адаптацию к внеутробным условиям.
Кровоизлияние и гипоксия-ишемия, два основных патологических состояния перинатального периода, не могут считаться совершенно изолированными явлениями. Нередко они сосуществуют, имея отчасти общие причины и провоцирующие факторы. Впрочем, определенные процессы, допустим, механическая травма или коагулопатии, иногда провоцируют кровоизлияние без гипоксии, кроме того, разница патологии и механизмов достаточна для отдельного объяснения.
Эпидемиология внутричерепных кровоизлияний значительно изменилась за последние три десятилетия. В результате прогресса акушерской практики значительно снизилась частота посттравматических кровоизлияний, главным образом субдуральных. В то же время относительная частота внутрижелудочковых кровоизлияний (ВЖК) увеличилась, потому что эта патология характерна для недоношенных, а в еще большей степени для очень незрелых новорожденных, ранее не выживавших. За последнее десятилетие отмечается заметное снижение количества ВЖК у недоношенных новорожденных, что в значительной степени связано с улучшением акушерского ухода, учащением использования стероидов в антенатальном периоде, а также лучшим неонатальным уходом с доступностью искусственного сурфактанта и совершенствованием стратегий поддержки дыхательной функции.
Современные методы визуализации, ультрасонография и МРТ, обеспечивают возможность диагностики ВЖК и субарахноидальных кровоизлияний in vivo с недоступной ранее точностью. Без этих исследований многие кровоизлияния такого рода не были бы выявлены.
Выделяют две основные группы неонатальных внутричерепных кровоизлияний. Субдуральные кровоизлияния в основном имеют травматическое происхождение и возникают у доношенных новорожденных часто с большой массой при рождении (Welch и Strand, 1986). Towner et al. (1999) изучали влияние родоразрешения у первородящих на неонатальное внутричерепное повреждение. Они обнаружили, что по сравнению с родившимися естественным путем частота внутричерепных кровоизлияний у младенцев выше после родов с использованием вакуум-экстрактора, щипцов или после кесарева сечения. При этом показатель после планового кесарева сечения не повышался, подтверждая, что основным фактором риска кровоизлияний являются патологические роды. Внутрипаренхиматозные кровоизлияния также могут быть травматическими у той же категории детей (Pierre-Kahn et al., 1986). Аналогичные кровоизлияния выявлялись и при антенатальном скрининге, в некоторых случаях в связи с аутоиммунной тромбоцитопенией. Sandberg et al. (2001) описали 11 случаев спонтанных паренхиматозных кровоизлияний.
В восьми случаях потребовалась хирургическая декомпрессия, а в четырех из 11 развился двигательный дефицит. ВЖК преобладает среди недоношенных детей (Volpe, 2008). Другие типы кровоизлияний, например субарахноидальные, часто сопровождают ВЖК, но нередко остаются недиагностированными, если обследование ограничивается ультрасонографическим исследованием. Паренхиматозные гематомы, особенно в области зрительного бугра, могут возникать в результате синус-тромбоза в сочетании с ВЖК (Wu et al, 2003).
Внутричерепные кровоизлияния, не связанные с внутрижелудочковым кровоизлиянием (ВЖК):
1. Субдуральное кровоизлияние. Субдуральные кровоизлияния могут возникать в результате разрыва твердой мозговой оболочки с повреждением синусов или вены Галена, или мелких приводящих вен; затылочного остеодиастаза с разрывом поперечного синуса или мозжечковых вен; разрыва серпа с распространением на нижний сагиттальный синус; или повреждения мостовых вен между полушариями мозга и нижним сагиттальным синусом или между по-перечным/сигмовидным синусом и основанием мозга (Govaert, 1993; Volpe, 2001). В первых двух ситуациях гематома возникает в задней черепной ямке, тогда как в других случаях расположение супратенториальное, близко к поверхности полушарий при повреждении мостовых вен, к межполушарной борозде при разрывах серпа и на основании мозга при разрыве вен, впадающих в латеральный синус.
Разрыв твердой мозговой оболочки связан с крупными размерами черепа при головном предлежании или избыточной тракцией головки при тазовом предлежании (Раре и Wigglesworth, 1979). Локализованная травма с переломом костей при наложении щипцов встречается редко (Pierre-Kahn et al., 1986). Тенториальное кровоизлияние может также возникнуть как осложнение при использовании вакуум-экстрактора (Hanigan et al., 1990, Govaert, 1993). Также имеются сообщения о паренхиматозных кровоизлияниях в лобные доли и ассоциированных с ними субдуральных гематомах без выраженной травмы.
Клинические проявления разнообразны и зависят от локализации и остроты кровотечения. При острых кровоизлияниях в заднюю черепную ямку возможно массивное кровотечение с компрессией жизненно важных структур ствола мозга, проявляющейся ступором или комой, ригидностью мышц шеи, опистотонусом, девиацией глаз, брадикардией и кратковременным апноэ. Судороги развиваются в 36% случаев (Govaert, 1993). Возможно напряжение родничка, генерализованная гипотония или гипертония, косоглазие, парез лицевого нерва, анизокория. Из 90 новорожденных, обследованных Govaert (1993), летальный исход наступил у 15 неоперированных и трех прооперированных младенцев. Среди последствий отмечают гидроцефалию, но затруднение оттока может быть временным и купируется с помощью введения подкожного резервуара в боковой желудочек.
В подострых случаях начало неврологических симптомов может быть отсрочено на 12 часов или более. Диагноз может подтверждаться возбудимостью, ступором, выбуханием родничка и дыхательными расстройствами (Menezes et al., 1983, Fenichel et al., 1984). Достаточно большие скопления можно выявить при ультразвуковом исследовании. При КТ, а особенно МРТ, определяют размер и точную локализацию гематомы (Menezes et al., 1983, Govaert, 1993, Sandberg et al., 2001). Хирургическое лечение эффективно, но могут развиться спайки, которые приводят к гидроцефалии с неизбежной установкой шунта. Vinchon et al. (2005) с помощью чрескожной тонкоигольной аспирации уменьшили объем субдуральной гематомы в пяти из семи случаев, требовавших хирургической декомпрессии.
Супратенториальная гематома по выпуклой верхнелатеральной поверхности полушарий, как правило, проявляется не сразу. В типичных случаях на 2-3 сутки жизни возникают фокальные эпилептические припадки и/или асимметрия мышечного тонуса (Deonna и Oberson, 1974, Sandberg, 2001). Характерно развитие паралича III пары черепных нервов, проявляющегося в виде расширенного нереагирующего зрачка на стороне поражения. Небольшие субдуральные гематомы по верхнелатеральной поверхности мозга могут давать только минимальные клинические проявления (Whitby et al, 2004).
В случаях субдурального кровоизлияния цереброспинальная жидкость (ЦСЖ) обычно становится кровянистой. С учетом доступных в настоящее время различных методов визуализации люмбальные пункции для диагностики внутримозговых кровоизлияний более не рекомендуются.
Базальные субдуральные гематомы, возникающие в результате латерального тенториального повреждения, приводят к скоплению крови под височной и/или затылочной долями. Govaert (1993) изучил 21 подтвержденный КТ случай полушарных гематом с аналогичным механизмом возникновения. Такие случаи иногда связаны с артериальными инсультами из-за компрессии средней мозговой артерии (Govaert et al., 1992b). Сходные наблюдения отмечены при вовлечении задней мозговой артерии (Deonna и Prod’hom, 1980).
2. Внутримозжечковое кровоизлияние. Внутримозжечковое кровоизлияние имеет много общих признаков с субдуральной гематомой задней черепной ямки. Однако механизм иной, более вероятно связанный с гипоксией и ишемией, чем с механической травмой, хотя кровоизлияние возможно и при затылочном остеодиастазе или травматическом повреждении мозжечка (Welch и Strand, 1986, De Campo, 1989). Часто ассоциируется с ВЖК. Внутримозжечковое кровоизлияние распространено среди недоношенных новорожденных с низкой массой тела, и в настоящее время все чаще распознается при рутинных МРТ у всех недоношенных младенцев с очень низкой массой тела в некоторых отделениях интенсивной терапии (Merrill et al., 1998, Limperopoulos et al, 2005). У двадцати пяти из 35 новорожденных в исследовании Limperopoulos имелись односторонние полушарные кровоизлияния. Они могут возникать в результате прорыва ВЖК в четвертый желудочек или проникновения крови из субарахноидального пространства в паренхиму мозжечка, кроме этого, проявляться в виде первичной внутримозжечковой гематомы или геморрагического инфаркта (Takashima и Becker, 1989).
Одна из прежних гипотез рассматривала роль фиксаторов дыхательных масок, однако она оказалась малоубедительной, потому что заболевание встречалось и в ситуациях, когда маска не применялась (Paneth et al., 1994). Эта разновидность кровоизлияний наиболее распространена среди очень незрелых недоношенных новорожденных с гестационным возрастом до 27 недель (Limperopoulos et al., 2005). Неврологические проявления, как правило, затмеваются симптомами и признаками гипоксии-ишемии или респираторного дистресса.

Смертельный исход в возрасте пяти дней.
Частыми проявлениями являются приступы апноэ, брадикардия и сниженный гематокрит. Диагностика с помощью ультрасонографии возможна при больших размерах гематомы или исследовании с использованием заднебокового сегмента родничка в качестве акустического окна (Merrill et al., 1998). КТ и МРТ более эффективны для определения распространенности поражения. Обструктивная гидроцефалия характерна даже после хирургической эвакуации скоплений и может быть связана с развитием кисты мозжечка, сообщающейся с четвертым желудочком (Huang и Shen, 1991). Клинически в качестве остаточного явления может наблюдаться мозжечковый дефицит (Williamson et al., 1985). В качестве осложнения экстракорпоральной мембранной оксигенации (Bulas et al., 1991) и в некоторых случаях органической ацидурии (Fischer et al., 1981, Dave et al., 1984) наблюдалось мозжечковое кровоизлияние. Недавно были представлены данные о мозжечковой атрофии как о характерном последствии тяжелой недоношенности, которой предшествовало мозжечковое кровоизлияние в неонатальном периоде или повреждение супратенториального белого вещества (Bodensteiner и Johnsen, 2005, Johnsen et al., 2005, Messerschmidt et al., 2005, Srinivasan et al., 2006).
3. Внутрипаренхиматозное кровоизлияние. Внутрипаренхиматозное кровоизлияние фактически всегда сопровождается субарахноидальным кровоизлиянием. В большинстве случаев затрагивается одна доля в результате травмы или геморрагического инфаркта (Pierre-Kahn et al., 1986, Hayashi et al., 1987, Huang и Robertson, 2004). У пяти доношенных новорожденных, обследованных Pierre-Kahn et al. (1986), гематома сообщалась с субдуральным пространством и кровяной сгусток был окружен заметным массивным отеком паренхимы мозга. В качестве основного причинного фактора рассматривались роды в тазовом предлежании и сложные роды в целом, хотя о внутрипаренхиматозных кровоизлияниях сообщалось также в случаях неосложненных вагинальных родов (Sandberg et al., 2001). Дополнительную роль могут сыграть дефекты свертывающей системы, особенно при неонатальной алло- и изоиммун-ной тромбоцитопении (Hanigan et al., 1995, Berkowitz et al., 2006).
Симптоматика напоминает субдуральную гематому (Fenichel et al., 1984, Govaert, 1993) с бессимптомным периодом иногда на протяжении более 24 часов, после которого возникают очаговые признаки и симптомы повышенного внутричерепного давления. Разнообразие очаговых проявлений зависит от пораженной доли головного мозга и может включать судороги, ассиметричный мышечный тонус и глазную симптоматику.
Хирургическое удаление показано при симптомах повышенного внутричерепного давления, сопровождающегося смещением срединных структур, подтвержденным при нейровизуализации. Резидуальная полость в ткани мозга может не проявляться клинически, но может сопровождаться очаговым дефицитом (Pasternak et al., 1980). Сходная картина возможна при геморрагическом инфаркте мозга.
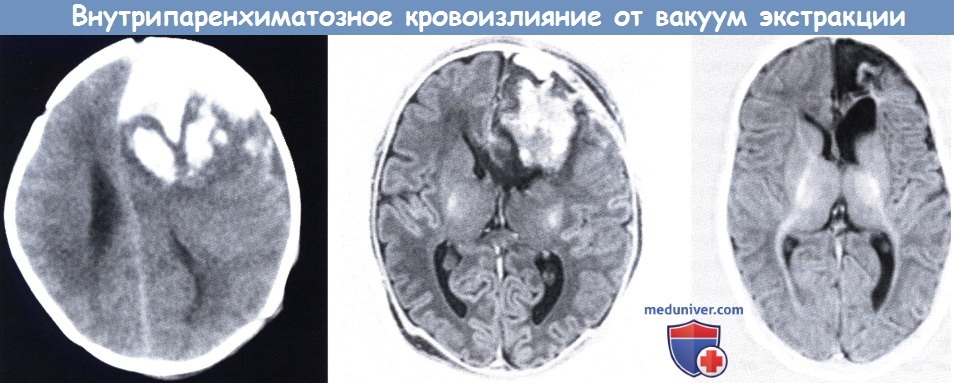
указывает на внутрипаренхиматозное кровоизлияние и субдуральную гематому со смещением срединных структур, (средний рисунок) МРТ (инверсия-восстановление),
конец первой недели после нейрохирургического вмешательства: все еще присутствуют крупное паренхиматозное кровоизлияние и незначительная асимметрия сигнала в заднем бедре внутренней капсулы (справа).
Повторное МРТ через три месяца указывает на дилатацию ex-vacuo и разрешение кровоизлияния. Имеется слабое замедление миелинизации переднего бедра внутренней капсулы.
Исход в течение 36 месяцев был благоприятным.
4. Кровоизлияние в таламус (зрительный бугор). Таламическое кровоизлияние представляет собой редкую форму неонатального внутримозгового кровоизлияния (Fenichel et al, 1984, Primhak и Smith, 1985, Trounce et al, 1985, Adams et al., 1988b, de Vries et al., 1992b). Кровоизлияние может быть ассоциировано с ВЖК (Roland et al., 1990, Govaert et al., 1992a, Govaert, 1993, Monteiro et al., 2001, Wu et al., 2003) или ограничиваться таламусом и окружающими структурами. Wu et al. (2003) недавно показали, что при сочетаниях таламического кровоизлияния с ВЖК есть основания для подозрения тромбоза венозных синусов. На стороне таламического кровоизлияния возможен некоторый венозный застой в перивентрикулярном белом веществе или даже венозный инфаркт. В настоящее время для подтверждения синус-тромбоза и решения о проведении антикоагулянтной терапии применяется допплеровское УЗИ через передний или задний родничок, а лучше КТ или МР венография. У новорожденных с таламическим кровоизлиянием, как правило, возникают судороги в промежутке между 2 и 14 сутками после нормальных родов.
Глазная симптоматика может включать вертикальный паралич взора вверх, девиацию глаз в сторону поражения, ипсилатеральный саккадический парез и уплощение вызванных зрительных потенциалов, и все они были отнесены к фронто-мезенцефалическому оптическому тракту (Trounce et al., 1985). Несмотря на кажущееся благоприятное течение болезни в раннем периоде новорожденности, Monteiro et al. (2001) сообщали о развитии эпилепсии с непрерывными комплексами «пик—медленная волна» во время сна в результате первичного неонатального таламического кровоизлияния. В литературном обзоре сообщается о возникновении эпилепсии у 13 из 28 новорожденных. Менее благоприятные исходы представлены также Campistol et al. (1994). Необходимо отличать одностороннее кровоизлияние в зрительном бугре от более тяжелого состояния в виде двустороннего вовлечения таламической области и базальных ганглиев у доношенных новорожденных с «практически полной острой асфиксией» (Barkovich, 1992, Rutherford et al., 1995) и, иногда, с геморрагическим характером (Kreusser et al., 1984, Voit et al., 1987).
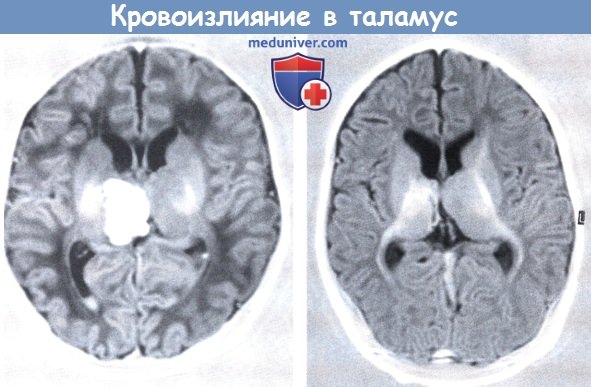
В коронарной проекции в режиме инверсии-восстановления определяется небольшое внутрижелудочковое скопление крови и крупное кровоизлияние в области правого таламуса,
которое почти полностью разрешилось по данным повторной МРТ, выполненной через три месяца.
5. Первичное субарахноидальное кровоизлияние. Кровоизлияние в субарахноидальное пространство, не связанное с распространением крови при внутрижелудочковых, субдуральных или внутрипаренхиматозных кровоизлияниях, представляет собой вполне обычное явление, связанное с обнаружением кровянистого или ксантохромного ликвора при выполнении люмбальной пункции в первые дни после рождения. Значительное субарахноидальное кровоизлияние, также видимое на КТ, распространено в меньшей степени. Escobedo et al. (1975) обнаружили, что только 29% новорожденных с массой
Редактор: Искандер Милевски. Дата публикации: 25.11.2018