гипоплазия синусов головного мозга и яремной вены
Алгоритм диагностики и терапии хронических форм нарушений венозного кровообращения
Изменения венозного кровообращения — один из важных патогенетических механизмов развития сосудистых заболеваний головного мозга. Выявление характерных «венозных жалоб» и своевременная комплексная терапия позволяют минимизировать патологические изменения и
Changes in venous blood circulation is one of important pathogenic mechanisms of development of cerebral vascular diseases. Reveal of typical «venous complaints» and timely complex therapy allow to minimize the pathological changes and eliminate phenomena of cerebral ischemia and hypoxia.
В РФ хронической венозной недостаточностью страдают 35–38 млн человек. К сожалению, стереотип, согласно которому патология вен считается только хирургической патологией, привел к тому, что огромное число больных не получают адекватной врачебной помощи [1]. Вместе с тем изменения венозного кровообращения являются одним из важных патогенетических механизмов развития сосудистых заболеваний головного мозга.
Регионарные изменения тонуса внутричерепных вен приводят к венозному застою и нарушению мозгового кровообращения при атеросклеротическом поражении сосудов мозга, артериальной гипертензии (АГ) и гипотензии, хронических заболеваниях легких, кардиальной патологии. Зафиксировано, что у 15% больных с АГ регистрируется компрессия яремных, брахиоцефальных и позвоночных вен, признаки нарушения венозного оттока головного мозга встречаются в 91% случаев АГ, а у больных с АГ 1–2 стадии — в 55% случаев [2, 3]. В то же время компенсаторные возможности головного мозга и его системы кровообращения так велики, что даже серьезные затруднения оттока венозной крови могут длительное время не вызывать клинических проявлений повышения внутричерепного давления и нарушения мозговых функций [4], поэтому ранняя диагностика данной патологии вызывает определенные трудности.
Для упрощения работы врача может применяться следующий алгоритм диагностики и терапии хронических форм нарушений венозного кровообращения.
Алгоритм диагностики и терапии хронических форм нарушений венозного кровообращения
Шаг 1. Выявление факторов риска
Врачу всегда следует помнить, что венозный застой в подавляющем большинстве случаев носит вторичный характер, т. е. возникает как симптом какого-либо основного заболевания, затрудняющего отток венозной крови из полости черепа. Поэтому диагностика прежде всего предусматривает выявление основной болезни (табл. 1).
Затруднение венозного оттока из полости черепа наблюдается при целом ряде заболеваний [5]:
Заболевания, вызывающие нарушение венозного оттока, приведены в табл. 1.
Кроме того, развитие венозной энцефалопатии может быть также обусловлено классическими причинами развития цереброваскулярной патологии: АГ, атеросклерозом, курением, сахарным диабетом, употреблением гормональных препаратов (эстрогенов), злоупотреблением алкоголем и наркотическими препаратами, использованием нитратов и некоторых вазодилататоров (никотиновая кислота, папаверин). Венозный отток может быть нарушен и в физиологических условиях, например, при натуживании, во время затяжного кашля, при физическом напряжении, пении, игре на духовых инструментах, родах, крике, нагибании головы (например, во время физкультурных упражнений), в положении лежа без подушки под головой, при сдавлении шеи тесным воротничком.
Шаг 2. Анализ жалоб и анамнеза
Нарушения венозного кровообращения, как правило, генетически детерминированы. В настоящее время роль исходного тонуса вен в формировании венозной дисциркуляции неоспорима. Конституциональный и наследственный факторы являются ключевыми для развития венозных дисгемий [6]. У пациентов с семейным «венозным» анамнезом обычно отмечается несколько типичных проявлений конституциональной венозной недостаточности — варикоз или флеботромбоз нижних конечностей, геморрой, варикоцеле, нарушение венозного оттока из полости черепа, варикозное расширение вен пищевода. Часто провоцирующим фактором является беременность.
Течение болезни имеет хронические, эпизодические и ремитирующие варианты.
Шаг 3. Осмотр пациента
При осмотре пациента обнаруживается «венозная триада»:
1) отечность лица в утренние часы после ночного сна, которая значительно уменьшается к вечеру при достаточной физической активности;
2) цианоз кожных покровов лица;
3) расширение подкожных вен шеи и лица.
При выраженном венозном застое больные не в состоянии опускать голову и долго находиться в горизонтальном положении. Артериальное давление (АД) у таких пациентов — обычно в пределах нормы, венозное давление колеблется от 55 до 80 мм вод. ст. Характерна низкая разница между систолическим и диастолическим давлением, в отличие от АГ. В тяжелых случаях возможны эпилептические припадки, психические расстройства [7]. Для венозной дисциркуляции характерно снижение корнеальных рефлексов. При пальпации определяется болезненность в точках выхода первой, реже второй ветвей тройничного нерва («синдром поперечного синуса») с формированием гипестезии в зоне иннервации первой ветви тройничного нерва, что, вероятно, связано с развитием невропатии, вызванной венозным застоем и нарушением микроциркуляции в системе vaza nervorum [8].
По типу превалирующего симптома выделяют следующие варианты хронической венозной недостаточности (энцефалопатии): цефалгический, гипертензионный (псевдотуморозный), беттолепсия, полиморфный (рассеянного мелкоочагового поражения мозга), синдром апноэ во сне, психопатологический/астеновегетативный [9].
Цефалгический синдром — наиболее частое клиническое проявление патологии венозной системы. Как правило, головная боль нарастает при движениях головой в стороны, перемене атмосферного давления, смене температуры окружающей среды, после волнения, приема алкоголя и др. Этот синдром имеет ряд характерных признаков (табл. 2).
Гипертензионный (псевдотуморозный синдром) характеризуется клиническими признаками повышения внутричерепного давления (ВЧД) при отсутствии очаговых неврологических симптомов, наличием застойных дисков зрительного нерва [10]. Развивается остро. Больные, как правило, жалуются на интенсивные приступообразные головные боли, эйфоричны, раздражительны, нередко гневливы. Появляется брадипсихизм с замедленностью движений. При исследовании ликвора обращает на себя внимание повышенное давление. Содержание белка незначительно увеличено или нормально, цитоз не увеличен, серологические реакции отрицательны. Псевдотуморозный синдром при хронической венозной патологии необходимо тщательно дифференцировать с опухолями мозга.
Беттолепсия (кашлевые синкопы) — развитие кратковременного обморока с судорожными подергиваниями во время приступа кашля. Случаи «кашлевых» обмороков (беттолепсии) достаточно редки и составляют не более 2% среди больных с венозной патологией. Эта форма нарушения венозного кровотока развивается при:
В патогенезе главную роль играет гипоксия мозга, возникающая при затяжном кашле, обусловленная повышением внутриплеврального давления, нарушением венозного кровотока в системе верхней полой вены, замедлением легочного кровотока при нарастании внутриплеврального давления, с уменьшением наполнения левого желудочка кровью, замедлением сердечной деятельности, уменьшением минутного объема сердца. В большинстве случаев пароксизмы при кашле не имеют отношения к эпилепсии, поскольку развиваются по патогенетическим механизмам, характерным для обморочных состояний. Приступы кашля возникают у больных в положении сидя или стоя, нередко во время еды или вскоре после нее. Провоцирующие факторы: холодный воздух, резкий запах, табачный дым, чрезмерный смех и др. Одновременно с кашлем развивается гиперемия лица, сменяющаяся цианозом с выраженным набуханием вен шеи. Обычно предвестников нет, может быть только легкое головокружение. Потеря сознания возникает в течение первой минуты от начала кашля. Длительность синкопального состояния от нескольких секунд до минуты. Появляется цианоз, больные нередко падают, часто ушибаются, кашель прекращается, окраска лица меняется с цианотичной на мраморно-бледную. Судорог обычно не наблюдается (иногда возможны тонические судороги). Нет прикуса языка и непроизвольного мочеиспускания.
Беттолепсия наблюдается преимущественно у лиц старшего возраста с хроническими заболеваниями дыхательных путей и легких (фарингит, ларингит, эмфизема легких, бронхиальная астма и др.). В более молодом возрасте появление обмороков при кашле наблюдается достаточно редко, главным образом, у лиц с повышенной чувствительностью каротидного синуса, либо при функциональной недостаточности механизмов, поддерживающих постуральный тонус.
Синдром рассеянного мелкоочагового поражения мозга клинически проявляется отдельными симптомами, такими как асимметрия носогубных складок, легкий нистагм, небольшое пошатывание при ходьбе. Реже встречаются двигательные, чувствительные, координаторные нарушения. Может развиться паркинсоноподобный синдром [11].
Психопатологический и астеновегетативные синдромы наиболее ранние признаки венозной недостаточности. Для них характерно наличие повышенной утомляемости, раздражительности, неустойчивое или плохое настроение, расстройства сна в виде постоянной сонливости или упорной бессонницы, вегетативные нарушения (неприятные ощущениями со стороны сердца, одышка, гипергидроз конечностей). Возможно развитие гиперестезии (непереносимости яркого света, громких звуков, резких запахов), интеллектуальные расстройства (расстройства внимания и памяти, способности к концентрации). Нередко наблюдаются головные боли. У больных отмечается изменение психического состояния в зависимости от атмосферного давления: при его падении повышается утомляемость, усиливается раздражительная слабость, гиперестезия (симптом Пирогова). В редких случаях развиваются психозы с бредовыми идеями и зрительными и слуховыми галлюцинациями [12]. Определяющими для астении являются постоянные жалобы на повышенную утомляемость, слабость, истощение после минимальных усилий в сочетании не менее чем с двумя из нижеперечисленных жалоб:
Наиболее характерные признаки астенических расстройств можно разделить на несколько групп в зависимости от доминирующих жалоб [13].
1. Физические расстройства:
2. Интеллектуальные расстройства:
3. Психологические расстройства:
4. Сексуальные расстройства:
Психопатологический и астеновегетативные синдромы преимущественно развиваются у пациентов молодого и среднего возраста.
Синдром апноэ во сне. У больных с ночными апноэ установлены отсутствие физиологического ночного снижения АД, нарушение церебральной венозной гемодинамики.
Шаг 4. Дополнительные методы исследования
Для более точной диагностики используются инструментальные методы исследования: офтальмоскопия, рентгенография черепа (краниография), ультразвуковые (УЗ) методы исследования венозной системы мозга, компьютерная томография или магнитно-резонансная томография, ангиография головного мозга. При проведении любого диагностического исследования необходимо учитывать, что венозная циркуляция чрезвычайно лабильна, и это связано с состоянием центральной гемодинамики, дыхательным циклом, мышечной активностью, позой. Желательно проведение обследования в дни с благоприятной геомагнитной ситуацией, при условии отсутствия у пациента повышения АД на момент осмотра, жалоб на головную боль и ощущение «тяжести» в голове в течение последней недели. В течение нескольких дней пациенты не должны принимать алкоголь. У женщин репродуктивного возраста оценку церебральной гемодинамики желательно проводить в первой половине менструального периода.
На краниограммах можно выявить усиление сосудистого рисунка, расширение диплоических вен, венозных выпускников. Офтальмологические методы позволяют уже на ранних стадиях сосудистых заболеваний головного мозга наряду с изменением артерий обнаружить расширение вен, их извитость, неравномерность калибра, при выраженном повышении внутричерепного давления — застойные явления на глазном дне. Достаточно информативны методы биомикроскопии конъюнктивы глазного яблока и венозной офтальмодинамометрии. Для уточнения причин и степени нарушения венозного оттока на уровне шеи используют ультразвуковое дуплексное сканирование (УЗДС), селективную контрастную флебографию, сцинтиграфию и компьютерную томографию. Каждый из этих методов имеет преимущества и недостатки. УЗДС позволяет достоверно оценивать скорость кровотока, взаимоотношения сосудов с окружающими тканями, но имеет ограничения, поскольку для исследования доступен сравнительно небольшой участок брахиоцефальных вен. Селективная контрастная флебография связана с определенным риском при введении контрастного вещества, часто неоправданным при данной патологии [15]. Сцинтиграфия не дает информации об окружающих вены структурах. Стандартная компьютерная томография позволяет оценивать диаметр вен и их взаимоотношения с окружающими структурами только в поперечных срезах, но не отображает характеристик потока крови, а кроме того, сопровождается лучевой нагрузкой. Магнитно-резонансная венография головного мозга характеризуется снижением интенсивности сигнала кровотока, вплоть до его выпадения, по верхнему сагиттальному синусу, большой мозговой вене и прямому синусу. Возможно также уменьшение размеров или полное отсутствие сигнала от кровотока по поперечному и сигмовидному синусам, внутренней яремной вене одной из гемисфер головного мозга, сочетающееся с расширением названных венозных структур с противоположной стороны; расширением эмиссарных и поверхностных мозговых вен [16].
Шаг 5. Выбор терапии
К сожалению, вопросы фармакотерапии расстройств венозного мозгового кровообращения до сих пор остаются спорными и недостаточно изученными, несомненно, что в первую очередь необходимо проводить терапию основного заболевания. Максимально ранняя энергокоррекция может дополнительно повлиять на выживаемость нейронов, уменьшить повреждение мозговой ткани, вызванной хронической ишемией и гипоксией, прежде всего, воздействовать на ядро астенического синдрома — гипоэргоз с повышенной истощаемостью психических функций [17]. С учетом современных представлений о патогенезе венозной энцефалопатии, основные усилия должны быть направлены на устранение следующих патологических факторов:
1) нормализацию тонуса венозного русла;
2) лейкоцитарной агрессии и воспаления;
3) коррекцию микроциркуляторных расстройств;
4) увеличение емкости венозного русла.
При лечении хронических нарушений венозного кровотока на различных стадиях чаще всего используются фармацевтические препараты, относящиеся к различным группам (антикоагулянты, средства, улучшающие микроциркуляцию, венотоники). Спектр действия большинства препаратов достаточно узок (декстраны влияют на реологию крови, антиагреганты уменьшают агрегационную активность тромбоцитов, венотоники улучшают тонус венозной стенки, вазодилататоры усиливают гипотонический эффект и т. д.), следовательно, для достижения оптимального терапевтического эффекта необходимо использовать несколько препаратов разных групп [2]. В последние годы идет поиск идеального препарата для лечения расстройств венозного мозгового кровообращения, который должен воздействовать на как можно большее количество патогенетических звеньев, иметь минимальное количество побочных эффектов и высокую биодоступность. Естественно, что наибольший интерес представляют препараты, имеющие в спектре своей фармакологической активности энергокорригирующие и микроциркуляторные механизмы действия при максимальной возможности сочетания с венотоническими лекарственными средствами.
Терапия нарушений венозного кровообращения
Клиническая симптоматика поражения мозга на начальных стадиях нарушения венозного кровообращения минимальна, но микроциркуляторное русло уже повреждено, что приводит к дальнейшей прогрессии патологического процесса, таким образом, базовой терапией является назначение препаратов, обладающих ангиопротекторным эффектом.
Ангиопротекторы
Первой группой базовой терапии являются ангиопротекторы — лекарственные средства, основные действие которых — восстановление тонуса сосудов и их проницаемости. Как правило, они к тому же обладают полимодальным механизмом действия.
Одним из таких фармакологических средств является Актовегин — препарат, активирующий обмен веществ в тканях, улучшающий трофику и стимулирующий процессы регенерации. Особое значение в его механизме действия придают активирующему влиянию на энергетический метаболизм клеток различных органов [18]. Это связано, прежде всего, со способностью повышать захват и утилизацию глюкозы и кислорода, приводя к улучшению аэробной продукции энергии в клетке и оксигенации в микроциркуляторной системе. Одновременно улучшается анаэробный энергообмен в эндотелии сосудов, сопровождающийся высвобождением эндогенных веществ с мощными вазодилататирующими свойствами — простациклина и оксида азота. В результате улучшается перфузия органов и снижается периферическое сопротивление [19]. Этот механизм обеспечивает стабилизацию функционального метаболизма тканей в условиях временно индуцированного стресса и гипоксии при периферических артериальных расстройствах. Улучшение процессов утилизации тканями кислорода и глюкозы не изолировано, а сопряжено с изменениями функционального состояния как путей притока крови к капиллярам (артериолы) и путей ее оттока (посткапиллярные венулы), так и с изменениями параметров гемодинамики на уровне капилляров [20].
М. В. Путилина, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Гипоплазия артерии – проявления и лечение
Термин «гипоплазия» означает «недоразвитие». Такие дефекты внутриутробного развития встречаются и в артериях головного мозга. В артериях бассейна сонных артерий эти аномалии существуют приблизительно у 4% людей, а в артериях вертебро-базилярного бассейна – у каждого десятого.
Несмотря на то, что головной мозг самый энергоемкий орган и нуждается в массивном кровоснабжении, гипоплазия питающих его артерий может долго оставаться незамеченной. Это связано с особенностями системы кровообращения головного мозга.
За счет передней и задней соединительных артерий образуется сообщение артериальных бассейнов мозга, образующее круг. Он называется виллизиевым, и в его пределах возможен компенсаторный переток крови в участки с пониженным артериальным кровотоком, в том числе по причине гипоплазии какого-либо сегмента артерии. Именно эта особенность кровообращения мозга обеспечивает длительное бессимптомное течение большинства гипоплазий, которые нередко становятся случайной находкой.
Клинические проявления гипоплазии артерий мозга возникают на фоне другой патологии, ухудшающей условия компенсации мозгового кровообращения. Чаще всего это атеросклероз сосудов головного мозга или заболевания шейного отдела позвоночника. В результате могут возникать транзиторные ишемические атаки и ишемические инсульты.
Симптомы
Симптомы хронического нарушения кровообращения мозга зависят от сосудистого бассейна, в котором развивается ишемия ткани мозга. Всех пациентов может беспокоить:
Для гипоплазии артерий каротидного бассейна также характерны слабость и/или онемение в конечностях, нарушения речи. Для ишемии в бассейне позвоночных артерий – нарушения координации, неустойчивость походки.
Для диагностики гипоплазии мозговых артерий и определения лечебной тактики проводятся:
Консервативную терапию препаратами, улучшающими кровоснабжение и метаболизм головного мозга, проводят, если данные выполненного обследования позволяют заключить, что она сможет предотвратить дальнейшее усиление ишемии мозга и ишемический инсульт.
Операции
Однако многие пациенты с декомпенсацией кровоснабжения мозга на фоне гипоплазии артерий нуждаются в хирургическом лечении. В ведущих нейрохирургические центрах мира проводятся сложнейшие микрохирургические операции шунтирования артерий мозга, а также малоинвазивные рентгенхирургические внутрисосудистые вмешательства – баллонная ангиопластика и стентирование артерий.
Операция проходит под общим наркозом и продолжается четыре-пять часов. Сначала выделяется теменная ветвь поверхностной височной артерии (она располагается в покровах черепа). Затем проделывается трепанационное отверстие в височной кости. И далее операция проходит с использованием операционного микроскопа и микрохирургических инструментов. Выделяется крупная корковая ветвь средней мозговой артерии и соединяется с ветвью височной артерии с помощью сосудистого шва, выполненного микронитью.
Для подтверждения прочности анастомоза еще до окончания операции выполняют контактное допплеровское исследование заинтересованных сосудов.
В дальнейшем пациент находится сначала в реанимационном, а затем – в послеоперационном отделении в течение 6-7 дней. За это время неоднократно проводятся контрольные допплерография и МРТ головного мозга.
Для поддержания нормального просвета сосуда баллонную ангиопластику часто комбинируют со стентированием сосуда специальной внутрисосудистой сетчатой конструкцией.
Сегодня в крупных многопрофильных иностранных клиниках используется более 400 моделей стентов. Это саморасправляющиеся конструкции из инертных для организма материалов. Они обладают памятью формы, могут устанавливаться в области извитостей и бифуркаций (раздвоений) сосудов, не деформируются с течением времени. Многие модификации длительно выделяют из своего покрытия препараты, препятствующие тромбообразованию и образованию атеросклеротических бляшек в области стента. Также относительно недавно в зарубежную практику введены стенты четвертого поколения. Это биодеградирующиеся конструкции, которые рассасываются в течение нескольких лет после выполнения функции.
Такой сложный раздел хирургии, как операции на сосудах головного мозга, требует не только особых навыков и многолетнего опыта нейрохирурга, который должен также владеть техникой ангиохирургических и микрохирургических вмешательств.
Необходимо современное оборудование – нейроэндоскопическая и микрохирургическая аппаратура, рентгенхирургические операционные, системы нейронавигации и интраоперационного мониторинга функций нервной системы, а также технически оснащенные реанимационные отделения для послеоперационных пациентов. Все эти условия созданы в крупных специализированных нейрохирургических зарубежных центрах, в которые обращаются самые сложные пациенты со всего мира.
Нарушение мозгового венозного кровотока у больных с гипертонической дисциркуляторной энцефалопатией
Изучить клинико-нейровизуализационные особенности венозной дисциркуляции у больных с гипертонической дисциркуляторной энцефалопатией (ГДЭ).
Материалы и методы
Были обследованы 132 пациента с ГДЭ, которых распределили на группы в зависимости от стадии ГДЭ, а также с учетом наличия конституциональной венозной недостаточности (КВН). Всем пациентам проведено полное клинико-неврологическое исследование, МРТ головного мозга и МР-венография.
У пациентов с КВН гипоплазия поперечных и сигмовидных синусов (57,5%), расширение поверхностных вен мозга (68,5 %) и вены Галена (65,6%), хронические тромбозы венозных синусов (24,7%) визуализировались чаще, чем у больных без КВН на всех стадиях ГДЭ. Установлена взаимосвязь выявленных изменений с клиническими проявлениями церебральной венозной дисциркуляции.
Применение методов нейровизуализации в сочетании с клинико-неврологическим исследованием позволяет оптимизировать этиопатогенетическую терапию, а также программу профилактических и реабилитационных мероприятий, которые должны проводиться с учетом выраженности венозных расстройств.
Хронические цереброваскулярные заболевания представляют собой важную медико-социальную проблему 1. Одной из наиболее распространенных форм хронических цереброваскулярных заболеваний является ГДЭ [3,4], развитие которой во многом зависит от нарушения венозного компонента церебральной гемодинамики, что может быть обусловлено наличием как врожденных причин в виде конституциональной венозной недостаточности (КВН), так и, в соответствии с концепцией «энцефалопатии пульсовой волны», формироваться вторично при гипертоническом поражении сосудов 8. В настоящее время выделен патогенетический подтип ГДЭ, сопровождающейся КВН, описан его клинико-неврологический симптомокомплекс, с помощью ультразвуковых методов изучено состояние гемодинамики на всех структурно-функциональных уровнях сосудистой системы мозга [7,8,10]. Тем не менее, в полной мере оценить структурное состояние венозного компонента сосудистой системы мозга ультразвуковыми методами диагностики не представляется возможным [11]. Внедрение в клиническую практику магнитно-резонансной томографии (МРТ) открыло новые перспективы в изучении венозной системы головного мозга [12].
Целью исследования было изучить клинико-нейровизуализационные особенности венозной дисциркуляции у больных ГДЭ.
Материал и методы
В исследование включали пациентов с артериальной гипертонией, сопровождавшейся ГДЭ, которые были обследованы в неврологическом отделении для больных с нарушением мозгового кровообращения ГУЗ «Центральная клиническая медико-санитарная часть им. заслуженного врача России В.А. Егорова» г. Ульяновска. Клиническими критериями КВН были «венозные» жалобы, обусловленные венозной церебральной дисциркуляцией, такие как пастозность лица и век в утренние часы, симптом «тугого воротника», симптомы «песка в глазах» и «высокой подушки», семейный «венозный» анамнез, наличие типичных проявлений венозной патологии (варикозное расширение и тромбоз вен нижних конечностей, геморрой, варикоцеле, варикозное расширение вен пищевода) и неврологических симптомов, в развитии которых особую роль играет венозная дисциркуляция. Критерием исключения служили соматические заболевания, которые могут быть причиной вторичных нарушений венозного кровообращения [10].
МРТ проводили на аппарате Siemens Magnetom Symphony с силой поля 1,5 Тесла. Исследование параметров церебрального венозного оттока осуществляли с использованием времяпролетной МР-венографии (Time of flight – TOF) в двухмерном (2D) изображении.
Статистический анализ полученных результатов проводился с использованием пакета прикладных программ Statistica 8.0 и Excel. Для проверки гипотезы о различии выборок групп больных использовали U-тест Манна– Уитни, а для определения связи между количественными показателями – непараметрический корреляционный анализ Спирмена. Результаты представлены в виде медианы, 25% и 75% квартилей – Мe [25%; 75%]. Различия считали достоверными при р
Результаты
Обследовали 132 пациентов с ГДЭ, в том числе 47 мужчин и 85 женщин в возрасте от 41 до 76 лет (в среднем 60±10,7 лет). Все пациенты страдали гипертонической болезнью в течение более 5 лет (в среднем 11,2±7,2 лет). В соответствии с классификацией Научного центра неврологии (1985 г.) у 37 (28,1%) пациентов диагностирована ГДЭ I стадии, у 51 (38,6 %) – II стадии, у 44 (33,3 %) – III стадии. Контрольную группу составили 30 человек с нормальным АД, в том числе 17 женщин и 13 мужчин в возрасте в среднем 59,4±10,3 лет.
| КВН (n=73) | КВН (n=59) | |
|---|---|---|
| Примечание: *p | ||
| Женщины, n (%) | 48 (65,8) | 37 (62,7) |
| Средний возраст, лет | 56,4±10,2 | 60,5±11,8 |
| Стадия ГДЭ, n (%) | ||
| I | 21 (28,8) | 16 (27,1) |
| II | 29 (39,7) | 22 (37,3) |
| III | 23 (31,5) | 21 (35,6) |
| Симптомы, n (%) | ||
| Симптом «тугого воротника» | 49 (67,2)* | 24 (40,7) |
| Симптом «высокой подушки» | 50 (68,5)* | 23 (38,9) |
| Симптом «песка в глазах» | 55 (75,3)* | 22 (37,3) |
| Пастозность лица и век в утренние часы | 60 (82,2)* | 22 (37,3) |
Признаки КВН выявили у 73 (55,3%) пациентов. Группы пациентов с КВН и без КВН не отличались по возрасту, полу и стадиям ГДЭ (табл. 1). «Венозные» жалобы у больных с КВН встречались достоверно чаще, чем в группе сравнения. Снижение корнеальных рефлексов, болезненность точек выхода и гипестезия в зоне иннервации первой ветви тройничного нерва и диссоциация коленных и ахилловых рефлексов, в развитии которых играет роль венозная дисциркуляция, у пациентов с КВН определялись уже на I стадии ГДЭ и наблюдались чаще, чем у пациентов без КВН, на всех стадиях ГДЭ (р ТАБЛИЦА 2. Неврологические симптомы церебральной венозной дисциркуляции у больных с КВН и без КВН, n(%)
иннервации первой ветви тройничного нерва
Результаты визуализации анатомического строения интракраниальной венозной системы по данным МРвенографии представлены в (табл. 3). Симметричное строение поперечных и сигмовидных синусов у пациентов с КВН на всех стадиях ГДЭ определялось значительно реже, чем у пациентов без КВН (р ТАБЛИЦА 3. Анатомические варианты строения поперечных и сигмовидных синусов у больных с КВН и без КВН, n (%)
У больных с КВН диаметры поверхностных вен и вены Галена превышали таковые у пациентов без КВН и пациентов контрольной группы и нарастали по мере прогрессирования ГДЭ. У больных ГДЭ III стадии они были значительно больше, чем у пациентов с ГДЭ I стадии (p ТАБЛИЦА 4. Размеры венозных структур (мм) по данным МР-венографии в группах больных с КВН и без КВН.
В соответствии с триадой R. Virchow (1856) стаз и иммобилизация крови в венозном русле играют важную роль в развитии венозного тромбоза [14]. В нашем исследовании при МР-венографии определялись тромбозы поперечных и сигмовидных синусов, сигнальная характеристика которых соответствовала диагностическим нейровизуализационным критериям тромбоза в хронической стадии [15,16]. У больных с тромбозом отсутствовали указания в анамнезе на клинические состояния, соответствующие классическому описанию церебрального венозного тромбоза, который часто развивается подостро (в 50-80% случаев в течение от нескольких дней до одного месяца) [17,18] и характеризуется полиморфизмом и неспецифичностью клинической картины [19], особенно у пациентов с КВН. На фоне уже имеющихся венозных жалоб и относительной адаптации к клиническим проявлениям КВН не всегда заметно нарастание симптомов центрального венозного тромбоза, что обусловливает позднее обращение больных за медицинской помощью. Тромбозы поперечных и сигмовидных синусов у пациентов с КВН встречались чаще (24,7%), чем у больных без КВН (8,5%, p 0,05). В контрольной группе случаев тромбоза поперечных и сигмовидных синусов не выявлено.
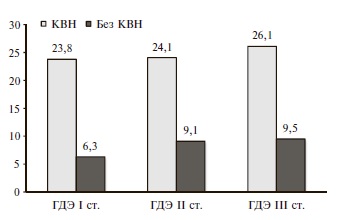
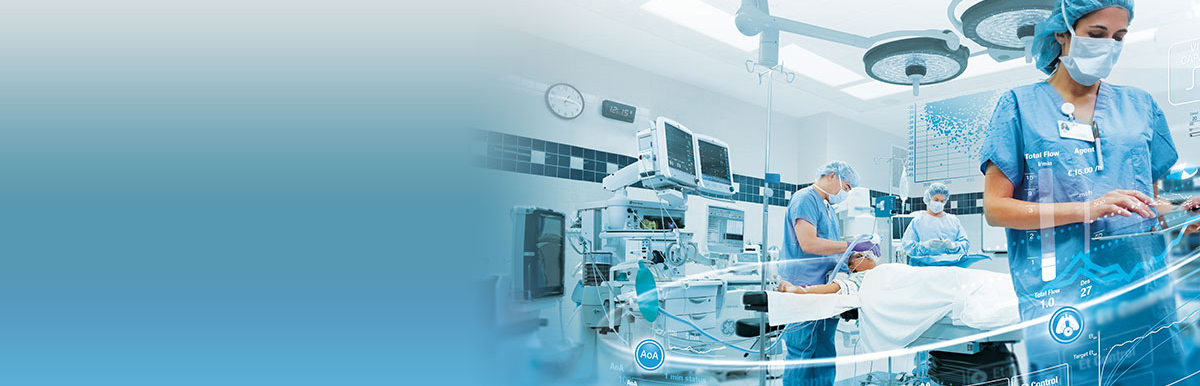
В целом при МР-венографии у 65,8% пациентов с КВН визуализировали расширение поверхностных вен головного мозга, у 57,5% – гипоплазию венозных синусов, у 64,4% – расширение вены Галена, у 24,7% – тромбозы венозных синусов (рис. 2).
| Расширение поверхностных вен | Расширение вены Галена | Гипоплазия венозных синусов | Тромбозы венозных синусов | |||||
|---|---|---|---|---|---|---|---|---|
| r | p | r | p | r | p | r | p | |
| Симптом «тугого воротника» | 0,46 | 0,03 | 0,52 | 0,02 | 0,54 | 0,02 | 0,47 | 0,03 |
| Симптом «песка в глазах» | 0,56 | 0,01 | 0,46 | 0,03 | 0,47 | 0,03 | 0,46 | 0,04 |
| Пастозность лица и век в утренние часы | -0,52 | 0,02 | -0,58 | 0,01 | -0,46 | 0,03 | -0,54 | 0,01 |
| Симптом «высокой подушки» | -0,47 | 0,02 | -0,44 | 0,04 | -0,42 | 0,04 | -0,48 | 0,03 |
| Снижение корнеальных рефлексов | 0,47 | 0,01 | 0,58 | 0,01 | 0,84 | 0,001 | 0,50 | 0,02 |
| Болезненность точек выхода и гипестезия в зоне иннервации первой ветви тройничного нерва | 0,42 | 0,04 | 0,48 | 0,02 | 0,80 | 0,01 | 0,46 | 0,04 |
| Диссоциация коленных и ахилловых рефлексов | 0,56 | 0,02 | 0,44 | 0,03 | 0,83 | 0,003 | 0,42 | 0,04 |
У больных с КВН наблюдалась корреляционная связь средней силы между расширением поверхностных вен и вены Галена, тромбозами венозных синусов и «венозными» жалобами и неврологическими симптомами церебральной венозной дисциркуляции, а также между гипоплазией венозных синусов и «венозными» жалобами (табл. 5). Обращало на себя внимание наличие высокой корреляции между гипоплазией венозных синусов и неврологическими симптомами церебральной венозной дисциркуляции.
Обсуждение
У больных ГДЭ с КВН в клинической картине заболевания существенное место занимают симптомы, свидетельствующие о венозной церебральной дисциркуляции и проявляющиеся уже на ранних стадиях ГДЭ. У пациентов без КВН нарастание клинических проявлений венозной дисциркуляции зависит от прогрессирования ГДЭ. МР-венография является важнейшим неинвазивным методом диагностики КВН у пациентов с ГДЭ. Нейровизуализационными коррелятами КВН у являются расширение поверхностных вен и вены Галена, гипоплазия и тромбозы венозных синусов в хронической стадии. При наблюдении больных ГДЭ, особенно при наличии КВН, необходим высокий уровень настороженности в отношении центрального венозного тромбоза вследствие неспецифичности, стертости и медленного нарастания симптоматики. Применение методов нейровизуализации в сочетании с клиниконеврологическим исследованием позволяет оптимизировать этиопатогенетическую терапию, а также программу профилактических и реабилитационных мероприятий, которые должны проводиться с учетом выраженности венозных расстройств у больного. Медикаментозная терапия должна быть направлена на облегчение венозного оттока из полости черепа.
Винпоцетин (Кавинтон®, «Гедеон Рихтер», Венгрия), производное алкалоида винкамина, содержащегося в растении барвинок малый, является препаратом выбора в лечении больных с церебральными венозными расстройствами, что обусловлено его воздействием на целый ряд патофизиологических процессов, вызывающих поражение эндотелия сосудов и нарушение церебральной, в том числе, венозной гемодинамики. Винпоцетин модулирует активность митохондриальной поры и предотвращает нарушение метаболизма в этих органеллах и гиперпродукцию активных форм кислорода (АФК) [20]. В эксперименте показано, что увеличение содержания АФК в сосудах приводит к стимуляции вазоконстрикции и ремоделирования с повышением системного сосудистого сопротивления, а увеличение концентрации АФК в головном мозге вызывает стимуляцию нейронов с увеличением симпатической активации и продукции провоспалительных цитокинов, воздействующих на эндотелий сосудов [21]. Кроме того, винпоцетин ингибирует фосфодиэстеразу и увеличивает уровень цГМФ в сосудистом эндотелии, что способствует вазодилатации [20], а также уменьшает выделение воспалительных цитокинов и хемокинов из эндотелиальных клеток, гладкомышечных клеток сосудов, макрофагов и микроглии путем ингибирования сигнального пути NF-κB [21]. Таким образом, препарат оказывает положительное действие на мышечную стенку и эндотелий сосудов и улучшает состояние церебральной гемодинамики в целом.
Благоприятное влияние винпоцетина на артериальные сосуды, вероятно, реализуется посредством воздействия как на мышечную стенку, так и на эндотелий. Предотвращая нарастание гипертонического или атеросклеротического ремоделирования, уменьшая периферическое сосудистое сопротивление, нормализуя пульсацию и улучшая вазоактивные свойства артерий, винпоцетин способствует улучшению и венозной гемодинамики, так как отток в венах осуществляется пассивно, в том числе за счет проталкивания крови. В венозных сосудах, с их невыраженной мышечной стенкой, вазоактивный эффект винпоцетина, вероятнее всего, преимущественно определяется воздействием на эндотелий, который, в отличие от артериального, обладает большей восприимчивостью к провоспалительным цитокинам, фактору некроза опухоли, липополисахаридам и запрограммирован на более высокий уровень адгезионного ответа [22,23]. В связи с этим противовоспалительный и антиоксидантный механизмы действия винпоцетина имеют крайне важное значение в отношении именно венозного эндотелия.
Важнейшим эффектом винпоцетина, способствующим увеличению микроциркуляции и перфузии ткани мозга, является улучшение реологических свойств крови путем снижения ее вязкости. В свою очередь, вязкость крови во многом зависит от агрегации и деформируемости эритроцитов, составляющих 99% всех ее клеток. Исследования показали, что винпоцетин, увеличивая уровень цГМФ в мембранах эритроцитов, оказывает положительное влияние на их деформируемость у больных с хроническими цереброваскулярными заболеваниями [20] и инсультом [24]. Помимо защиты нейронов в условиях ишемии и гипоксии за счет улучшения перфузии данный механизм уменьшает вероятность развития церебральных венозных тромбозов вследствие улучшения текучести крови и уменьшения выраженности застойных явлений, прежде всего, в венозных структурах мозга, что имеет важное значение для больных ГДЭ [25]. Уменьшение вероятности развития венозных тромбозов при лечении винпоцетином происходит также за счет противовоспалительного действия препарата на венозный эндотелий. Наряду с этим, винпоцетин предотвращает развитие и артериальных тромбозов путем снижения агрегации тромбоцитов, увеличения простациклин-тромбоксанового соотношения, что приводит к увеличению защитного атромбогенного потенциала сосудистой стенки, в частности, его антиагрегационного звена [26].
Таким образом, терапия винпоцетином у больных с хроническими цереброваскулярными заболевания оказывает системное действие и улучшает состояние всей сосудистой системы мозга, в том числе, ее венозного компонента. Препарат оказывает выраженное проти вовоспалительное действие на венозный эндотелий, улучшает его барьерную функцию, способствует сохранению структурной целостности венозных сосудов, улучшает их функциональное состояние. Следствием этого является улучшение реактивности вен и оттока венозной крови от мозга и, как следствие, уменьшение застойных явлений в сосудах мозга и выраженности хронической гипоксии у данной группы больных. Наряду с этим, важнейшими механизмами действия препарата при восстановлении неврологического дефицита, уже сформировавшегося в условиях хронического нарушения мозгового кровообращения, являются активация периферических бензодиазепиновых рецепторов [20] и влияние на нейропластические процессы путем стимуляции экспрессии BDNF [27].
Клиническая эффективность Кавинтона® установлена в двойных слепых, плацебо-контролируемых, рандомизированных исследованиях у больных с различными формами цереброваскулярной патологии: уменьшение частоты жалоб на головную боль, головокружение, шум в ушах, выраженности когнитивных, эмоциональных и астенических расстройств, статических нарушений, снижение риска падений, регресс речевых, двигательных, мнестических расстройств, улучшения качества жизни [24,27-33]. Кроме того, последние исследования [34] позволили выявить уникальный механизм действия винпоцетина, аналогичный феномену ишемического прекондиционирования (феномен прерывистой ишемии или метаболической адаптации) и позволяющий рассматривать препарат как средство профилактики развития церебральных катастроф у больных с хроническими нарушениями как артериальной, так и венозной гемодинамики различной степени выраженности.
Следует отметить хорошую переносимость и безопасность терапии винпоцетином у больных различных возрастных групп, а также у пациентов с сопутствующими заболеваниями. Препарат хорошо сочетается с другими лекарственными средствами, в том числе его можно комбинировать с другими венотоническими препаратами и антиоксидантами.
Появление на фармацевтическом рынке инновационной лекарственной формы винпоцетина (Кавин тон® Комфорте) в виде диспергируемых (растворимых в воде или слюне) таблеток способствовало повышению приверженности к терапии и ее эффективности у ряда пациентов. Одним из наиболее важных преимуществ данной формы является высокая биодоступность, обусловленная тем, что микросферы, на которые распадается таблетка во время растворения в полости рта, защищают находящееся в них действующее вещество при прохождении по желудочно-кишечному тракту до всасывания в тонком кишечнике. Также растворение Кавинтон® Комфорте в полости рта исключает травматизацию слизистой оболочки желудка и обеспечивает оптимальную скорость всасывания препарата.
Кавинтон® Комфорте является предпочтительной формой для больных с нарушениями глотания, возникшими в результате хронического нарушения мозгового кровообращения, а также больных с острым инсультом или инсультом в анамнезе, у которых прием обычных таблеток и желатиновых капсул сопряжен с определенными трудностями. Тошнота, когнитивные и психоэмоциональные расстройства, часто возникающие при данных состояниях, также являются причиной выбора новой формы. С учетом отсутствия у Кавинтона® Комфорте отрицательного воздействия на слизистую оболочку желудка он является препаратом выбора для больных с сопутствующими заболеваниями желудочнокишечного тракта. Кроме того, Кавинтон® Комфорте не требуется запивать водой, что делает его применение удобным и комфортным для работающих, занятых пациентов, а также для путешественников.
Немедикаментозные методы лечения больных с хроническими цереброваскулярными заболеваниями должны включать соблюдение растительной диеты, дозированную дыхательную гимнастику, отводящий массаж головы и шеи, физиотерапевтические процедуры (гальванический воротник, СМТ на шейно-воротниковую зону, теплые ножные ванны). Для пациентов с хроническими цереброваскулярными заболеваниями, обязательным компонентом которых являются венозные расстройства различной степени выраженности, необходима разработка индивидуальной программы реабилитации. В соответствии с консенсусом International Union of Phlebology, основные составляющие реабилитационной программы больных с хроническими венозными заболеваниями включают лечебную физкультуру, адаптированную физическую нагрузку, психологическую и социальную поддержку. Особое внимание уделено необходимости системного подхода к пациентам с венозными расстройствами, индивидуальной разработке алгоритма реабилитационных мероприятий для каждой группы пациентов с учетом выраженности венозной недостаточности, возраста, двигательной активности, сопутствующих заболеваний, состояния психического здоровья. Отмечена необходимость проведения рандомизированных контролированных исследований для оценки эффективности многочисленных реабилитационных протоколов.
.gif)
_575.gif)