химия терапия при онкологии головного мозга
Хирургия головного мозга
(495) 506 61 01
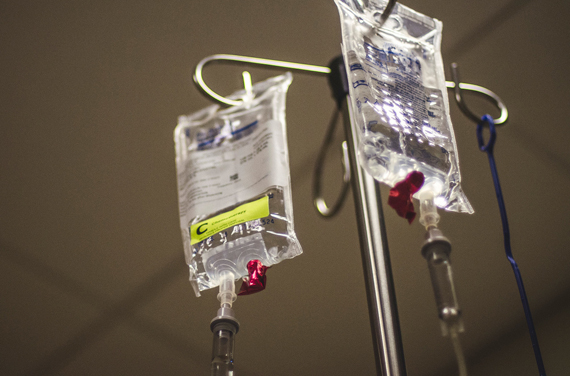
Химиотерапия при опухолях головного мозга
Химиотерапия является одним из трех основных методов лечения злокачественных опухолей. Принцип химиотерапии заключается в том, что пациенту назначаются особые цитотоксические препараты, которые губительно действуют на быстроразмножающиеся клетки, к которым и относятся опухолевые клетки. К химиопрепаратам относится много групп химических веществ, каждая из которых обладает своим механизмом действия, конечной целью которого является разрушение клеток опухоли.
Такая особенность опухолевых клеток, как усиленный метаболизм и размножение ввиду генетических мутаций в них, играет важную роль в применении цитостатиков. Это делает их чувствительными к химиопрепаратам. Однако, кроме опухолевых клеток в организме имеются и другие здоровые клетки, которые также характеризуются повышенным метаболизмом и усиленным размножением. Это клетки эпителия, а также клетки костного мозга, которые отвечают за кроветворение и иммунную систему. Химиопрепараты влияют, таким образом, не только на опухоль, но и на здоровые ткани, что приводит к известным побочным реакциям.
Обычно, химиотерапия при опухолях мозга проводится курсами, которые чередуются перерывами. Эти перерывы нужны для организма как передышка, чтобы он мог восстановиться. Следует отметить, что химиопрепараты применяются каждый для определенных типов опухолей и поэтому химиотерапия назначается обычно после оперативного вмешательства, которое позволяет определить гистологический тип опухоли мозга. Если же химиотерапия проводится без предварительной операции на мозге, то для определения гистологического типа опухоли делается т.н. стереотаксическая биопсия мозга. При этом химиотерапия может проводиться различными способами, который выбирает лечащий врач.
При системном введении химиопрепарата пациент получает лекарство внутривенно или перорально в виде таблеток. Такой способ характеризуется наибольшим риском побочных эффектов. При регионарном введении химиопрепаратов лекарственное средство вводится непосредственно в артерии, которые кровоснабжают область расположения опухоли.
При интратекальном способе химиопрепарат вводится путем люмбальной пункции в цереброспинальный ликвор. Таким образом, цитостатик действует непосредственно на ткань мозга. Этот способ используется при данном расположении опухолей. В случае, когда химиопрепарат вводится непосредственно в ткань опухоли, говорят об интерстициальном методе химиотерапии.
В химиотерапии опухолей мозга также применяется т.н. конвекционный методе доставки препарата в опухоль. При этом в саму ткань опухоли или окружающие мягкие ткани имплантируется тонкий пластиковый катетер, через который постоянно медленно вводятся необходимые химиопрепараты, обычно в течение нескольких дней.
Обычно при химиотерапии используется схема, в которой применяется несколько цитостатических препаратов в определенной дозе в течение определенного времени.
Среди химиопрепаратов, которые применяются в лечении опухолей мозга, широкое применение на сегодня нашли такие средства, как Темозоломид и Кармустин, а также препараты на основе платины цисплатин (Платинол) и карбоплатин (Параплатин). Кроме указанных средств, исследователи сегодня изучают возможность применения и других цитостатиков для лечения опухолей мозга.
Среди побочных эффектов химиотерапии опухолей мозга можно отметить все те эффекты, которые встречаются при химиотерапии других видов злокачественных опухолей.
Как уже было сказано, химиопрепараты губительно действуют на клетки с усиленным метаболизмом и быстрым ростом. К таким клеткам относятся не только опухолевые клетки, но и клетки здоровых тканей: клетки эпителия ЖКТ и волосяных луковиц, а также клетки костного мозга, который относится к кроветворной системе. Дело в том, что эпителий в организме у нас постоянно обновляется, а клетки костного мозга так же постоянно обновляют состав форменных элементов крови. С этим-то и связаны все побочные эффекты химиотерапии.
В костном мозге происходит созревание форменных элементов крови: эритроцитов, лейкоцитов и тромбоцитов. Эти клетки характеризуются интенсивным развитием, в результате чего их созревание во время химиотерапии страдает. Возникает анемия, лейкоцитопения и тромбоцитопения. Это проявляется слабостью, быстрой утомляемостью, плохим аппетитом, шумом в ушах. Кожа становится бледной.
Лейкоцитопения ведет к снижению защитных сил организма и иммунитета. Могут легко присоединяться всякие инфекции. Профилактика инфекционных осложнений химиотерапии заключается в соблюдении пациентом личной гигиены и контакта с инфекционными больными. При развитии инфекции у таких больных в обязательном порядке используются антибиотики. В случае возникновения апластической анемии применяются т.н. эритропоэтины, которые стимулируют созревание эритроцитов в костном мозге. Для стимуляции роста белых клеток крови используются т.н. колониестимулирующие факторы, среди которых известен такой препарат, как филграстим.
При снижении уровня тромбоцитов отмечается повышенная кровоточивость. На коже возникают т.н. петехии в виде мелкоточечной сыпи. При выраженной тромбоцитопении проводятся трансфузии тромбоцитарной массы.
Кроме влияния на указанные ткани и клетки, цитостатики влияют на эпителий органов ЖКТ, что проявляется тошнотой, рвотой, чувством дискомфорта в животе, вздутием и диареей.
Химиопрепараты негативно влияют и на репродуктивную систему как женщин, так и мужчин, приводя к вторичному бесплодию. У женщин химиотерапия может привести к появлению симптомов менопаузы в виде приливов жара, сухости во влагалище и нарушений менструального цикла.
Химиотерапия оказывает неблагоприятное воздействие и на функцию почек, а также печени. Для снижения негативных эффектов на эти органы при химиотерапии рекомендуется пить больше жидкости, чтобы быстрее вывести токсические вещества из организма.
(495) 506-61-01 — где лучше оперировать головной мозг
Кибер-нож в лечении опухолей головного мозга
На базе нейрохирургической клиники Аахенского Университета с 1998 года применяется специальная методика гамма-кобальтового облучения для лечения опухолей и сосудистых новообразований головного мозга. Подробнее
Национальный Онкоцентр Им. Сураски является интегральной частью крупнейшей муниципальной мед. клиники Сураски и предоставляет передовое лечение опухолей мозга всех видов.Подробнее
Материалы конгрессов и конференций
X РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ХИМИО- И ХИМИОЛУЧЕВАЯ ТЕРАПИЯ МЕТАСТАЗОВ НЕКОТОРЫХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ В ГОЛОВНОЙ МОЗГ
М.Б. Бычков, В.А. Горбунова, Д.Р. Насхлеташвили, З.П. Михина
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
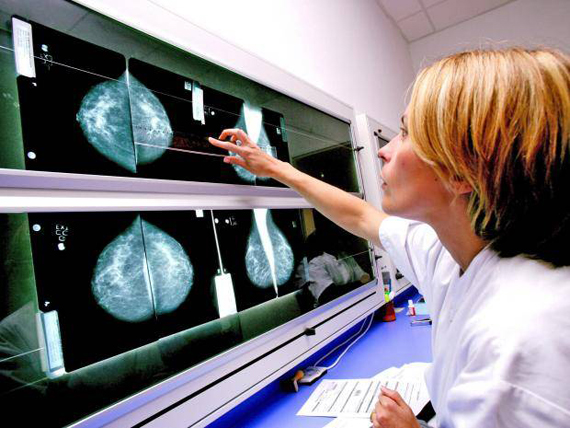
Метастазы в головной мозг – серьезное осложнение опухолевого процесса, которое отмечается у 12–20% онкологических больных. В структуре метастатического поражения головного мозга первое место занимает рак легкого (48%), далее следуют рак молочной железы (15%), меланома (9%), рак толстой кишки (5%), рак почки (4%). Метастазы в мозг сарком, семином и других опухолей бывают реже (Alfred Yung W.K., 2003 г.).
По числу больных, у которых выявлены метастазы в головной мозг, рак легкого (РЛ) у мужчин и рак молочной железы (РМЖ) у женщин занимают ведущее место (7, 17). Метастазы в головной мозг обнаруживаются на аутопсии у 25% больных, умерших от злокачественных новообразований. Прижизненно поражение головного мозга диагностируется примерно в 1,5–3 раза реже по сравнению с находками на вскрытии (7, 8, 23).
Обычно метастазы в мозг развиваются в течение от 6 месяцев до 2 лет после выявления первичной опухоли и ассоциируются с прогрессированием болезни. Метастазы в мозг могут проявляться в любое время заболевания раком, чаще возникают метахронно, но могут проявляться синхронно или даже до выявления первичной опухоли. Внутримозговые метастазы в 10–22% могут быть первым проявлением заболевания либо обнаруживаться во время лечения. Однако в наибольшей степени сроки их выявления зависят от биологических особенностей первичной опухоли. Так, при мелкоклеточном раке легкого (МРЛ) метастазы в головном мозге обнаруживаются в большинстве случаев (50–80%) в течение первого–второго года заболевания, а при РМЖ – в более отдаленные сроки – от 3–4 до 15 лет и более (8, 13, 19). По данным некоторых исследований неблагоприятным прогностическим фактором для больных раком молочной железы, указывающим на повышенный риск метастазирования в головной мозг, является гиперэкспрессия HER2/neu в первичной опухоли (11, 16, 17).
В последние годы отмечается рост числа больных с метастазами в головной мозг. При этом увеличение частоты клинически проявляемых метастазов связано как с совершенствованием диагностики за счет внедрения в клиническую практику рентгеновской компьютерной (РКТ) и магнитно-резонансной томографии (МРТ), так и с увеличением продолжительности ремиссий вследствие использования более эффективных современных программ лечения.
Метастазы в мозг всегда гематогенные, они продуцируют и секретируют ангиогенные субстанции, что делает их васкуляризируемыми и позволяет опухолевым клеткам легче проникать через гематоэнцефалический барьер (ГЭБ). Симптомы метастатического поражения головного мозга обычно развиваются в течение нескольких недель и зависят от размеров, числа и локализации метастазов.
Ранее считалось, что только жирорастворимые препараты могут проникать в головной мозг, однако в исследовании Vick с соавт. (1977 г.) было показано, что функция ГЭБ сильно различается при наличии поражения головного мозга по сравнению с нормальным, и он перестает выполнять «барьерную» функцию в присутствии опухоли.
Hasagawa с соавт. (1979 г.) отметили, что жирорастворимость не является обязательным условием проникновения препарата в ткани мозга и, что водорастворимые лекарственные вещества, такие как метотрексат, циклофосфан и цисплатин способны проникать в опухолевые клетки после их парентерального введения.
В настоящее время считается, что ГЭБ играет важную роль у больных с метастазами в мозг, но его защитные свойства ограничены нормальной тканью мозга, а не самим метастазом. Приводятся данные о том, что нарушение функции ГЭБ наступает уже при размерах метастаза около 1 мм (1, 21, 23).
На основании полученных результатов лечения метастатических опухолей головного мозга определены факторы, при которых лекарственное лечение может быть эффективным. Прежде всего это чувствительность первичной опухоли к системной химиотерапии (наилучшие результаты получены у больных МРЛ и РМЖ); супратенториальное расположение метастазов (лечение метастазов в задней черепной ямки оказалось менее эффективным по сравнению с другими областями мозга); множественные мелкоочаговые метастазы. Благоприятными признаками также являются отсутствие других отдаленных метастазов и длительный интервал между диагностикой первичной опухоли и метастазами в мозг (больные с более коротким интервалом имеют худший прогноз).
Выбор метода лечения (операция, лучевая терапия, химиотерапия) зависит от распространенности опухолевого процесса, морфологической характеристики опухоли, возраста больных и общего состояния.
По данным различных исследований, медиана продолжительности жизни больных с метастазами в мозг составляет без лечения 1-2 месяца, у получающих кортикостероиды – 2-3 месяца, у получавших лучевую терапию (ЛТ) – 3-6 месяцев, у подвергнутых оперативному лечению и последующему облучению мозга – 10-16 месяцев, у получающих химиотерапию (при чувствительных к химиотерапии нозологических формах) – 8-12 месяцев (Wen P.Y. et al., 2001 г.).
В отделении химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России в течение длительного периода времени проводятся исследования по изучению эффективности различных схем химиотерапии у больных с метастатическим поражением головного мозга.
Схема AVP впервые разработана в отделении химиотерапии, где проводилось изучение её эффективности при метастазах в головной мозг МРЛ (2, 3, 4, 6, 10, 12).
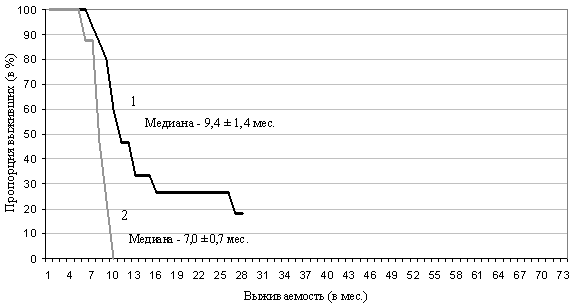
Медиана продолжительности жизни больных с объективным эффектом составила 9,4±1,4 месяцев по сравнению с 7,0±0,7 месяцев у пациентов со стабилизацией или прогрессированием метастазов в головном мозге. Около 40% больных прожили год и 27% – два года в группе AVP при достижении объективного эффекта со стороны внутримозговых метастазов; и все больные при отсутствии эффекта прожили менее 10 месяцев (рис. 1).
При сравнении AVP и других схем (CAV, AC и др.) отмечались достоверно лучшие показатели как по полным (52,0% и 12%), так и по объективным ответам в головном мозге (62,3% и 24%) при использовании AVP (p=0,0035 и 0,0067, соответственно).
В отделении химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России в настоящее время проводится изучение других режимов химиотерапии при метастазах МРЛ в головной мозг.
Так, продолжается изучение комбинации ArDV (араноза + доксорубицин + винкристин) во 2-й линии лечения больных распространенным МРЛ. Лечение проводится по схеме: араноза 1000 мг в/в в 1 и 2 дни, доксорубицин 40 мг/м² в/в в 1-й день, винкристин 2 мг в/в в 1-й день 21-дневного цикла. При использовании данного режима химиотерапии у 10 больных МРЛ с метастазами в головной мозг, получавших ранее химиотерапию, у 3-х пациентов достигнута полная регрессия в мозге, у 1 – частичная регрессия.
Таблица 1.
Эффективность режима ArDV (араноза + доксорубицин + винкристин) во II линии химиотерапии больных МРЛ с метастазами в головной мозг (данные отделения химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России).
| Количество больных | Полная регрессия | Частичная регрессия | Стабилизация | Прогрессирование |
|---|---|---|---|---|
| 10(100%) | 3(30%) | 1(10%) | 4(40%) | 2(20%) |
В отделении химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России продолжается изучение комбинированной химиотерапии по схеме: кампто 60 мг/м² внутривенно в 1, 8 дни + цисплатин 80 мг/м² внутривенно в 1 день у больных распространенной формой МРЛ в качестве I линии лечения. При оценке эффекта химиотерапии метастазов в головной мозг (по данным РКТ головного мозга с внутривенным контрастированием) у 3 из 10 больных (30%) зарегистрирована частичная регрессия опухоли, у 2 (20%) – полная регрессия метастазов в мозг (9).
В последние годы в мире проводится ряд клинических исследований по изучению эффективности новых схем химиотерапии у больных немелкоклеточным раком легкого (НМРЛ) с метастатическим поражением головного мозга.
Quadvlieg V. c соавт. (2004 г.) показали высокую эффективность схемы химиотерапии: гемцитабин 1000 мг/м² внутривенно в 1 и 8 дни + цисплатин 50 мг/м² внутривенно в 1 и 8 дни (20). Курсы химиотерапии проводились каждые 3-4 недели. В целом, при лечении были достигнуты 9 полных регрессий в головном мозге (25%) и 14 частичных регрессий (39%). Таким образом, общий эффект составил 64% (23 из 36 больных). Медиана продолжительности эффекта составила 6,8 мес.
В настоящее время проводятся исследования по изучению эффективности темодала при метастазах в головной мозг в монохимиотерапии, в сочетании с лучевой терапией, а также в составе лекарственных комбинаций (15).
Таблица 2.
Темодал при метастазах злокачественных опухолей в мозг (данные отделения химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России).
| Количество больных | Полная регрессия | Частичная регрессия | Стабилизация | Прогрессирование | |
|---|---|---|---|---|---|
| НМРЛ | 7 | — | — | 3 | 4 |
| РМЖ | 1 | — | — | — | 1 |
| Меланома | 3 | 1 | — | — | 2 |
| Всего | 11 (100%) | 1 (9%) | — | 3 (27%) | 7 (64%) |
Предварительные исследования показывают, что темодал в сочетании с ЛТ увеличивает эффективность лечения метастазов в головной мозг у больных с солидными опухолями на 20-30% в сравнении с одной ЛТ (5).Данные мультицентрового исследования выживаемости больных с метастазами НМРЛ в мозг, получавших лечение темодалом в комбинации с ЛТ по сравнению с одной ЛТ показаны в таблице 3.
Таблица 3.
Выживаемость больных с метастазами НМРЛ в мозг, получавших лечение темодалом в комбинации с лучевой ЛТ по сравнению с ЛТ в самостоятельном варианте.
| Число больных | Объективный ответ | Медиана продолжительности жизни | |
|---|---|---|---|
| Темодал + ЛТ | 52 | 48% (p=0.031) | 7,9 мес. (p=0.06) |
| ЛТ | 51 | 27,5% | 4,3 мес. |
| Всего: | 103 | — | — |
Таблица 4.
Темодал + лучевая терапия у больных с метастазами в головной мозг (данные ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России).
| Число больных | Полная регрессия | Частичная регрессия | Стабилизация | Прогрессирование | |
|---|---|---|---|---|---|
| МРЛ | 2 | 1 | 1 | — | — |
| НМРЛ | 10 | 2 | 5 | 3 | — |
| РМЖ | 5 | 1 | 3 | 1 | — |
| Меланома | 4 | 1 | — | 2 | 1 |
| Всего | 21 (100%) | 5 (23,8%) | 9 (42,8%) | 6(28,6%) | 1 (4,8%) |
В настоящее время продолжаются исследования по изучению сочетания новых противоопухолевых препаратов (кампто, топотекан) с ЛТ при лечении больных с метастатическим поражением мозга.
В последние годы проводятся исследования по изучению эффективности таргетных препаратов у больных с метастазами в головной мозг. Как показали предклинические исследования, отмечается гиперэкспрессия рецепторов эпидермального фактора роста в опухолевой ткани при метастатическом поражении головного мозга и первичных опухолях мозга.
Основываясь на этих данных, Giovanni L.С. с соавт. (2004 г.) изучали эффективность препарата ZD1839 (иресса) у больных НМРЛ с метастазами в головной мозг. В исследование были включены 35 больных НМРЛ (26 мужчин и 9 женщин). 28 больных ранее получали цисплатин-содержащие схемы химиотерапии, 16 проводилась ЛТ на область головного мозга. Схема лечения: иресса 250 мг/сутки внутрь, до прогрессирования болезни. У 5 (17%) больных была достигнута частичная регрессия, у 7 – стабилизация (24%). Таким образом, контроль роста опухоли был отмечен у 12 (41%) пациентов. Результаты данного исследования показывают, что Иресса эффективна у больных с метастазами НМРЛ в головной мозг, получавших ранее лечение (химио- и лучевую терапию).
1. Бредбери М. Концепция гематоэнцефалического барьера. М., «Медицина», 1983, с. 480.
2. Бычков М.Б., Горбунова В.А., Орел Н.Ф., Егоров Г.Н., Насхлеташвили Д.Р. Лекарственная терапия метастазов в головной мозг. Вестник Московского Онкологического Общества, 2004 г., №1 (504).
4. Бычков М.Б., Орел Н.Ф., Насхлеташвили Д.Р. Современные возможности лекарственного лечения мелкоклеточного рака легкого. В кн.: Этюды химиотерапии. М., 2000, с. 70–74.
6. Горбунова В.А., Бычков М.Б., Михина З.П., Войнаревич А.О., Насхлеташвили Д.Р. Химиотерапия больных раком молочной железы с метастазами в головной мозг. Материалы III съезда онкологов и радиологов СНГ 25-28.05.2004 г., часть II, стр. 256-257.
7. Идрисова М.И. Поражение головного мозга при раке легкого. Дисс. канд. мед. наук, М., 1980, 212 стр.
8. Моисеенко В.М., Семиглазов В.Ф., Тюляндин С.А. Современное лекарственное лечение местно-распространенного и метастатического рака молочной железы. «Грифон», Санкт-Петербург, 1997, с. 254.
9. Насхлеташвили Д. Р. Кампто (Иринотекан) в лечении первичных и метастатических опухолей головного мозга. Журнал “Врач”, 2005 г., №12, стр. 67-69.
10. Орел Н.Ф. Новые производные нитрозомочевины. В книге.: Новые цитостатики в лечении злокачественных опухолей, М., 1998, с. 25–39.
11. Altaha R., Crowell E., Ducatman B., Higa G., Abraham J.; West Virginia University, Morgantown, WV. Risk of brain metastases in HER2/neu-positive breast cancer. Journal of Clinical Oncology, 2004 ASCO Annual Meeting Proceedings (Post-Meeting Edition). Vol 22, No 14S (July 15 Supplement), 2004: 682.
12. Bychkov M.B. Gorbounova V.A,. Marenich A.F, Voinarevich A.O. D.R. Naskhletashvili Combined chemotherapy with AVP (Nidran + Vepesid + Cisplatin) in patients with extensive lung cancer. – Lung cancer. Vol. 29, Supplement 1, 2000, p. 37-38.
13. Fisher B., Osborne C.K., Margolese R.G. Bloomer W.D. Neoplasms of the breast. In: Cancer medicine, vol. 2, 4th ed. Holland J.F., Bast R.C. Morton D.L., Frei III E., Kufe D.W., Weichselbaum R.R. Williams & Wilkins. Baltimore, Philadelphia, London, Paris, Bangkok, Buenos Aires, Hong Kong, Munich, Sydney, Tokyo, Wroclaw, 1997, p. 2349–2429.
14. French L.A., Galicich J.H. The use of steroid for control of cerebral edema. Clin. Neurosurg., 1964, 10, p. 212–223.
15. Gorbounova V.A., Bychkov M.B., Michina Z.P., Naskhletashvili D.R., Tеmozolomide in patients with brain metastases. 16th International Congress of Anti-Cancer Treatment (01-04/02/2005 г., Paris, France). Abstract book, p. 306.
16. Heimberger, et al. Cl. Cancer Res., 2002; 8: 3496-3502.
17. Herrero A., Grandez R., Puertolas T., Alonso Orduna V., Martinez Trufero J., Pazo Cid R., Artal A., Lao J., Ruiz de Lobera A., Anton Torres A.; Hospital Miguel Servet, Zaragoza, Spain. High incidence of brain metastases at the time of death in women with metastatic breast cancer treated with trastuzumab. Journal of Clinical Oncology, 2004 ASCO Annual Meeting Proceedings (Post-Meeting Edition). Vol 22, No 14S (July 15 Supplement), 2004: 765.
18. Lai R.K., Dang C., Thaler H., Malkin M.G. The incidence of brain metastases in HER2/neu+ stage IV breast cancer patients. ASCO, 2001, abstract 2014.
19. Nieder C., Niewald M., Hagen T. Brain metastases of bronchial and breast carcinoma. Differences in metastatic behavior and prognosis. Radiologie, 1995, 35, 11, p. 816–821.
20. V. Quadvlieg, L. Bosquee, M. Gustin, N. Barthelemy; CHU LIEGE, LIEGE, Belgium; CHR Citadelle LIEGE, LIEGE, Belgium. Frontline gemcitabine and cisplatin based chemotherapy in patients with NSCLC inoperable brain metastases. Journal of Clinical Oncology, 2004 ASCO Annual Meeting Proceedings (Post-Meeting Edition). Vol 22, No 14S (July 15 Supplement), 2004: 7117.
21. Qin D., Ma J., Xiao J., Tang Z. Effect of brain irradiation on blood-CSF barrier permeability of chemotherapeutic agents. Am. J. Clin. Oncol. Cancer Clin. Trials., 1997, 20, 3, p. 263–265.
22. Vecht C.J. Clinical management of brain metastasis. J. Neurol, 1998, 245, 3, p. 127–131.
Мифы и правда о химиотерапии
Миф 1: химиотерапия малоэффективна
В поддержку этого мнения ссылаются на цитируемое в интернете исследование профессора Гарвардского университета Джона Кэрнса, якобы опубликованное в «Scientific American» и в «Журнале клинической онкологии» в 2004 году, о том, что на самом деле химиотерапия помогает лишь 2,3-5% случаев (комментарий об источнике см. в конце нашего материала). Зато именно «химия» вызывает «сопротивление опухоли, которое выражается в метастазах».
Чтобы говорить об эффективности химиотерапии «при раке», надо уточнить, что понятие «онкология» включает в себя множество разных заболеваний.
Есть нейробластома у детей или хорионкарцинома матки. Их можно полностью излечить именно с помощью химиотерапии. Излечение означает, что у человека нет рецидивов в течении 5 лет.
Есть опухоли, высокочувствительные к химиотерапии – саркома Юинга, рак предстательной железы, рак мочевого пузыря. С помощью химиотерапии они поддаются контролю — возможно излечение, как минимум, можно добиться длительной ремиссии.
Есть промежуточная группа – рак желудка, рак почки, остеогенная саркома, при которых уменьшение опухоли от химиотерапии происходит в 75-50% случаев.
А есть рак печени, поджелудочной железы. Эти опухоли малочувительны к лекарственной терапии, но к ним сейчас применяют другие методы лечения – оперируют или облучают. И еще есть рак крови – понятие, которым пациенты называют острые лейкозы и лимфомы. Они вообще развиваются по другим законам.
Даже при запущенной стадии рака с метастазами, прогноз очень сильно зависит от того, какой у вас конкретно подтип опухоли. Например, гормоночувствительный подтип рака молочной железы даже с метастазами контролю поддается очень хорошо. Поэтому делать какие-то выводы о «химиотерапии при раке в целом» — некорректно.
В последнее время подход к лечению онкологических пациентов всё больше индивидуализируется. Совсем давно говорили: «У вас рак – какой ужас!», — потом: «У вас рак определенного органа – это плохо». А сейчас врач внимательно посмотрит на «паспорт» опухоли из гистохимических и иммунногенетических маркеров и характеристики опухоли, которую пациенту выдали при гистологическом исследовании (такое изучение опухоли теперь входит в стандарты обследования) и в зависимости от этого выберет тактику лечения.
Я не нашла подтверждающей информации, что врачи с такими именами (они есть, но они не онкологи) высказали такое мнение.
Сегодня Россия, как Европа и США, переходит к стандартам доказательной медицины. В этой системе все доказательства оцениваются по определенной шкале. И меньше всего доверия — аргументам из серии «профессор Иванов (или профессор Смит) сказал». Более серьезный уровень аргументов – метаанализы, то есть объединение нескольких, уже проведенных маленьких исследований в одно, когда их результаты складывают и считают вместе.
Химиотерапия – это лечение. И, как у всякого лечения, у нее бывают побочные эффекты. Они бывают от любых лекарств, они бывают после хирургических операций. Сама химиотерапия тоже бывает разной в зависимости от цели. Предоперационную химиотерапию применяют до хирургической операции, чтобы максимально уменьшить размер опухоли и сделать хирургическое вмешательство максимально щадящим.
Цель постоперационной «химии» – убрать отдельные опухолевые клетки, которые еще могут циркулировать в организме.
А бывает химиотерапия паллиативная. Ее применяют, когда опухоль запущена, со множественными метастазами, и вылечить больного невозможно, но возможно затормозить дальнейшее прогрессирование и попытаться контролировать опухоль. В этом случае химиотерапия призвана подарить пациенту время, но, как правило, она сопровождает его до конца. И тогда может создаться впечатление, что пациент умер не от рака, а от «химии», хотя это не так.
Кроме того, при предоперационной или послеоперационной «химии» часто врачи наблюдают пациента не только в тот момент, когда он получает капельницы с препаратами, но и между курсами. Поэтому смертельные случаи от побочных эффектов редки.
Миф 3: химиотерапия непоправимо «сажает» печень, кровь, нервы
Главный механизм действия химиопрепаратов – воздействие на механизм деления клетки. Клетки раковых опухолей очень быстро делятся, поэтому, воздействуя на деление клеток, мы останавливаем рост опухоли.
Но, помимо опухоли, в организме много других быстро делящихся клеток. Они есть во всех системах, которые активно обновляются, — в крови, в слизистых. Те химиопрепараты, которые воздействуют не выборочно, действуют и на эти клетки.
Основные осложнения химиотерапии:
— падение показателей крови
— поражения печени
— изъязвление слизистых и связанные с этим тошнота и понос
— выпадение и ломкость ногтей.Такой эффект объясняется тем, что цитостатическая химиотерапия действует не только на клетки опухоли, но на все быстроделящиеся клетки организма.Также у отдельных препаратов, которые оказывают на организм токсичное действие, бывают специфические осложнения. (Часть препаратов химиотерапии сделана на основе платины – это тяжелый металл).
Токсичные препараты химиотерапии могут вызвать ряд неврологических симптомов – головные боли, бессонницу или сонливость, тошноту, депрессию, спутанность сознания. Иногда возникает ощущение онемения конечностей, «мурашки». Эти симптомы проходят после прекращения действия препарата.
После химиотерапии у пациента ожидаемо падают показатели крови. Обычно пик падения приходится на седьмой-четырнадцатый день, потому что «химия» как раз подействовала на все клетки, которые были в периферической крови, а новые костный мозг выработать еще не успел. Падение происходит в зависимости от препарата, который применялся; одни из них действует преимущественно на тромбоциты, другие – на лейкоциты и нейтрофилы, третьи – на эритроциты и гемоглобин.
Химиотерапевтическое лечение проходит циклами. В зависимости от схемы химиотерапии, человек может получить, например, три дня капельниц химиотерапии, а следующие будут через 21 день. Этот промежуток называется «один цикл», он дается специально, чтобы организм пациента восстановился.
Перед каждым новым сеансом химиотерапии состояние пациента контролируют, смотрят, что было с ним в этот промежуток – делают клинический и биохимический анализ крови. Пока человек не восстановился, новый цикл лечения не начинается.
Если кроме снижения показателей крови до определенного уровня в промежуток между «химиями» ничего плохого не происходило — кровь восстановится сама. Чрезмерное падение тромбоцитов создает угрозу кровотечения, пациенту с такими показателями делают переливание тромбоцитарной массы. Если упали лейкоциты, которые отвечают за иммунитет, а человек заразился какой-то инфекцией, начался кашель, насморк, поднялась температура, — сразу назначают антибиотики, чтобы инфекция не распространилась. Обычно все эти процедуры делаются амбулаторно.
В перерывах между курсами химиотерапии пациента ведет онколог из районного онкодиспансера или поликлиники.
Перед самым первым циклом химиотерапии пациенту должны объяснить все возможные осложнения, рассказать про каждый препарат и его воздействие; и пациент может проконсультироваться со своим онкологом. Взвешивание рисков – отправная точка химиотерапии. Врач и пациент выбирают между повреждением, которое может принести химиотерапия, и преимуществом, которое может за ней последовать, — а именно – продление жизни порой на десятки лет.
Это – ключевой момент в принятии решения о необходимости применения химиопрепаратов: если мы понимаем, что при назначении того или иного лекарства процент успеха будет ниже, чем побочные эффекты, применять его просто нет смысла.
Миф 4: метастазы вырастают из «стволовых клеток рака», которые «химия» все равно не убивает
Причины возникновения метастазов у разных опухолей очень разные, как именно возникают метастазы, мы пока не знаем. Единственное, что мы знаем – «стволовых клеток рака» не бывает.
Опухоль в разных своих фрагментах и клетки метастазов – это очень неоднородное образование, там все клетки разные, они быстро делятся и быстро мутируют. Но в любом случае химиотерапия воздействует на все метастазы, где бы они ни были. Исключение – метастазы в головном мозге, куда проникают не все препараты. В этих случаях назначают особое лечение, либо особое введение препаратов – в спинномозговой канал. Бывают даже такие опухоли, у которых нельзя найти первичный очаг, — то есть, все, что мы видим в организме – это метастазы. Но лечение все равно назначают, и оно, во многих случаях, успешно проводится.
Миф 5: химиотерапия – метод, поддерживаемый фарминдустрией
Якобы давно есть препараты эффективнее, безвреднее и дешевле, но о них не говорят, боятся обвалить фармрынок.
Этот миф существует и по поводу других заболеваний, особенно это касается ВИЧ.
«Альтернативные препараты», которые принимают онкологические пациенты, в лучшем случае оказываются безобидными травками, от которых нет заметного действия. Увы, бывает хуже. Например, иногда пациенты начинают пить чудодейственные лекарства на основе смеси разных масел, а ведь масло – это очень тяжелый продукт для печени. В итоге пациент буквально вызывает у себя воспаление печени, и мы не можем начать цикл химиотерапии, потому что «химия» на печень тоже воздействует. И хорошо, если пациент хотя бы рассказывает нам, что он принимал, и мы можем понять, что так ухудшило ситуацию. Но лечение в итоге откладывается, эффективность его понижается. Кроме того, ряд новых лекарств для лечения, например, рака молочной железы, сейчас основан на растительных компонентах. Например, препарат трабектедин содержит специальным образом обработанную вытяжку из морских тюльпанов. Так что иногда препараты, которые пациенты принимают в ходе официального лечения, сами по себе – «природные».
Что до «гигантских денег фарминдустрии», часть препаратов химиотерапии, например, метотрексат, — это очень старые, давно разработанные лекарства, они стоят буквально копейки. Никаким «обвалом» или «подъемом отрасли» уменьшение или увеличение их производства не грозит.
В любом случае препараты для лечения онкологических заболеваний пациенты в России получают бесплатно.
Новые лекарства при раке
В последнее время в дополнение к цитостатикам – препаратам химиотерапии, которые действовали на весь организм целиком, появились новые препараты. Это – новое поколение препаратов химиотерапии – таргетные препараты и лекарства, основанные на принципиально ином принципе действия – иммунопрепараты.
Таргетный препарат – это лекарство, воздействующее не на весь организм, а адресно на клетки опухоли. При этом важно – молекулы конкретного таргетного препарата могут присоединиться к рецепторам клетки только определенного вида опухоли. Конкретный подтип опухоли определяется генетическим анализом во время молекулярно-генетического исследования.
Иммунопрепараты воздействуют на иммунную систему организма и иммунные механизмы опухоли в её ядре. В результате в организме активизируется собственный иммунитет, который начинает бороться с раковыми клетками.
Сравнительно новый метод — гормонотерапия, но здесь круг показаний еще уже – опухоль должна быть гормоночувствительная. Считается, что на гормонотерапию лучше всего реагируют опухоли молочной железы и предстательной железы, хотя и здесь гормоны можно использовать только при определенных показаниях.
Кстати, с гормонотерапией связан еще один миф: чаще всего она используется в форме таблеток, и пациенты считают, что таблетки – это «не лечение» при такой болезни, как рак.
Можно ли обойтись без химиотерапии
Катерина Коробейникова. Фото: Ольга Молостова
Без химиотерапии, одними гормонами иногда лечат, например, рак молочной железы. Хотя понятно, что гормоны тоже небезобидны, от них бывают свои осложнения.
Вместе с тем надо понимать: мы изобретаем новые препараты, но и раковые клетки мутируют и к ним приспосабливаются. Даже у пациента, которому раньше лечение без «химии» помогало, опухоль может спрогрессировать и стать нечувствительной к лекарствам, которые сдерживали ее рост. В этом случае химиотерапия применяется как экстренное лечение.
Например, пациентка с раком молочной железы долгое время принимает гормоны, и опухоль не растет. Внезапно она чувствует слабость, появляются метастазы в печени. В этом случае мы проводим несколько циклов химиотерапии, возвращаем организм в состояние, когда опухоль вновь начинает реагировать на гормоны, и тогда пациентка возвращается к прежней схеме лечения.
Совсем без химиотерапии на нынешнем уровне развития онкологии мы не обойдемся. Но при этом развивается «сопроводительное лечение» — вместе с химиотерапией пациент получает целый набор лекарств, ослабляющих тошноту, ускоряющих восстановление клеток крови и нормализующих стул. Так что неприятные побочные эффекты химиотерапии удается значительно ослабить.
Сомнительный источник
Об исследовании «профессора Гарвардского университета Джона Кэрнса», которое озвучивает миф 1: химия малоэффективна, я слышу впервые. Единственный практикующий врач по имени Джон Кернс, которого удалось найти в интернете, — это невролог-радиолог, который занимается проблемами головного мозга, а про химиотерапию вообще ничего не писал.Возможно, речь идет о британском враче Джоне Кернсе (John Cairns), с 1991 года на покое – он 1923 года рождения. Кернс — автор книг «Рак: Наука и Общество» (1978) и «Вопросы жизни и смерти: взгляды на здравоохранение, молекулярную биологию, рак и перспективы человеческого рода» (1997). Годы работы Джона Кернса говорят о том, что он ссылался на статистику выживаемости 1970-1980-х годов, и публиковаться в научных журналах в начале 2000-х не мог.Если речь идет об этом Джоне Кернсе, то мы можем говорить лишь об устаревших исследованиях в онкологии: с 1970-х годов эффективность лекарств сильно изменилась.«Журнал клинической онкологии» в число современных авторитетных изданий не входит.