впр головного мозга это
Типичные поражения нервной системы плода: корреляция между МРТ и данными УЗИ
Авторы: Heron Werner, Taisa Davaus Gasparetto, Pedro Daltro, Emerson Leandro Gasparetto, Edward Araujo Júnior
Вступление
Оценка состояния плода улучшилась за эти годы благодаря развитию инструментальных методов диагностики. Столкнувшись с более сложными диагнозами, МРТ стала широко использоваться в качестве дополнения к пренатальному УЗИ.
Поскольку показания к МРТ головного мозга плода в основном основаны на, вызывающих подозрение, результатах УЗИ, МРТ плода обычно проводится во второй половине беременности, от 18 до 20 недель.
Наиболее распространенные показания для визуализации головного мозга плода кратко обсуждаются ниже и включают анэнцефалию, вентрикуломегалию, агенезию мозолистого тела, голопрозэнцефалию, гидранэнцефалию, микроцефалию, порок Киари, инэнцефалию, порок развития Денди-Уокера и другие.
Дефекты мозга и ЦНС
Анэнцефалия
Анэнцефалия относится к дефектам заращения передней нервной трубки, с общей частотой приблизительно 1 на 1000 рождений и летальным прогнозом. Анэнцефалия характеризуется отсутствием свода черепа, что приводит к обнажению нервной ткани. Ранний диагноз может быть легко поставлен с помощью УЗИ в первом триместре (Рис. 1).
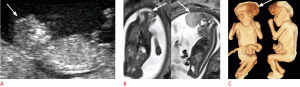
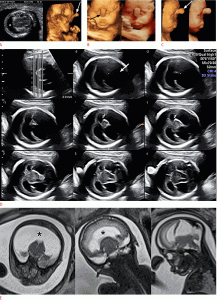
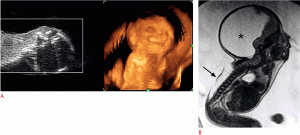
Рисунок 1: Плод в 13 недель с экзэнцефалией.
А . Сагиттальное УЗИ показывает плоскую головку (стрелка). B, C . Корональные (слева) и сагиттальные (справа) T2-взвешенные изображения (B) и 3-мерные изображения реконструкции магнитно-резонансной томографии показывают дисморфную мозговую ткань в амниотической полости (стрелки).
Вентрикуломегалия
Вентрикуломегалия является одним из наиболее частых патологических изменений головного мозга. Она связана с дисбалансом между продукцией и реабсорбцией спинномозговой жидкости, что приводит к избытку последней. В результате боковые желудочки могут демонстрировать различные степени увеличения, которые могут быть или не быть связаны с дилатацией третьего и четвертого желудочков. Термин вентрикуломегалия используется только тогда, когда ширина одного или обоих желудочков, измеренная на уровне гломуса, составляет ≥10 мм на любой стадии беременности.
В случаях обнаружения при УЗИ вентрикуломегалии, МРТ полезна для оценки паренхимы головного мозга, а также для оценки связанных пороков развития (Рис. 2).
Связи с другими аномалиями встречаются примерно в 70-85% случаев, включая миеломенингоцеле (30%) и травмы головного мозга, такие как агенезия мозолистого тела, пороки развития коры, перивентрикулярная гетеротопия, пороки развития мозжечка, перивентрикулярное повреждение белого вещества и др. Кроме того, могут наблюдаться дефекты, затрагивающие сердце, грудную клетку, почки, брюшную стенку, лицо и конечности. Тем не менее, в некоторых случаях вентрикуломегалия является единственной патологической находкой, которая называется изолированной вентрикуломегалией. В таких случаях риск развития анеуплоидии может быть выше, и необходим более конкретный анализ (Рис. 3).
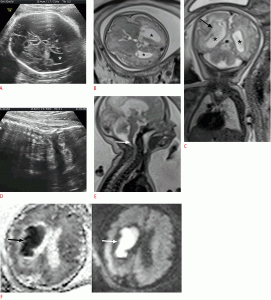
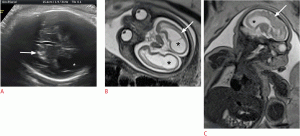
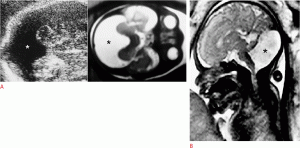
Рисунок 2: Плод с дилатацией левого желудочка в 35 недель.
А-С . Осевое УЗИ (A), аксиальная T2-взвешенная (B) и корональная T2-взвешенная (C) магнитно-резонансная томограммы показывают дилатацию левого желудочка (звездочки). В левом полушарии, близко к левому желудочку присутствует гетерогенный сигнал (C, стрелка). E . Сагиттальный T2-взвешенный снимок показывает сужение ствола мозга (стрелка). F . Взвешенное по аксиальной диффузии изображение (слева) и соответствующая карта видимых коэффициентов диффузии (справа) показывают гематому вблизи левого желудочка (стрелки).
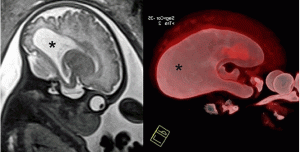
Рисунок 3: Плод с вентрикуломегалией в 34 недели.
Сагиттальные Т2-взвешенные (слева) и 3-мерные реконструкции (справа) изображения демонстрируют увеличенный задний рог в боковых желудочках (звездочки).
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Скачайте руководство по уходу прямо сейчас
Агенезия мозолистого тела
Мозолистое тело – важная комиссура, соединяющая полушария головного мозга. Оно формируется от передней к задней комиссуры, за исключением рострума. Агенезия мозолистого тела может быть диагностирована с помощью УЗИ. Диагноз может быть подтвержден на основании косвенных признаков, таких как параллельность боковых желудочков, подъем третьего желудочка, дилатация затылочного рога боковых желудочков, отсутствие извилин и наличие комиссуры Пробста, которая не достигает контралатерального полушария и впоследствии изгибает, вызывая вмятины на передне-медиальной стенке лобного рога (Рис. 4). МРТ плода также может выявить другие аномалии данной системы, включая частичный агенез, дисгенез и гипоплазию. Кроме того, часто встречаются ассоциированные пороки развития с участием супратенториальных и инфратенториальных структур (в 80% случаев), и могут возникать связанные аномалии вне ЦНС, включая врожденные пороки сердца, скелетные дефекты и дефекты мочеполовой системы (в 60% случаев)
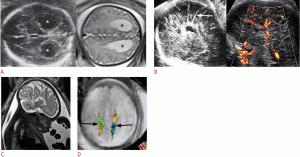
Рисунок 4: Плод с агенезией мозолистого тела в 35 недель.
A . Аксиальное УЗИ (слева) и МРТ (справа) показывают увеличенный задний рог бокового желудочка (звездочки). B . Корональная шкала серого (слева) и силовая допплерография (справа) показывают отсутствие поясной извилины и радиального расположения извилины (стрелка). C . Сагиттальная Т2-взвешенная магнитно-резонансная томография также показывает те же особенности, что и при УЗИ. D . Осевая трактография показывает комиссуры Пробста (стрелки).
Голопрозэнцефалия
Голопрозэнцефалия – это заболевание раннего происхождения, наблюдаемое даже во время органогенеза головного мозга и являющееся результатом нарушения расщепления переднего мозга. В зависимости от степени тяжести она классифицируется как алобарная, полулобарная и долобарная, с конкретными данными визуализации для каждой формы. Заболеваемость составляет примерно 1 на 10000 рождений, а прогноз алобарной и полулобарной форм – неблагоприятный.
Выживание при легких формах обычно связано с умственной отсталостью. Развитие лица связано с формированием мозга; следовательно, могут возникнуть дефекты лица, начиная от легкого гипотелоризма до циклопии. УЗИ – очень эффективный метод диагностики алобарной и полулобарной голопрозэнцефалии.
Рисунок 5: Плод в 11 недель с голопрозэнцефалией алобарной формы.
A . Аксиальное УЗИ (слева) демонстрирует слияние таламуса и желудочков (звездочка), что также показано в режиме трехмерного рендеринга (справа) с хоботком (стрелка). B . На передних изображениях трехмерного УЗИ в режимах рендеринга (слева) и HDLive (справа) лица показан хоботок (стрелка). C . Вид профиля трехмерного УЗИ в режимах рендеринга (слева) и HDLive (справа) плода показывает хоботок (стрелка). D . Серийные изображения 3D УЗИ (режим томографической ультразвуковой визуализации) показывают слияние желудочков (стрелка). Аксиальные (слева), корональные (в центре) и сагиттальные (справа) МРТ изображения, взвешенные по Т2, показывают моновентрикулу (звездочки) и слитые полушария головного мозга.
Гидроанэнцефалия
Рисунок 6: Плод с гидранэнцефалией в 22 недели.
A, B . Осевое УЗИ (A) и 3-мерное УЗИ в режиме рендеринга (B) демонстрируют гидранэнцефалию (звездочки). C . Сагиттальная Т2-взвешенная магнитно-резонансная томография показывает, что паренхима головного мозга образует тонкую полоску с гидранэнцефалией (звездочки).
Микроцефалия
Микроцефалия определяется как значительное уменьшение окружности головы ниже пятого процентиля или на два стандартных отклонения ниже среднего. Обычно она выявляется на 24 неделе, поскольку на этом сроке легче проводить дальнейшую диагностику благодаря контрасту между размером головы и телом плода. Основными причинами являются аутосомно-рецессивные или доминантные расстройства, инфекции (цитомегаловирус, токсоплазмоз, краснуха и вирус Зика), радиация, наркотики, алкоголь и гипоксия.
Рисунок 7: Микроцефалия на 35 неделе после внутриутробной инфекции вирусом Зика.
A . Аксиальное УЗИ показывает паренхиматозные кальцификации (стрелка) и дилатацию бокового желудочка (звездочка). Обратите внимание, что оценка мозга ограничена артефактом затенения окостеневшего черепа. B . Осевая Т2-взвешенная магнитно-резонансная томография показывает гладкую и тонкую кортикальную ленту (стрелка) и увеличенную желудочковую систему (звездочки). C . Сагиттальная Т2-взвешенная магнитно-резонансная томография показывает расширение желудочка (звездочка) и относительную гладкость поверхности мозга, атрофию головного мозга и неоднородную кору (стрелка).
Порок Киари
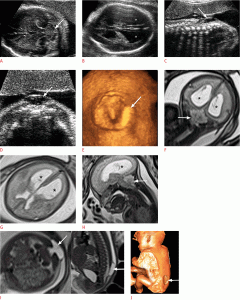
Рисунок 8: Плод с пороком Киари II в 26 недель.
A . Аксиальное УЗИ показывает признак грыжи мозжечка (стрелка). Осевое УЗИ показывает признак двусторонней депрессии лобной части черепа и расширение желудочков (звездочки). C, D . Сагиттальные (C) и аксиальные (D) сонографические изображения демонстрируют менингоцеле (стрелки). E . Менингоцеле (стрелка) следует отметить при 3-мерном УЗИ в режиме рендеринга. F. Корональная Т2-взвешенная магнитно-резонансная томография показывает небольшую заднюю ямку, вентрикуломегалию (звездочки) и облитерацию большой цистерны (стрелка). G . Осевая Т2-взвешенная магнитно-резонансная томография показывает расширение желудочка (звездочки). H. Сагиттальная Т2-взвешенная магнитно-резонансная томография показывает расширение желудочка (звездочка) и грыжу мозжечка (стрелка). I. На аксиальном (слева) и сагиттальном (справа) снимках Т2-взвешенной магнитно-резонансной томографии показано менингоцеле (стрелки). J . Трехмерная реконструкция из магнитно-резонансной томографии показывает менингоцеле (стрелка).
Существует еще одна тяжелая форма мальформации Киари, известная как тип III. Эта форма встречается редко и состоит из энцефалоцеле с грыжей содержимого задней ямки (Рис. 9) и иногда затылочной доли. Грыжа ткани всегда аномальна, с областями некроза, глиоза и фиброза.
Инэнцефалия
Инэнцефалия – это редкий порок развития нервной трубки, возникающий в начале эмбрионального развития плода (около третьей недели). Он характеризуется выраженной ретрофлексией головы из-за дефекта в затылочной области с вовлечением поражения позвонков. Изменения позвонков описываются с точки зрения неспособности визуализировать задние дуги из-за слияния с передним аспектом тела позвонка. Лицо обращено вверх, кожа покрывает области нижней челюсти и грудной клетки. Связанные аномалии присутствуют в 84% пораженных плодов, включая гидроцефалию, порок развития Денди-Уокера, энцефалоцеле, менингоцеле, диафрагмальную грыжу, омфалоцеле и аномалии сердечной и аортальной дуги. Данные, полученные при УЗИ, могут указывать на диагноз, но обычно трудно визуализировать весь позвоночник в продольной плоскости, используя эту методику, и детали мозга плода и спинного мозга могут не наблюдаться удовлетворительно. МРТ может очертить внутричерепные и интраспинальные аномалии более подробно (Рис. 10).
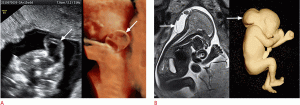
Рисунок 10. Плод с инэнцефалией в 28 недель.
A, B . Сагиттальное УЗИ (слева) и трехмерное УЗИ в режиме рендеринга (справа) (A) и сагиттальная Т2-взвешенная магнитно-резонансная томография (B) демонстрируют короткий шейный отдел позвоночника с выраженной ретрофлексией. Следует отметить гидроцефалию (звездочка) и дизрафизм (стрелка).
Синдром Дэнди-Уокера
Порок развития Денди-Уокера – это аномалия развития задней ямки с частотой 1 на 25 000-35 000 живорождений и небольшим преобладанием у женщин. Он характеризуется полным или частичным агенезом червей мозжечка, кистозной дилатацией четвертого желудочка и расширением задней ямки, с превосходящим смещением тенториума и слиянием венозных пазух. Из-за позднего эмбриологического развития мозжечка диагноз агенезии или частичной агенезии червей не может быть предложен до конца 19-й недели, когда черви мозжечка должны быть полностью развиты. Часто встречаются пороки развития, в том числе агенезия мозолистого тела (25%), липома мозолистого тела, порок развития извилины мозга, голопрозэнцефалия (25%), гетеротопия мозжечка (25%). Кроме того, высока частота кариотипических нарушений, в основном трисомии 18 и 13, а также триплоидии (до 40% случаев).
Рисунок 11. Плод с пороком развития Денди-Уокера в 28 недель.
A . Аксиальное УЗИ (слева) и Т2-взвешенная магнитно-резонансная томография (справа) демонстрируют увеличение задней ямки (звездочки). B . Сагиттальная Т2-взвешенная магнитно-резонансная томография показывает кисту задней ямки (звездочка).
Заключение
Диагноз аномалии головного мозга плода является критическим стрессом для родителей, и эффективное консультирование зависит от точного пренатального диагноза. Кроме того, точный диагноз антенатальных состояний важен не только для ведения затронутой беременности, но также и для будущих беременностей, чтобы помочь в выявлении наследственных заболеваний и предоставить информацию для точного дородового консультирования.
Исследование плода и плаценты при врожденных пороках развития, несовместимых с жизнью
Целью исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к индуцированному прерыванию беременности по медицинским показаниям, структурные изменения в последе при наличии пороков развития. Проведено ран
The aim of the study was to reveal the structure of fatal congenital malformations of the fetus, leading to the induced interruption of pregnancy due to medical indications, structural changes in the afterbirth in the presence of malformations. The randomized comparative study was conducted in 2 stages (retrospective and prospective).
Врожденные пороки развития (ВПР) плода считают важнейшей медицинской и социальной проблемой, поскольку они занимают ведущее место в структуре причин перинатальной, неонатальной и младенческой заболеваемости, смертности и инвалидности [1]. Также актуальной является проблема прерывания беременности в поздние сроки по медицинским показаниям со стороны плода, так как на ее долю приходится около 20% от общего числа абортов, а количество осложнений возрастает в 3–4 раза при прерывании беременности во втором триместре по сравнению с первым [2]. Согласно данным ВОЗ, ВПР отмечают у 4–6% детей. В России ежегодно более 50 000 детей рождаются с ВПР, число пациентов с ВПР превышает 1,5 млн человек. При наличии у плода ВПР, несовместимых с жизнью, или сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, женщине предоставляется информация о возможности искусственного прерывания беременности по медицинским показаниям [3]. При отказе женщины прервать беременность из-за наличия ВПР, несовместимых с жизнью, или иных сочетанных пороков беременность ведется в соответствии с разделом I настоящего порядка. Высокие затраты на лечение, уход и реабилитацию детей с ВПР обусловливают необходимость разработки и совершенствования не только методов контроля, диагностики и профилактики ВПР у детей, но и изучения патоморфологии плода и последа [4].
В последние десятилетия интенсивно изучаются многочисленные антенатальные факторы, приводящие к повреждению нервной системы плода — внутриутробные инфекции, генетические дефекты, проблемы резус-конфликта, воздействие на плод лекарственных веществ и целый ряд других факторов. Нередко причинами врожденных пороков развития плода и последа являются инфекционные причины: инфекционные фетопатии формируются с 16-й недели, когда происходит генерализация инфекции у плода, вследствие чего могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [5].
Большое количество работ посвящено методам прерывания беременности в позднем сроке по медицинским показаниям со стороны плода — врожденным порокам развития плода, реабилитации женщин после элиминации плода [6–11]. В то же время недостаточно описаны результаты патологоанатомического исследования плода и плаценты при врожденных пороках, несовместимых с жизнью. Наше исследование посвящено прерыванию беременности во втором триместре по медицинским показаниям со стороны плода. Данная публикация посвящена вопросам патологоанатомического исследования плода и последа.
Целью данного исследования было выявить структуру врожденных пороков развития плода, несовместимых с жизнью, приведших к прерыванию беременности по медицинским показаниям, их сочетания со структурными изменениями в последе.
Материалы и методы исследования
Исследование одобрено локальным этическим комитетом ФГБОУ ВО ОмГМУ МЗ РФ, Омск (№ 63 от 09.10.2014 г.) и выполнено на базе БУЗОО ГКПЦ, Омск. Прерывание беременности во II триместре по медицинским показаниям проводилось согласно Распоряжению Министерства здравоохранения Омской области № 308-р от 17.09.2013 г. в указанном учреждении, где был создан центр по прерыванию беременности второго триместра и женщине выдавалось заключение перинатального консилиума специалистами (акушер-гинеколог, перинатолог, неонатолог и др.). Гистологическое исследование элиминированных плодов и плацент проведено согласно рекомендациям А. П. Милованова и осуществлялось в патологоанатомическом отделении БУЗОО ОДКБ, Омск.
Основным показанием к прерыванию беременности на всех этапах являлись ВПР плода, несовместимые с жизнью. При наличии у плода ВПР, несовместимого с жизнью, или наличии сочетанных пороков с неблагоприятным прогнозом для жизни и здоровья, при ВПР, приводящих к стойкой потере функций вследствие тяжести и объема поражения при отсутствии методов эффективного лечения, предоставлялась информация о возможности искусственного прерывания беременности по медицинским показаниям. Искусственное прерывание беременности проводилось при наличии информированного добровольного согласия женщины.
На первом ретроспективном этапе (до внедрения в практику регламентирующих документов [3, 12]) проведен анализ гистологического исследования плацент после прерывания беременности у 150 женщин, которые в зависимости от метода прерывания были разделены на две группы: группу А составили 75 женщин, которым проведено прерывание беременности в поздние сроки методом трансвагинального трансцервикального амниоцентеза: амниоинфузия 10% раствором хлорида натрия. Группу Б составили 75 женщин, которым с целью прерывания беременности в поздние сроки для возбуждения и стимуляции родовой деятельности использовали гель динопростон для эндоцервикального введения. Более подробно методы прерывания беременности, их эффективность и исходы описаны в наших предыдущих публикациях [13–15]. Критериями включения пациенток в группы А и Б были следующие: срок беременности 18–21 неделя 6 дней, возможность родоразрешения через естественные родовые пути и отсутствие противопоказаний к применению гипертонического раствора хлорида натрия (10% NaCl) и простагландинов. Пациентки обеих групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Все пациентки были консультированы в медико-генетическом отделе.
На втором этапе под проспективным наблюдением было 195 беременных, разделенных на две группы. Основную группу составили 98 женщин, которым проведено прерывание беременности в поздние сроки следующим комбинированным методом: мифепристон перорально и введение ламинарий в цервикальный канал. В группу сравнения были включены 97 женщин, прерывание беременности которым проводилось по схеме ВОЗ. Критерии включения в группы: пациентки, которым дано заключение консилиума врачей для прерывания беременности по медицинским показаниям со стороны плода в сроки гестации 18–21 неделя согласно приказам МЗСР РФ № 736 от 03 декабря 2007 г. [16] и № 572н от 01.11.2012 [3].
На проспективном этапе исследования материалом для изучения послужили результаты патоморфологического исследования плодов (аутопсийного материала) и последов (макроскопическое и микроскопическое). В работе использованы антропометрические, органометрические, гистологические методы. С целью уточнения гестационного возраста плода и дополнительных скрытых аномалий развития в соответствии с имеющимися стандартами использовали антропометрические и органометрические исследования [17–20]. Гистологические исследования органов плода, плодных оболочек, пуповины и плаценты проводили на парафиновых срезах, изготовленных по общепринятой методике и окрашенных гематоксилином и эозином, а также избирательно пикрофуксином по методу Ван Гизона. Для гистологического исследования предварительно материал фиксировали в 10% нейтральном формалине, после промывки и стандартной проводки заливали в парафин. Парафиновые срезы толщиной 3–5 мкм окрашивали гематоксилином и эозином. Элементы соединительной ткани определяли пикрофуксином по методу Ван-Гизона. Методы гистологического исследования выполнялись по прописям, изложенным в классических руководствах по гистологической технике и гистохимии. Обследование элиминированных плодов включало тщательную визуальную оценку имеющихся стигм эмбриогенеза, врожденных пороков. Для гистологического исследования отбирали фрагменты органов с целью изучения их гистоархитектоники [17].
Использовался способ статистической обработки результатов по критерию t таблиц Стьюдента, позволяющий вычислить степень достоверности различий при небольшом числе наблюдений. Перед каждым вычислением достоверности различий между количественными признаками, а также для выбора критерия корреляции оценивали нормальность их распределения по критерию Колмогорова–Смирнова. В случае ненормального распределения количественных признаков или неравенстве дисперсий применялся U-критерий Манна–Уитни. Для факторов, имеющих биноминальное распределение, дополнительно были рассчитаны 95% доверительные интервалы.
Результаты исследования
Пациентки всех групп были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету. Эффективность прерывания беременности в поздние сроки методом амниоцентеза составила 93,3%, при применении простагландинов — 92%, на проспективном этапе не имела достоверных различий и составила 99,0% в основной группе и 96,9% — в группе сравнения.
В структуре выявленных ВПР плода на первом месте в основной группе были врожденные пороки сердечно-сосудистой системы (34 наблюдения — 34,7%), на втором — пороки центральной нервной системы (ЦНС) (29 наблюдений — 29,6%), на третьем — множественные пороки развития (13–13,3%), на четвертом — пороки мочевыводящей системы (9–9,2%) (табл. 1). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (7–7,1%) и другие (6–6,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие. В группе сравнения на первом месте также были врожденные пороки сердечно-сосудистой системы (32 наблюдения — 33,0%), на втором — пороки ЦНС (30 наблюдений — 30,9%), на третьем — множественные пороки развития (15–15,5%), на четвертом — пороки мочевыводящей системы (10–10,3%). В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата (8–8,2%) и другие (2–2,1%): кожи и мышц, желудочно-кишечного тракта, легких, шеи и лица, прочие.
Среди пороков сердечно-сосудистой системы в обеих группах чаще наблюдались транспозиция магистральных сосудов, дефекты межжелудочковой и межпредсердной перегородок, общий артериовенозный канал, тетрада Фалло, сочетанные пороки сердца, аномалии Эбштейна, гипоплазия левого отдела, прочие врожденные пороки сердечно-сосудистой системы.
В структуре пороков ЦНС чаще наблюдалась гидроцефалия, анэнцефалия, синдром Арнольда–Киари и Денди–Уокера, микроцефалия, агенезия мозолистого тела, акрания, spina bifida (спинномозговая грыжа). Гидроцефалия — заболевание, характеризующееся избыточным накоплением цереброспинальной жидкости в желудочках и подоболочечных пространствах головного мозга, сопровождающееся их расширением и атрофией мозгового вещества.
В ходе ретроспективной оценки исследования последов в группе А в подавляющем большинстве наблюдений (78,7%) определялись серозно-гнойный и гнойно-некротический децидуит и лишь в небольшом проценте случаев (21,3%) наблюдался серозный децидуит. Также в этой группе отмечалось наличие дисциркуляторных нарушений (выраженный отек стромы ворсин, тромбоз межворсинчатого пространства, ретроплацентарные гематомы). В группе Б серозный париетальный децидуит определялся в большинстве случаев (54,7%), воспалительные изменения не определялись в 38,7% наблюдений, серозно-гнойный париетальный децидуит обнаружен в 6,6% случаев.
На ретроспективном этапе при исследовании последа в большей степени были обнаружены патологическое строение и пороки развития пуповины, чем в плаценте. Так, на первом месте среди признаков патологического строения пуповины была тощая пуповина: 19 наблюдений в основной группе (19,4%) и 21 (21,6%) в группе сравнения (табл. 2). На втором месте определялись ложные узлы пуповины: 16 (16,3%) и 17 (17,5%) соответственно исследуемым группам, на третьем месте — истинные узлы пуповины: 14 (14,2%) и 15 (15,5%). Нередко в структуре патологических вариантов строения пуповины было оболочечное прикрепление пуповины: 12 (12,2%) и 9 (9,3%) соответственно. Реже были выявлены гипо- и гиперизвитая пуповина: 8 (8,2%) и 7 (7,2%) соответственно исследуемым группам; единственная артерия пуповины: 6 (6,1%) и 4 (4,1%); гематома пуповины: 1 (1,0%) в основной группе и 2 (2,1%) в группе сравнения. Всего при исследовании нарушения строения пуповины были выявлены в 76 случаях основной группы и в 75 — группы сравнения, в целом в исследовании — в 77,4% наблюдениях.
При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения (23 наблюдения — 23,5% в основной группе и 29–30,0% в группе сравнения). Серозный париетальный децидуит определялся в 17,3% наблюдений основной группы и 16,5% группы сравнения. Такие скудные изменения в плаценте, выявленные при исследовании, свидетельствуют о том, что ВПР плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с нарушениями строения и пороками развития плаценты. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Таким образом, в структуре выявленных ВПР плода, несовместимых с жизнью, в исследуемых группах на первом месте были врожденные пороки сердечно-сосудистой системы, на втором — пороки ЦНС, на третьем — множественные пороки развития, на четвертом — пороки мочевыводящей системы. В остальных наблюдениях выявлены ВПР опорно-двигательного аппарата и другие: желудочно-кишечного тракта, дыхательной системы, шеи и лица, прочие.
При гистологическом исследовании плаценты ретроспективного этапа (до внедрения в акушерскую практику современных методов производства позднего индуцированного аборта) при проведении амниоинфузии гипертоническим раствором в подавляющем большинстве определялись серозно-гнойный и гнойно-некротический мембранит, при применении динопростона чаще наблюдался серозный париетальный децидуит. После внедрения в работу акушерско-гинекологической службы регламентирующего Приказа 572н при гистологическом исследовании плаценты у пациенток второго этапа обеих групп отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения.
При исследовании последа чаще встречались пороки развития пуповины, чем плаценты. На первом месте среди признаков патологического строения пуповины была тощая пуповина, на втором месте — ложные узлы пуповины, на третьем — истинные узлы. Реже определялось оболочечное прикрепление пуповины. Значительно реже были выявлены гипо- и гиперизвитая пуповина, единственная пупочная артерия; гематома пуповины. При гистологическом исследовании плаценты отмечалась относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения. Скудные изменения в плаценте (в сравнении с изменениями в пуповине), выявленные при исследовании, свидетельствуют о том, что врожденные пороки развития плода, несовместимые с жизнью, чаще сочетаются с патологией строения пуповины, чем с плацентарными пороками. Также относительная сохранность амниального эпителия, полнокровие сосудов и незначительные воспалительные изменения указывают на то, что прерывание беременности проводилось современным медикаментозным способом, который имитирует спонтанную сократительную деятельность матки и не вызывает грубых изменений в плаценте.
Литература
* ФГБОУ ВО ОмГМУ МЗ РФ, Омск
** БУЗОО ОДКБ, Омск


_575.gif)