антиноцицептивная система мозга ее основные структуры
Ноцицептивная и антиноцицептивная системы.
Ноцицептивная система восприятия боли. Имеет рецепторный, проводниковый отдел и центральное представительство. Медиатор этой системы – вещество Р.
Антиноцицептивная система – система обезболивания в организме, которое существляется путем воздействия эндорфинов и энкефалинов (опиоидные пептиды) на опиоидные рецепторы различных структур ЦНС: околоводопроводного серого вещества, ядер шва ретикулярной формации среднего мозга, гипоталамуса, таламуса, соматосенсорной зоны коры.
Характеристика ноцицептивной системы.
Периферический отдел болевого анализатора.
Эти высокопороговые рецепторы, реагирующие на раздражающее действие факторов. По механизму возбуждения ноцицепторы делят на механоноцицепторы и хемоноцицепторы.
Механорецепторы расположены преимущественно в коже, фасциях, суставных сумках и слизистых оболочках пищеварительного тракта. Это свободные нервные окончания группы АΔ (дельта; скорость проведения 4 – 30 м/с). Реагируют на деформирующие воздействия, возникающие при растяжении или сжатии тканей. Большинство из них хорошо адаптируются.
Хеморецепторы расположены также на коже и слизистых внутренних органов, в стенках мелких артерий. Представлены свободными нервными окончаниями группы С со скоростью проведения 0,4 – 2 м/с. Реагируют на химические вещества и воздействия, создающие дефицит О2 в тканях нарушающие процесс окисления (т.е. на алгогены).
К таким веществам относятся:
1) тканевые алгогены – серотонин, гистамин, АХ и другие, образуются при разрушении тучных клеток соединительной ткани.
2) плазменные алгогены: брадикинин, простагландины. Выполняют функцию модуляторов, повышая чувствительность хемоноцицепторов.
3) Тахикинины при повреждающих воздействиях выделяются из окончаний нервов (вещество Р). Воздействуют местно на мембранные рецепторы того же нервного окончания.
I нейрон – тело в чувствительном ганглии соответствующих нервов, иннервирующих определенные участки организма.
II нейрон – в задних рогах спинного мозга. Далее болевая информация проводится двумя путями: специфическим (лемнисковым) и неспецифическим (экстралемнисковым).
Специфический путь начинается от вставочных нейронов спинного мозга. В составе спиноталамического тракта импульсы поступают к специфическим ядрам таламуса, (III нейрон), аксоны III нейрона достигают коры.
Неспецифический путь несет информацию от вставочного нейрона к различным структурам мозга. Выделяют три основных тракта, неоспиноталамический, спиноталамический и спиномезэнцефалический. Возбуждение по этим трактам поступает в неспецифические ядра таламуса, оттуда во все отделы коры больших полушарий.
Специфический путь заканчивается в соматосенсорной зоне коры.
Здесь происходит формирование острой, точно локализованной боли. Кроме того, за счет связей с моторной корой осуществляются моторные акты при воздействии болевых раздражений, происходит осознание и выработка программ поведения при болевом воздействии.
Неспецифический путь проецируется в различные области коры. Особое значение имеет проекция в орбитофронтальную область коры, которая участвует в организации эмоционального и вегетативного компонентов боли.
Характеристика антиноцицептивной системы.
Функция антиноцицептивной системы заключается в контроле над активностью ноцицептивной системы и предотвращении ее перевозбуждения. Ограничительная функция проявляется увеличением тормозного влияния антиноцицептивной системы на ноцицептивную систему в ответ на нарастающий по силе болевой стимул.
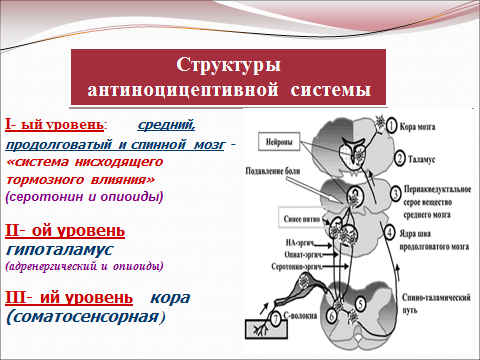
Первый уровень представлен комплексом структур среднего, продолговатого и спинного мозга, к которым относятся околоводопроводное серое вещество, ядра шва и ретикулярной формации, а также желатинозная субстанция спинного мозга.
Структуры этого уровня объединяются в морфофункциональную «систему нисходящего тормозного контроля». Медиаторами являются серотонин и опиоиды.
Второй уровень представлен гипоталамусом, который:
1) оказывает нисходящее тормозное влияние на ноцицептивные структуры спинного мозга;
2) активизирует систему «нисходящего тормозного контроля», т. е. первый уровень антиноцицептивной системы;
3) тормозит таламические ноцицептивные нейроны. Медиаторами этого уровня являются катехоламины, адренергические вещества и опиоиды.
Третьим уровнем является кора больших полушарий, а именно II соматотропная зона. Этому уровню отводится ведущая роль в формировании активности других уровней антиноцицептивной системы формирование адекватных реакций на повреждающие факторы.
Механизм деятельности антиноцицептивной системы.
Антиноцицептивная система оказывает свое действие посредством:
1) эндогенных опиоидных веществ: эндорфинов, энкефалинов, и динорфинов. Эти вещества, связываются с опиоидными рецепторами, имеющимися во многих тканях организма, особенно в ЦНС.
2) В механизме регуляции болевой чувствительности участвуют и неопиоидные пептиды: нейротензин, ангиотензин II, кальцитонин, бомбезин, холецистокинин, которые оказывают также тормозной эффект на проведение болевой импульсации.
3) В купировании определенных видов боли участвуют и непептидные вещества: серотонин, катехоламины.
В деятельности антиноцицептивной системы различают несколько механизмов, отличающихся друг от друга по длительности действия и нейрохимической природе.
Срочный механизм – активируется непосредственно действием болевого стимула и осуществляется с участием структур нисходящего тормозного контроля, Осуществляется серотонином, опиоидами, адренергическими веществами.
Этот механизм обеспечивает конкурентную аналгезию на более слабое раздражение, если одновременно на другое рецептивное поле действует более сильный.
Короткодействующий механизм активируется при кратковременном действии на организм болевых факторов. Центр – в гипоталамусе (вентромедиальное ядро) механизм – адренергический.
1) ограничивает восходящий ноцицептивный поток на уровне спинного мозга и супраспинальном уровне;
2) обеспечивает аналгезию при сочетании действия ноцицептивного и стрессогенного факторов.
Длительнодействующий механизм активизируется при длительном действии на организм ноциогенных факторов. Центром является латеральное и супраоптическое ядра гипоталамуса. Механизм опиоидный. Действует через структуры нисходящего тормозного контроля. Имеет эффект последействия.
1) ограничение восходящего ноцицептивного потока на всех уровнях ноцицептивной системы;
2) регуляция активности структур нисходящего контроля;
3) обеспечивает выделение ноцицептивной информации из общего потока афферентных сигналов, их оценку и эмоциональную окраску.
Тонический механизм поддерживает постоянную активность антиноцицептивной системы. Центры тонического контроля находятся в орбитальной и фронтальной областях коры больших полушарий. Нейрохимический механизм – опиоидные и пептидергические вещества
Управления двигательными функциями на уровне нервного центра (значимость рецепторов растяжения мышечных веретен, рецепторов гольджи, реципрокное функционирование нейронов)
Характеристика видов энергетического баланса
Виды энергетического баланса.
I У здорового взрослого человека существует энергетическое равновесие: поступление энергии = расходу. При этом масса тела остается постоянной, сохраняется высокая работоспособность.
IIПоложительный энергетический баланс.
Поступление энергии с пищей превышает расход. Приводит к избыточному весу. В норме у мужчин подкожный жир составляет 14 – 18%, а у женщин – 18 – 22%. При положительном энергетическом балансе эта величина возрастает до 50% от массы тела.
Причины положительного энергетического баланса:
1) наследственность (проявляется в повышенном литогенезе, адипоциты устойчивы к действию липолитических факторов);
2) поведение – избыточное питание;
3) заболевания обмена могут быть связаны:
а) с поражением гипоталамического центра регуляции обмена (гипоталамическое ожирение).
б) с повреждением лобных и височных долей.
Положительный энергетический баланс является фактором риска здоровья.
IIIОтрицательный энергетический баланс. Расходуется энергии больше, чем поступает.
а) недостаточность питания;
б) следствие сознательного голодания;
Методы определения объемной и линейной скорости кровотока
Объемная скорость кровотока.
Это объем крови, протекающий через поперечное сечение сосудов данного тила в единицу времени. Q = P1 – Р2 / R.
Р1 и Р2 – давление в начале и конце сосуда. R – сопротивление току крови.
Объем крови, протекающий в 1 минуту через аорту, все артерии, артериолы, капилляры или через всю венозную систему как большого, так и малого круга одинаков. R – общее периферическое сопротивление. Это суммарное сопротивление всех параллельных сосудистых сетей большого круга кровообращения.R = ∆ P / Q
Согласно законам гидродинамики сопротивление току крови зависит от длины и радиуса сосуда, от вязкости крови. Эти взаимоотношения описываются формулой Пуазейля:
Применительно к ССС наиболее изменчивые величины r и γ вязкость связана с наличием веществ в крови, характера кровотока – турбулентного или ламинарного
Линейная скорость кровотока.
Это путь, проходимый частицей крови в единицу времени. Y = Q / π · r 2
При постоянном объеме крови, протекающей через любое общее сечение сосудистой системы должна быть неодинаковой линейная скорость кровотока. Она зависит от ширины сосудистого русла. Y = S/t
В практической медицине измеряют время полного кругооборота крови: при 70 – 80 сокращениях время кругооборота составляет или 20 – 23 секунды. Вещество вводят в вену и ждут появления реакции.
Классификация потребностей. Классификация реакций, обеспечивающих поведение. Их хар-ка.
Процессы, обеспечивающие поведенческий акт.
Поведением называют все виды деятельности организма в окружающей среде. Поведение направлено на удовлетворение потребностей. Потребности формируются вследствие изменения внутренней среды или связаны с условиями обитания, в том числе и с социальными условиями жизни.
В зависимости от причин вызывающих потребности, их можно разделить на 3 группы.
1) Биологические или витальные. Связаны с необходимостью обеспечения существования организма (это пищевые, половые, оборонительные потребности и т. д.).
2) Познавательные или психо – исследовательские.
Появляются в виде любознательности, любопытства. У взрослых эти причины являются движущей силой исследовательской деятельности.
3) Социальные потребности. Связаны с жизнью в обществе, с ценностями данного общества. Проявляются в виде потребности иметь определенные бытовые условия, занимать определенное положение в обществе, играть определенную роль, получать услуги определенного уровня и т. д. Видом социальной потребности является жажда власти, денег т. к. это зачастую является условием достижения других социальных потребностей.
Различные потребности удовлетворяются с помощью врожденных или приобретенных программ поведения.
Одна и та же, по сути, поведенческая реакция носит индивидуальный характер, связанный с индивидуально – типологическими особенностями субъекта.
Характеристика реакций обеспечивающих поведение.
Они делятся на 2 группы: врожденные и приобретенные
Врожденные: безусловный рефлекс, реакции, программируемые нервными центрами: инстинкт, импринтинг, ориентировочный рефлекс, мотивации
Антиноцицептивная система
В практике врача встречаются случаи, когда люди страдают врожденным отсутствием чувства боли (врожденная аналгия) при полном сохранении проводящих ноцицептивных путей. Кроме того, имеют место клинические наблюдения спонтанных болевых ощущений у людей при отсутствии внешних повреждений или заболеваний. Объяснение этих и подобных факторов стало возможным с появлением в 70-х годах XX в. представления о существовании в организме не только ноцицептивной, но и антиноцицептивной, антиболевой, или обезболивающей, эндогенной системы. Существование антиноцицептивной системы было подтверждено экспериментами, когда электростимуляция некоторых точек ЦНС приводила к отсутствию специфических реакций на болевые раздражения. При этом животные оставались в бодрствующем состоянии и адекватно реагировали на сенсорные стимулы. Следовательно, можно было заключить, что электростимуляция в таких экспериментах приводила к формированию состояния аналгезии, подобно врожденной аналгии у людей.
Антиноцицептивная система выполняет функцию «ограничителя» болевого возбуждения. Эта функция заключается в контроле за активностью ноцицептивных систем и предотвращении их перевозбуждения. Проявляется ограничительная функция в увеличении тормозного влияния антиноцицептивной системы в ответ на нарастающий по силе ноцицептивный стимул. Однако это ограничение имеет предел и при сверхсильных болевых воздействиях на организм, когда антиноцицептивная система не в состоянии выполнить функцию ограничителя, может развиваться болевой шок. Кроме того, при снижении тормозных влияний антиноцицептивной системы перевозбуждение ноцицептивной системы может приводить к возникновению спонтанных психогенных болей, часто проецирующихся в нормально функционирующие органы (сердце, зубы и др.). Следует учесть, что активность антиноцицептивной системы имеет генетическую обусловленность.
Антиноцицептивная система представляет собой совокупность структур, расположенных на разных уровнях ЦНС, имеющих собственные нейрохимические механизмы.
Первый уровень представлен комплексом структур среднего, продолговатого и спинного мозга, к которым относятся серое околоводопроводное вещество, ядра шва и ретикулярной формации, а также желатинозная субстанция спинного мозга. Возбуждение этих структур по нисходящим путям оказывает тормозное влияние на «ворота боли» спинного мозга, угнетая тем самым восходящий ноцицептивный поток. Структуры, реализующие данное торможение, в настоящее время объединяют в морфофункциональную «систему нисходящего тормозного контроля», медиаторами которой являются серотонин, а также опиоиды.
Второй уровень представлен в основном гипоталамусом, который:
1) оказывает нисходящее тормозное влияние на ноцицептивные нейроны спинного мозга;
2) активирует «систему нисходящего тормозного контроля», т.е. первый уровень антиноцицептивной системы;
3) тормозит таламические ноцицептивные нейроны.
Гипоталамус опосредует свое действие через адренергический и опиоидный нейрохимические механизмы.
Третьим уровнем является кора большого мозга, а именно II соматосенсорная зона. Этому уровню отводится ведущая роль в формировании активности других структур антиноцицептивной системы и адекватных реакций на повреждающие факторы.
Психогенная регуляция болевого ощущения. Это корковая регуляция и эмоциональные состояния переживаемые человеком, в результате которых изменяются пороги болевой чувствительности. Известны случаи снижения болевой чувствительности. Когда человек заранее предупрежденный о воздействии болевого раздражителя, как бы настраивается на возникновение боли и легче ее переносят.
Механизмы деятельности антиноцицептивной системы.
Эндогенные механизмы регуляции болевого ощущения.
Механизм обезбаливающего ЭФФЕКТА
Опиоидная система действует как нейромедиаторы, возникает ТПСП на ноцицепторах. Вызывает выработку ГАМК- ТПСП торможение., т.е. является нейромодулятором.
Эндерфины(d b y) и энкефалины (метионин и лейцин-энкефалин). Эндогенные опиоиды на уровне переферических ноцицептеров угнетают действие веществ, вызывающих боль. Они также способны уменьшить активность С-волокон, угнетать спонтанную и вызванную активность нейронов на ноцицептивную импульсацию, формируя у людей состояние анальгезии. Одновременно эндорфины активизируют антиноцицептивную систему. НАЛОКСОН- блокирует действие опиатной системы.
В настоящее время известно четыре типа опиатных рецепторов: мю-, дельта-, каппа- и сигма. В организме вырабатываются собственные эндогенные опиоидные вещества в виде олигопептидов, получивших название эндорфинов (эндоморфинов), энкефалинов и динорфинов. Эти вещества связываются с опиатными рецепторами и приводят к возникновению пре- и постсинаптического торможения в ноцицептивной системе, следствием чего являются состояния аналгезии или гипалгезии. Такая гетерогенность опиатных рецепторов и соответственно избирательная к ним чувствительность (аффинитет) опиоидных пептидов отражает различные механизмы болей разного происхождения.
Кроме пептидов эндогенной антиноцицептивной природы, установлены и непептидные вещества, участвующие в купировании определенных видов боли, например серотонин, катехоламины. Возможно, что существуют и другие нейрохимические вещества антиноцицептивной эндогенной системы организма, которые предстоит открыть.
IY. Норадренергическая система (главная роль принадлежит Голубому пятну) Включается при отрицательных стенических реакциях (ярость, гнев- при драке)
В деятельности антиноцицептивной системы различают несколько механизмов, отличающихся друг от друга по длительности действия и по нейрохимической природе медиаторов.
Срочный механизм активируется непосредственно действием болевых стимулов и реализуется с участием структур нисходящего тормозного контроля. Этот механизм осуществляется через активацию серотонин – и опиоидергических нейронов, входящих в состав серого околоводопроводного вещества и ядер шва, а также адренергических нейронов ретикулярной формации. Благодаря срочному механизму обеспечивается функция ограничения афферентного ноцицептивного потока на уровне нейронов задних рогов спинного мозга и каудальных отделов ядер тригеминального комплекса. За счет срочного механизма реализуется конкурентная аналгезия, т.е. подавление болевой реакции на стимул в том случае, когда одновременно действует другой, более сильный стимул на другую рецептивную зону.
Длительно действующий механизм активируется при длительном действии на организм ноцигенных факторов. Центром его являются латеральное и супраоптическое ядра гипоталамуса. По нейрохимической природе этот механизм опиоидный. При этом вовлекаются системы нисходящего тормозного контроля, поскольку между этими структурами и гипоталамусом имеются хорошо выраженные двусторонние связи. Длительно действующий механизм имеет хорошо выраженный эффект последействия. Функции этого механизма заключаются в ограничении восходящего ноцицептивного потока на всех уровнях ноцицептивной системы и регуляции активности системы нисходящего тормозного контроля. Данный механизм обеспечивает также выделение ноцицептивной афферентации из общего потока афферентных возбуждений, их оценку и эмоциональную окраску.
Тонический механизм поддерживает постоянную активность антиноцицептивной системы. Центры расположены в орбитальной и фронтальной областях коры большого мозга, а также в гипоталамусе. Основными нейрохимическими механизмами являются опиоидные и пептидергические. Его функция заключается в постоянном тормозном влиянии на активность ноцицептивной системы на всех уровнях ЦНС даже в отсутствие ноцицептивных воздействий.
Ноцицептивная система и антиноцицептивная системы составляют болевой баланс организма.
Взаимодействие болевой и обезболивающей систем. Состояние гипералгезии (повышенная болевая чувствительность) может быть обусловлено как увеличением активности ноцицептивной системы, так и снижением тонуса антиноцицептивной системы. При гипалгезии возникают противоположные взаимоотношения. Функциональные изменения тонуса антиноцицептивной или ноцицептивной систем, приводящие к изменению болевой чувствительности, имеют, безусловно, приспособительное значение. Так, повышение тонуса ноцицептивной системы или снижение тонуса антиноцицептивной при реакции настораживания приводит к снижению порогов боли, что дает больше возможностей для идентификации опасных для организма раздражителей внешней среды. Взаимодействие ноцицептивной и антиноцицептивной эндогенных систем формирует порог боли, т.е. выступает как механизм регуляции болевой чувствительности. Ноцицептивная и антиноцицептивная системы входят в одну функциональную систему, деятельность которой направлена на сохранение целостности тканей организма. Нормальное функционирование данных систем возможно только при сохранении активности обеих взаимодействующих частей.
АНТИНОЦИЦЕПТИВНАЯ СИСТЕМА
Полный текст:
Аннотация
Ключевые слова
Об авторах
Список литературы
1. Крыжановский Г.Н., Графова В.Н., Данилова Е.З., Игонькина С.Н., Сахарова О.П. Болевой синдром спинального происхождения // Бюлл. экспер. биол. и мед. – 1973. – №9. – С.31-35.
2. Крыжановский Г.Н., Графова В.Н., Данилова Е.З., Игонькина С.Н. Исследование болевого синдрома спинального происхождения (к концепции генераторного механизма болевого синдрома) // Бюлл. экспер. биол. и мед. – 1974. – № 7. – С. 15-20.
4. Овсянников В.Г. Боль (этиология, патогенез, принципы и механизмы лечения). – Ростов н/Д., 1990. – 80 с.
5. Овсянников В.Г. Боль // Общая патология. – Ростов-н/Д.: Цветная печать, 1997. – С. 223-236.
6. Овсянников В.Г. Боль как феномен патологии // III научная сессия РГМУ. – Ростов-н/Д., 2000. – С. 102-103.
7. Овсянников В.Г. Онтогенетические особенности центральных аминергических механизмов в норме и при острой соматической боли. – Ростов-н/Д.: Учебная типография Рост-ГМУ, 2012. – 116 с.
8. Bingel U., Schoell E., Herken W., Buchel C., May A. Habituation to painfull stimulation involves the antinociceptive system // Pain. – 2007. – Vol. 131, issue 1-2. – Р. 21-30.
9. Овсянников В.Г. Очерки патофизиологии боли. Учебное пособие для студентов и врачей. – Ростов-на-Дону: РГМУ, 2003. – 148 с.
10. Daroff R.B., Fenichel G.M., Jankovic J., Mazziotta J.C. Principles of Pain Management // Bradley’s Neurology in Clinical Practice. – 2012. – Sixth Edition, Chapter 44. – Р. 783-801.
11. Basbaum A., Moss M., Glazer E. Opiate and stimulation produced analgesia: the contribution of the mono-amines // Advances in Pain Research and Therapy. V. 5. Eds Bonica J., Lindblom U., Iggo A.N.Y.: Raven Press, 1983. – P. 323-329.
12. Лиманский Ю.П. Физиология боли. – Киев, 1986. – 93 с.
14. Брагин Е.О. Нейрохимические механизмы регуляции болевой чувствительности // Успехи физиол. наук. – 1985. – Т. 16, № 1. – С. 21-42.
16. Slipman C.W., Derby R., Simione F.A., Mayer T.G., Chou L.H., Lenrow D.A., Addi Salahadin, Chin K.R. Central influence on Pain. Interventional Spine: An Algorithmic Approach, First Edition. – 2008. – Chapter 5. – P. 39-52.
17. Крыжановский Т.Н., Данилова Е.И., Графова В.Н., Решетняк В.К. Особенности развития болевых синдромов при взаимодействии генераторов патологически усиленного возбуждения // Бюлл. экспер. биол. и мед. – 1994. – Т. 118, № 10. – С. 364-367.
18. Goadsby P., Lance I. Physiopathologie de la migraine // Revne du Praticien. 1990. – Vol. 40, № 5. – P. 389-393.
19. Takagi H., Harima A. Analgesic effect of L-threo-3,4-dihydroxyphenilserine (L-DOPS) in patients with chronic pain // European Neuro-psychopharmacology. – 1996. – Vol. 6, № 1. – P. 43-47.
20. Wei H., Petrovaara A. Peripheral administered alfa-2-adrenoreceptor agonist in modulation of chronic allodynia induced by spinal nerve ligation in the rat // Anesthesia and Analgesia. – 1997. – Vol. 85, № 5. – P. 1122-1127.
21. Зайцев А.А. Фармакологический анализ опиоид- и адренергических механизмов регуляции гемодинамических ноцицептивных реакций // Нейрофармакологическая регуляция болевой чувствительности. – Л., 1984. – С. 53-74.
22. Зайцев А.А. Особенности и механизмы болеутоляющего действия клофелина // Актуальные проблемы лекарственного обезболивания. – Л., 1989. – С. 62-65.
23. Gordon N., Heller P., Levin I. Enhancement of pentazocine-analgesia by clonidine // Pain. – 1992. – Vol. 48. – P. 167-170.
25. Sagan I. Chromaffin cell transplants for alleviation of chronic pain // ASSAIO Journal. – 1992. – Vol. 38, № 1.– P. 24-28.
26. Decosterd I., Buchser E., Gilliard N. et al. Intrathecal implants of bovine chromaffin cells alleviate mechanical allodynia in a rat model of neuropathic Pain // Pain. – 1998. – Vol. 76, № 1-2. – P. 159-166.
27. Михайлович В.А., Игнатов Ю.Д. Болевой синдром. – Л.: Медицина, 1990. – 336 с.
28. McMahon S.B., Koltzenburg Martin, Tracey Irene, Dennis C. Turk. Representation of pain in the Brain // Wall and Melzack, Textbook of Pain. – 2013. – Sixth edition, Chapter 7. – P. 111-128.
29. Каракулова Ю.В. О патогенетических механизмах формирования головных болей напряжения // Журнал неврологии и психиатрии им. С.С.Корсакова. – 2006. – т.106, 7б. –С. 52-56.
30. Ушакова С.А. Клинико-диагностическая оценка состояния серотонинергической системы и активности сукцинатдегидрогеназы у больных с болевыми синдромами: Автореф…. дисс. канд. мед. наук. – 1998, Саратов. – 27 стр.
31. Данилов А.Б., Давыдов О.С. // Нейропатическая боль. – М, 2007. –191 стр.
32. Haze I. Toward an understanding of the rationale for the use of dietary supplementation for chronic pain management: serotonin model // Cranio. – 1991. – Vol. 9, №4. – P. 339-343.
33. Chen A. An introduction to segmental electric acupuncture in the treatment of stress related physical and mental disorders // Acupuncture and Electro-Therapeutics Research. – 1992. – Vol. 17, № 4. – P. 273-283.
35. Овсянников В.Г., Шумарин А.Е., Зайнаб А.М., Простов И.К. Изменение содержания и соотношения серотонина и гистамина в структурах головного мозга и спинном мозге крыс при острой соматической боли различной локализации //Материалы V научной конференции РостГМУ. – Ростов-н/Д., 2010. – С. 190-192.
36. Ярош А.К. Роль холин- и адренергических механизмов в регуляции болевой чувствительности животных в динамике постоперационного эмоционально-болевого состояния // Республиканский межведомственный сборник «Фармакология и токсикология». – Киев, 1987. – С. 63-66.
38. Terman G., Levis I., Liebeskind I. Endogenous Pain Inhibitory Substrates and Mechanisms Recent Advances in the Management of Pain. – 1984. – P. 43-56.
39. Jose de Andres. Clinical experience with botulinum toxin Type A in back pain: a European Perspective // Pain Management in the 21-st Century. 2-th World Congress of the World Institute of Pain. – Istanbul, June 2001. – P. 5-7.
40. Royal M. Clinical experience with botulinum toxin Type A in back pain: a US Perspective // Pain Management in the 21-st Century. 2-th World Congress of the World Institute of Pain. – Istanbul, June 2001. – P. 7-9.
41. Игнатов Ю.Д., Андреев Б.В. ГАМК-ергические механизмы регуляции болевой чувствительности // Нейро-фармакологические аспекты боли. – Л., 1982. – С. 61-81.
42. Андреев Б.В. ГАМК-ергические механизмы боли и аналгезии: Автореф. … дисс. докт. мед. наук. – СПб., 1993. – 42 с.
44. Чурюканов М.В., Чурюканов В.В. Функциональная организация и терапевтический потенциал эндогенной каннабиноидной системы // Эксперим. и клиническая фармакология. – 2004. – №2 – С. 70-78.
45. Алексеев В.А. с соавт. Боль. Руководство для врачей. – М., 2009. – 303 с.
48. Mobarakeh J.I., Yanai K., Takahashi K., Sakurada Sh. // Future medical engineering based on Bionanotechnology: Proceedings of the final Symposium of the Tohoku University 21st Century Center of Exellence Program / Sendai International Center. – Japan, 2007. – P. 771-783.
Для цитирования:
Овсянников В.Г., Бойченко А.Е., Алексеев В.В., Каплиев А.В., Алексеева Н.С., Котиева И.М., Шумарин А.Е. АНТИНОЦИЦЕПТИВНАЯ СИСТЕМА. Медицинский вестник Юга России. 2014;(3):46-54. https://doi.org/10.21886/2219-8075-2014-3-46-54
For citation:
Ovsyannikov V.G., Boychenko A.E., Alekseev V.V., Kapliev A.V., Alekseeva N.S., Kotieva I.M., Shumarin A.E. Department of pathological physiology. Medical Herald of the South of Russia. 2014;(3):46-54. (In Russ.) https://doi.org/10.21886/2219-8075-2014-3-46-54