что такое бласты в костном мозге
Что такое бласты в костном мозге
На основании общеклинического анализа крови сложно дать оценку состояния гемопоэза. Более полное представление дает изучение костного мозга (цитологическое, цитохимическое и др.).
Цитологический анализ костного мозга играет большую роль в диагностике заболеваний кроветворной системы. Подсчет миелограммы дает представление о характере эритропоэза (нормобластический или мегалобластический), позволяет обнаружить клетки, характерные для различных заболеваний системы крови (множественной миеломы, острых лейкозов, хронического миелолейкоза, хронического лимфолейкоза, лейкемизированных неходжкинских лимфом, болезни Гоше, Ниманна-Пика, метастазов рака в костном мозге и др.).
Данные миелограммы необходимы для проведения дифференциального диагноза с лейкемоидными реакциями. Сопоставление данных костномозгового кроветворения с картиной периферической крови и клинической симптоматикой позволяет уточнить причину анемии.
Имеются абсолютные и относительные показания к стернальной пункции.
Абсолютные показания: все анемии (кроме типичной железодефицитной), различные цитопении (одноростковая, двуростковая, панцитопения), острые лейкозы, хронические лейкозы в начальной стадии (для подтверждения диагноза и исключения лейкемоидных реакций), выраженное изолированное увеличение СОЭ (для исключения множественной миеломы и макроглобулинемии Вальденстрема), подозрение на метастазы злокачественной опухоли в костном мозге.
Относительные показания: железодефицитные анемии, хронические лейкозы в развернутой стадии.
Аспирационная биопсия костного мозга является технически простым, безопасным и легкодоступным методом. Наиболее часто используется стернальная пункция, предложенная в 1927 г. М. И. Аринкиным и впервые выполненная на кафедре факультетской терапии Военно-медицинской академии. При необходимости можно пунктировать гребень или бугристость подвздошной кости, у детей — пяточную кость. Пункция грудины выполняется иглой И. А. Кассирского с предохранительным щитком. После взятия аспирата костного мозга производят подсчет количества миелокариоцитов, мегакариоцитов, ретикулоцитов, готовят мазки для подсчета миелограммы.
Нормальная миелограмма
| Показатели миелограммы | Среднее значение (%) | Пределы колебаний (%) |
| Ретикулярные клетки | 0,9 | 0,1-1,6 |
| Недифференцированные бласты | 0,6 | 0,1-1,1 |
| Миелобласты | 1,0 | 0,2-1,7 |
| Промиелоциты | 2,5 | 1,0-4,1 |
| Миелоциты нейтрофильные | 9,6 | 7,0-12,2 |
| Метамиелоциты нейтрофильные | 11,5 | 8,0-15,0 |
| Палочкоядерные нейтрофилы | 18,2 | 12,8-23,7 |
| Сегментоядерные нейтрофилы | 18,6 | 13,1-24,1 |
| Всего клеток нейтрофильного ряда | 60,8 | 52,7-68,9 |
| Миелоциты эозинофильные | 0,1 | 0,0-0,2 |
| Метамиелоциты эозинофильные | 0,2 | 0,1-0,4 |
| Эозинофилы | 2,8 | 0,4-5,2 |
| Всего клеток эозинофилъного ряда | 3,2 | 0,5-5,8 |
| Миелоциты базофильные | 0,1 | 0-0,3 |
| Базофилы | 0,1 | 0-0,3 |
| Всего клеток базофильного ряда | 0,2 | 0-0,5 |
| Лимфобласты | 0,1 | 0-0,2 |
| Пролимфоциты | 0,1 | 0-0,2 |
| Лимфоциты | 8,8 | 4,3-13,3 |
| Всего клеток лимфоидного ряда | 9,0 | 4,3-13,7 |
| Монобласты | 0,1 | 0-0,2 |
| Моноциты | 1,9 | 0,7-3,1 |
| Плазмобласты | 0,1 | 0-0,2 |
| Проплазмоциты | 0,1 | 0,1-0,2 |
| Плазматические клетки | 0,9 | 0,1-1,8 |
| Эритробласты | 0,6 | 0,2-1,1 |
| Нормобласты базофильные | 3,6 | 1,4-5,8 |
| Нормобласты полихроматофильные | 12,9 | 8,9-16,9 |
| Нормобласты оксифильные | 3,2 | 0,8-5,6 |
| Всего клеток эритроидного ряда | 20,5 | 14,5-26,5 |
| Мегакариоциты | 0,4 | 0,2-0,6 |
Миелокариоциты миелограммы. У здоровых людей количество миелокариоцитов (всех ядросодержащих клеток костного мозга) в камере Горяева составляет 50-250•10 9 /л.
Мегакариоциты миелограммы. Нормальное количество мегакариоцитов в камере Фукса-Розенталя составляет 0,05-0,1•10 6 /л. Необходимо также определять количество мегакариоцитов в окрашенных мазках в 250 полях зрения под малым увеличением и при подсчете миелограммы в процентах.
Следует помнить, что снижение уровня миелокариоцитов и мегакариоцитов в миелограмме отмечается также при разведении аспирата периферической кровью (технические погрешности при выполнении стернальной пункции).
Ретикулоциты миелограммы. Нормальное количество ретикулоцитов в костном мозге составляет 20-30%о. Увеличение их числа наблюдается при гемолитических и постгеморрагических анемиях.
Морфологический анализ клеток костного мозга (подсчет миелограммы) производят на 500 клеток костного мозга, после чего вычисляют процентное содержание каждого вида клеток.
При анализе миелограммы необходимо оценить клеточность костного мозга (нормо-, гипо- или гиперклеточный), дать качественную характеристику всех клеточных рядов с определением индексов созревания, лейкоэритробластического соотношения, характера эритропоэза (нормобластический, мегалобластический или с мегалобластоидными чертами) и количества митозов. Отдельно следует оценить мегакариоцитопоэз (количество и функция мегакариоцитов).
Костномозговой индекс созревания нейтрофилов определяется по формуле: (промиелоциты + миелоциты + метамиелоциты)/ (палочкоядерные + сегментоядерные нейтрофилы)
В норме костномозговой индекс созревания нейтрофилов равен 0,6-0,8.
Индекс созревания эритроидных клеток определяется по формуле: (полихроматофильные + оксифильные нормоциты)/(эритробласты + базофильные + полихроматофильные + оксифильные нормоциты)
В норме индекс созревания эритроидных клеток равен 0,8-0,9.
Уменьшение индекса свидетельствует о задержке гемоглобинизации и/или преобладании молодых базофильных нормоцитов, дает возможность ориентировочно оценить запасы и обмен железа в организме.
Лейкоэритробластическое соотношение определяется по формуле: (гранулоциты): (ядросодержащие клетки эритроидного ряда) и в норме составляет 3-4:1.
Количество митозов в норме составляет 3,5 на 1000 для клеток гранулоцитарного ряда и 5 на 1000 — для клеток эритроидного ряда.
Заключение по миелограмме не должно быть категоричным, поскольку для постановки диагноза необходимо учитывать клинические данные и показатели периферической крови.
Для более полной характеристики гемопоэза, особенно мегакариоцитопоэза, в ряде случаев требуется гистологическое исследование костного мозга методом трепанобиопсии.
Определение сидеробластов и сидероцитов в миелограмме
При железодефицитных и сидеробластных анемиях важно определять количество сидероцитов и сидеробластов — эритроцитов и эритробластов, содержащих в цитоплазме железо в виде гемосидерина и ферритина (зернышки синего цвета при окраске по Перлсу диаметром 0,2-1,5 мкм). У здоровых людей в периферической крови содержится 1,1-3,0% (в среднем 1,6%) сидероцитов. Содержание сидеробластов в костном мозге составляет 15-40% от всех клеток эритроидного ряда; количество гранул в них обычно 1-2 (не более 4).
Клиническое значение. При хронических железодефицитных анемиях отмечается снижение количества сидероцитов и сидеробластов в костном мозге, гранулы железа в них практически выявить не удается.
Увеличение количества сидеробластов с большим количеством гранул железа в каждом из них, появление кольцевых форм сидеробластов наблюдается при наследственных и приобретенных сидеробластных анемиях (интоксикация свинцом, один из вариантов миелодиспластического синдрома — рефрактерная анемия с кольцевыми сидеробластами).
Наряду с исследованием крови и костного мозга для диагностики специфических поражений и осложнений проводимой терапии в ряде случаев необходим анализ биологических жидкостей (мочи, кала, мокроты, экссудатов, ликвора).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое бласты в костном мозге
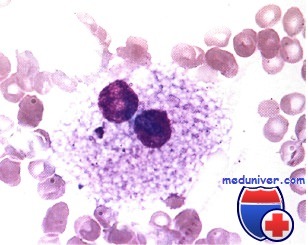
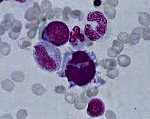
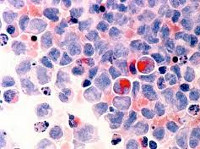
Острые лейкозы – это самые опасные и стремительные болезни крови. При острых лейкозах происходит поломка на уровне самых молодых клеток крови, клеток-предшественников, клеток-бластов, которые являются одним из подвидов белых кровных телец, лейкоцитов. Слово бласт происходит от слова blastos, что по-гречески означает «росток, зародыш, побег». Бласты – это быстро растущие клетки. Здоровая бластная клетка со временем развивается в какую-либо полезную клетку крови. В норме число бластов не превышает 1% от всех клеток костного мозга. В кровь они почти никогда не выходят. Если человеку срочно понадобилось большое число каких-нибудь клеток крови (например, лейкоцитов при тяжелой инфекции), то бластов организм может вырабатывать и больше, но все же их относительное число редко превышает 10%.
Бласты, которые размножаются при остром лейкозе, другие. Их можно сравнить с хулиганами-тунеядцами в человеческом обществе, потому что они не работают, питаются запасами организма и вместо собственного развития в полезные клетки быстро плодят себе подобных. Лейкозные бласты вытесняют здоровые клетки крови из их дома внутри костей и поселяются там сами. Из-за этого нарушается процесс обновления нормальной крови, начинается ее дефицит: быстро снижается гемоглобин, тромбоциты, здоровые лейкоциты. Пациент начинает слабеть, могут появиться самопроизвольные кровотечения и высокая температура. В анализе крови врач видит снижение гемоглобина и тромбоцитов и резкое повышение лейкоцитов за счет опухолевых клеток-бластов. Больше всего опухолевых клеток в костном мозге.
Принципиально врачи выделяют два типа бластов: лимфобласты и миелобласты. В зависимости от типа бластов и лейкозы бывают лимфобластные и миелобластные (нелимфобластные). Это зависит от того, в начале какого из двух путей развития клетки крови произошла авария.
В норме из здоровых лимфобластов (клеток-предщественников) образуются высокоспециализированные клетки иммунной системы В- и Т- лимфоциты. Задачи В- и Т-клеток можно сравнить с задачами войск специального назначения, которые действуют точно и эффективно. Из миелобластов в дальнейшем получаются остальные виды клеток: красные кровяные тельца, тромбоциты, гранулоциты. Красные кровяные тельца (эритроциты) – переносят кислород, тромбоциты отвечают за свертывание крови, если мы, например, поранились. Гранулоциты – «общевойсковая» часть иммунной системы, они действуют более массированными ударами.
Если произошла поломка, то нормальные клетки не созревают, а бласты остаются недоразвитыми. По внешнему виду бласта, а также с помощью проточной цитометрии можно определить, какая клетка могла бы из него получиться. Это важно для выбора лечения и понимания, насколько успешным будет лечение. Вид клеток-предшественников врачи обозначают в диагнозе, например: острый В-лимфобластный лейкоз (лейкоз из клеток-предшественников В-лимфоцитов), острый монобластный лейкоз (лейкоз из клеток-предшественников моноцитов) и т.д.
Диагноз «острый лейкоз» ставят, если выясняют, что бластов в костном мозге пациента более 20%. Чтобы понять, какой именно лейкоз у больного, делают проточную цитометрию бластов.
Острые лейкозы бывают очень разные. Лейкоз, например, может появиться «на ровном месте», то есть у человека, у которого никогда не было никаких болезней страшнее насморка. Такими лейкозами обычно болеют дети и молодые люди. У людей старшего возраста острые лейкозы, как правило, вторичны. Это значит, что в результате каких-то причин (химиотерапия по поводу других болезней, облучение или отравление некоторыми химическими веществами) может нарушиться кроветворение, то есть появляется так называемый миелодиспластический синдром (мы уже описывали его в других разделах нашего сайта). Последней ступенью миелодиспластического синдрома является вторичный острый лейкоз. Первичные лейкозы более агрессивны, чем вторичные, но все лейкозы лечат по единым принципам. Чтобы полностью вылечить пациента, часто необходимо сделать пересадку донорских стволовых клеток крови.
О некоторых типах острых лейкозов мы расскажем в этой главе:
Что такое бласты в костном мозге
Лейкоз – это злокачественное заболевание, при котором в костном мозге нарушается процесс кроветворения. В результате в кровь попадает большое количество незрелых лейкоцитов, которые не справляются со своей основной функцией – защитой организма от инфекций. Постепенно они вытесняют здоровые клетки крови, а также проникают в различные органы, нарушая их работу.
Рак крови – одно из самых распространенных онкологических заболеваний, которое встречается как у детей, так и у взрослых. Прогноз заболевания зависит от множества факторов: типа лейкоза, возраста пациента, сопутствующих заболеваний. За последние десятилетия были разработаны и постоянно совершенствуются методы эффективного лечения лейкемии.
Лейкемия, белокровие, рак крови.
Leukemia, leucosis, bloodcancer.
Симптомылейкоза могут развиваться остро или постепенно. Они неспецифичны, зависят от типа лейкоза и на начальных этапах могут напоминать грипп или другое инфекционное заболевание.
Симптомами лейкоза являются:
Общая информация о заболевании
Все клетки крови – лейкоциты, эритроциты, тромбоциты – образуются в костном мозге – специфической кроветворной ткани, которая находится в костях таза, грудине, позвонках, ребрах, длинных трубчатых костях. Он содержит стволовые клетки, которые дают начало всем клеткам крови. В процессе деления из них сначала формируются лимфоидные и миелоидные стволовые клетки. Из лимфоидных стволовых клеток образуются лимфобласты, а из миелоидных – миелобласты, а также предшественники эритроцитов и тромбоцитов. Из лимфобластов и миелобластов получаются лейкоциты. Бласты отличаются от зрелых лейкоцитов строением и функциями и должны пройти через ряд последовательных делений, в ходе которых образуются все более специализированные клетки-предшественники. После последнего деления из предшественников формируются зрелые, функциональные клетки крови. Таким образом, из лимфоидных стволовых клеток образуются лимфоциты (разновидность лейкоцитов), а из миелоидных – эритроциты, тромбоциты и остальные виды лейкоцитов (нейтрофилы, базофилы, эозинофилы и моноциты). Это зрелые клетки крови, способные выполнять свои специфические функции: эритроциты доставляют кислород к тканям, тромбоциты обеспечивают свертываемость крови, лейкоциты – защиту от инфекций. После выполнения своей задачи клетки погибают.
Весь процесс деления, гибели и созревания клеток крови заложен в их ДНК. При ее повреждении нарушается процесс роста и деления клеток крови, преимущественно лейкоцитов. В кровь попадает большое количество незрелых лейкоцитов, не способных выполнять свою функцию, и в результате организм не справляется с инфекциями. Незрелые клетки очень активно делятся, живут дольше, постепенно вытесняя другие клетки крови – эритроциты и тромбоциты. Это приводит к анемии, слабости, частым длительным кровотечениям, кровоизлияниям. Незрелые лейкоциты также могут проникать в другие органы, нарушая их функцию, – в печень, селезенку, лимфатические узлы, головной мозг. В результате пациент жалуется на боли в животе и в голове, отказывается от еды, худеет.
В зависимости от того, какой тип лейкоцитов вовлечен в патологический процесс и как быстро развивается заболевание, различают следующие виды лейкозов.
Таким образом, при острых лейкозах в костном мозге и крови накапливается большое количество незрелых, бесполезных лейкоцитов, что требует незамедлительного лечения. При хронических лейкозах заболевание начинается постепенно, в кровь попадают более специализированные клетки, способные какое-то время выполнять свою функцию. Они могут протекать годами, не проявляя себя.
Кто в группе риска?
Основные методы диагностики лейкемии
Изменение уровня лейкоцитов, эритроцитов, тромбоцитов, внешний вид лейкоцитов, степень их зрелости позволяют врачу заподозрить у пациента лейкоз. Похожие изменения в соотношении клеток крови возможны и при других заболеваниях – инфекциях, иммунодефицитных состояниях, отравлениях токсическими веществами, – однако при них в крови отсутствуют бласты – предшественники лейкоцитов. Бласты имеют характерные признаки, хорошо различимые под микроскопом. Если они обнаружены в крови, велика вероятность того, что у пациента один из видов лейкоза, поэтому необходимо дальнейшее обследование.
Дополнительно врач может назначить:
Тактика лечения лейкоза определяется типом заболевания, возрастом пациента и его общим состоянием. Оно проводится в специализированных гематологических отделениях больниц. Лечение острого лейкоза необходимо начинать как можно раньше, хотя в случае хронического лейкоза при медленном прогрессировании заболевания и хорошем самочувствии терапия может быть отложена.
Существует несколько методов лечения лейкемии.
Прогноз заболевания зависит от типа лейкоза. При остром лимфобластном лейкозе более 95 % пациентов излечивается, при остром миелобластном – около 75 %. При хронических лейкозах на прогноз влияет стадия заболевания, на которой начато лечение. Этот тип лейкоза прогрессирует медленно, и средняя продолжительность жизни пациентов составляет 10-20 лет.
Специфическая профилактика лейкозов отсутствует. Для своевременной диагностики заболевания необходимо регулярно проходить профилактические медицинские осмотры.
Рекомендуемые анализы
Миелодиспластический синдром
Миелодиспластический синдром – группа гематологических заболеваний, при которых наблюдаются цитопения, диспластические изменения костного мозга и высокий риск возникновения острого лейкоза. Характерные симптомы отсутствуют, выявляются признаки анемии, нейтропении и тромбоцитопении. Диагноз устанавливается с учетом данных лабораторных анализов: полного анализа периферической крови, гистологического и цитологического исследования биоптата и аспирата костного мозга и т. д. Дифференциальный диагноз может представлять значительные затруднения. Лечение – переливание компонентов крови, химиотерапия, иммуносупрессивная терапия, пересадка костного мозга.
Общие сведения
Миелодиспластический синдром – группа заболеваний и состояний с нарушениями миелоидного кроветворения и высоким риском развития острого лейкоза. Вероятность развития увеличивается с возрастом, в 80% случаев данный синдром диагностируется у людей старше 60 лет. Мужчины страдают несколько чаще женщин. У детей миелодиспластический синдром практически не встречается. В последние десятилетия гематологи отмечают увеличение заболеваемости среди лиц трудоспособного возраста. Предполагается, что причиной «омоложения» болезни могло стать существенное ухудшение экологической обстановки.
До недавнего времени лечение миелодиспластического синдрома было только симптоматическим. Сегодня специалисты разрабатывают новые методы терапии, однако эффективное лечение этой группы болезней все еще остается одной из самых сложных проблем современной гематологии. Пока прогноз при миелодиспластическом синдроме, в основном, зависит от особенностей течения болезни, наличия или отсутствия осложнений. Лечение осуществляют специалисты в сфере онкологии и гематологии.
Причины и классификация миелодиспластического синдрома
С учетом причин развития различают два типа миелодиспластического синдрома: первичный (идиопатический) и вторичный. Идиопатический вариант выявляется в 80-90% случаев, диагностируется преимущественно у пациентов старше 60 лет. Причины возникновения установить не удается. В числе факторов риска первичного миелодиспластического синдрома – курение, повышенный уровень радиации при выполнении профессиональных обязанностей или проживании в неблагоприятной экологической зоне, частый контакт с бензином, пестицидами и органическими растворителям, некоторые наследственные и врожденные заболевания (нейрофиброматоз, анемия Фанкони, синдром Дауна).
Вторичный вариант миелодиспластического синдрома наблюдается в 10-20% случаев, может возникать в любом возрасте. Причиной развития становится химиотерапия или радиотерапия по поводу какого-то онкологического заболевания. В число лекарственных средств с доказанной способностью вызывать миелодиспластический синдром включают циклофосфан, подофиллотоксины, антрациклины (доксорубицин) и ингибиторы топоизомеразы (иринотекан, топотекан). Вторичный вариант отличается более высокой резистентностью к лечению, более высоким риском развития острого лейкоза и более неблагоприятным прогнозом.
В современной редакции классификации ВОЗ различают следующие типы миелодиспластического синдрома:
Симптомы миелодиспластического синдрома
Клиническая симптоматика определяется степенью нарушений миелопоэза. При мягко протекающих расстройствах возможно длительное бессимптомное или стертое течение. Из-за слабой выраженности клинических проявлений некоторые больные не обращаются к врачам, и миелодиспластический синдром обнаруживается во время проведения очередного медицинского осмотра. При преобладании анемии наблюдаются слабость, одышка, плохая переносимость физических нагрузок, бледность кожных покровов, головокружения и обморочные состояния.
При миелодиспластическом синдроме с тромбоцитопенией возникает повышенная кровоточивость, отмечаются десневые и носовые кровотечения, на коже появляются петехии. Возможны подкожные кровоизлияния и меноррагии. Миелодиспластический синдром с выраженными нейтропенией и агранулоцитозом проявляется частыми простудами, стоматитом, синуситом или стрептодермией. В тяжелых случаях возможно развитие пневмонии или сепсиса. Инфекционные заболевания нередко вызываются грибками, вирусами или условно-патогенными микробами. У каждого пятого пациента с миелодиспластическим синдромом выявляется увеличение лимфоузлов, селезенки и печени.
Диагностика миелодиспластического синдрома
При исследовании костного мозга количество клеток обычно нормальное либо повышенное. Уже на ранних стадиях обнаруживаются признаки дизэритропоэза. Количество бластов зависит от формы миелодиспластического синдрома, может быть нормальным либо увеличенным. В последующем наблюдаются дисгранулоцитопоэз и дисмегакариоцитопоэз. У некоторых больных признаки дисплазии костного мозга выражены очень слабо. В процессе цитогенетического исследования у ¾ больных выявляются хромосомные нарушения. Дифференциальный диагноз миелодиспластического синдрома проводят с В12-дефицитной анемией, фолиево-дефицитной анемией, апластической анемией, острым миелолейкозом и другими острыми лейкозами.
Лечение и прогноз при миелодиспластическом синдроме
Тактика лечения определяется выраженностью клинической симптоматики и лабораторных изменений. При отсутствии явных признаков анемии, геморрагического синдрома и инфекционных осложнений осуществляется наблюдение. При миелодиспластическом синдроме с выраженной анемией, тромбоцитопенией и нейтропенией, а также при высоком риске возникновения острого лейкоза назначают сопроводительную терапию, химиотерапию и иммуносупрессивную терапию. При необходимости осуществляют пересадку костного мозга.
Сопроводительная терапия является самым распространенным методом лечения миелодиспластического синдрома. Предусматривает внутривенные инфузии компонентов крови. При длительном применении может провоцировать повышение уровня железа, влекущее за собой нарушения деятельности жизненно важных органов, поэтому переливания гемокомпонентов производят при одновременном приеме хелаторов (лекарственных средств, связывающих железо и способствующих его выведению).
Иммуносупрессоры эффективны при лечении миелодиспластического синдрома с отсутствием хромосомных аномалий, наличием гена HLA-DR15 и гипоклеточном костном мозге. Химиотерапию применяют при невозможности трансплантации костного мозга. Высокие дозы препаратов используют при трансформации миелодиспластического синдрома в острый лейкоз, а также при рефрактерных анемиях с избытком бластов при нормоклеточном и гиперклеточном костном мозге, низкие – при невозможности пересадки костного мозга. Наряду с перечисленными средствами пациентам назначают гипометилирующие средства (азацитидин). Наиболее надежным способом достижения полноценной длительной ремиссии является трансплантация костного мозга.
Прогноз зависит от типа миелодиспластического синдрома, количества хромосомных аномалий, необходимости в регулярных переливаниях компонентов крови, выраженности клинических проявлений и наличия осложнений. Различают 5 групп риска. Средняя выживаемость больных миелодиспластическим синдромом, входящих в группу с самым низким уровнем риска, составляет более 11 лет; с самым высоким – около 8 месяцев. Вероятность отторжения костного мозга после трансплантации – около 10%.